
科目: 来源: 题型:
【题目】减少NO2、SO2、CO等有害气体对大气环境的危害,是人类的共同追求。
(1)在原子经济学原则引导下,化学家用CO与H2在加热加压条件合成了液体燃料甲醇,其化学反应方程式为__。
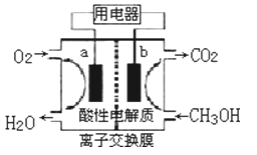
(2)以甲醇做燃料的电池,如图所示,其负极是__(填a或b),负极的反应式为___,正极的反应式为___。该燃料电池在理想状态下,将有96.5%的化学能转化成电能,即消耗1mol液体甲醇所能产生的最大电能达702.1kJ,则通常甲醇燃烧的热化学反应方程式为__。
(3)已知:NO2(g)+SO2(g)SO3(g)+NO(g) △H=+41.8kJmol﹣1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是___。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1molSO3的同时生成1molNO2
当上述反应平衡时,测得NO2与SO2体积比为1:6,则平衡常数K=__。当给已达平衡状态的上述反应升温时,平衡常数K′__。(变大、变小或不变)
查看答案和解析>>
科目: 来源: 题型:
【题目】研究和深度开发CO、CO2的应用具有重要的社会意义。回答下列问题:
I.CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H1=akJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=bkJ/mol
则反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)的△H=__kJ/mol。
Ⅱ.某温度下,在容积为2L的密闭容器中投入8molCO2(g)、16molH2(g)发生反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),15min后达到平衡,此时CO2的转化率为75%。则
CO(g)+H2O(g),15min后达到平衡,此时CO2的转化率为75%。则
①0~15min内用二氧化碳表示平均反应速率v(CO2)=__,
②计算此条件下该反应的平衡常数K=__。
Ⅲ.捕碳技术是指从空气中捕获二氧化碳的各种科学技术的统称。目前NH3和(NH4)2CO3等物质已经被用作工业捕碳剂。
(1)下列物质中能作为CO2捕获剂的是__。
A.Na2CO3 B.NaOH C.CH3CH2OH D.NH4Cl
(2)用(NH4)2CO3捕碳的反应:(NH4)2CO3(aq)+H2O(1)+CO2(g)![]() 2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充人一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充人一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
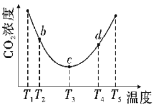
b、c、d三点的平衡常数Kb、Kc、Kd从大到小的顺序为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为:Li1﹣xCoO2+LixC6═LiCoO2+C6(x<1),下列关于该电池的说法不正确的是( )
A.放电时,Li+在电解质中由负极向正极迁移
B.放电时,负极的电极反应式为LixC6﹣xe﹣═xLi++C6
C.充电时,若转移1mole﹣,石墨(C6)电极将增重7xg
D.充电时,阳极的电极反应式为LiCoO2﹣xe﹣═Li1﹣xCoO2+xLi+
查看答案和解析>>
科目: 来源: 题型:
【题目】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为__;第一电离能I1(Si)__I1(Ge)(填>或<)。
(2)基态Ge原子核外电子排布式为__;SiO2、GeO2具有类似的晶体结构,其中熔点较高的是__。
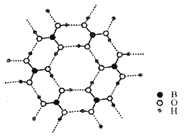
(3)如图为H3BO3晶体的片层结构,其中B的杂化方式为__;硼酸在热水中比在冷水中溶解度显著增大的主要原因是__。
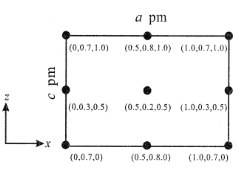
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形),晶胞参数为apm、bpm和和cpm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为__;CsSiB3O7的摩尔质量为Mg.mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为__g·cm-3(用代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种利用生物电化学方法脱除水体中NH4+的原理如图所示。
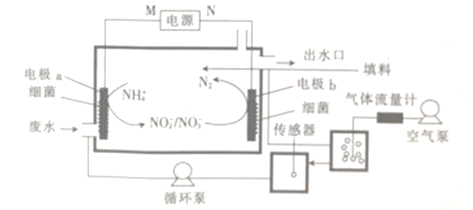
下列说法正确的是
A. M为电源的负极,N为电源的正极
B. 装置工作时,电极a周围溶液的pH降低
C. 装置内工作温度越高,NH4+的脱除率一定越大
D. 电极b上发生的反应之一为2NO2-+8H++8e-=N2↑+4H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如图。
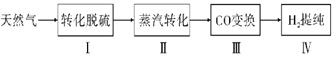
请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T·F菌作用下,酸性环境中脱硫过程示意图如下。
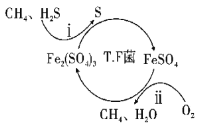
(1)过程i的离子反应方程式为__。
(2)已知:
①Fe3+在pH=1.9时开始沉淀pH=3.2时沉淀完全。
②30℃时,在T·F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
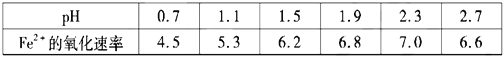
下列说法正确的是___
A.在转化脱硫中,最佳的pH范围是1.5<pH<1.9
B.在转化脱硫中需要不断补充Fe2(SO4)3
C.在转化脱硫中是O2间接地把H2S氧化为S
D.在转化脱硫中CH4作为还原剂被氧化
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。

(3)①该过程的热化学方程式是__。
②比较压强p1和p2的大小关系:p1__p2(选填“<”、“>”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.提纯:将CO2和H2分离得到H2的过程示意图如图。
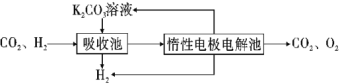
(4)吸收池中发生反应的离子方程式是__。
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A.放电时负极反应为:Zn+2OH--2e-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3+5OH--3e-=FeO42-+4H2O
C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是( )
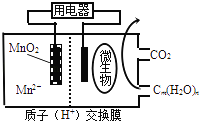
A.放电过程中,H+从正极区移向负极区
B.分子组成为Cm(H2O)n的物质一定是糖类
C.微生物所在电极区放电时发生还原反应
D.左边电极反应式为:MnO2+4H++2e﹣=Mn2++2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2 + 2H2O + 4e == 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H+ + 2e == H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,0.1mol·L-1的某二元酸H2A溶液中,逐渐加入NaOH溶液,可能存在的含A粒子的物质的量分数随pH变化的关系如图所示,下列说法正确的是( )
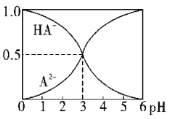
A.H2A的电离方程式:H2A![]() H++HA-
H++HA-
B.pH=5时,在NaHA和Na2A的混合溶液中:c(HA-):c(A2-)=1:100
C.等物质的量浓度的NaHA和Na2A溶液等体积混合,离子浓度大小关系为:c(Na+)>c(A2-)>c(HA-)
D.Na2A溶液必存在c(OH-)=c(H+)+c(HA-)+2c(H2A),各粒子浓度均大于0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com