
科目: 来源: 题型:
【题目】在不同条件下,分别测得反应2SO2+O2![]() 2SO3的化学反应速率,其中表示该反应进行得最快的是( )
2SO3的化学反应速率,其中表示该反应进行得最快的是( )
A.v(SO2)=4 mol·L-1·min-1B.v(O2)=3 mol·L-1·min-1
C.v(SO2)=0.1 mol·L-1·s-1D.v(O2)=0.1 mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化碳酰胺[CO(NH2)2·H2O2]是一种与过氧化氢性质相似的固体氧化剂,因其具有价廉、安全、易于储存、使用方便等优点,被广泛应用于日用化工、食品、建筑、农业等领域。请回答下列问题:
I.过氧化碳酰胺的制备
实验室用尿素和双氧水制备过氧化碳酰胺的步骤如下:取5.0 mL 30% H2O2放入50 mL锥形瓶中,加入1.8 g尿素(H2O2与尿素的物质的量之比为3:2);将装有反应混合物的锥形瓶放入水浴锅中,水浴加热至60 °C,加热几分钟,得到一种澄清、透明的溶液;将溶液转移到大蒸发皿上,在60 °C恒温水浴锅上缓慢蒸发;溶液中缓慢析出针状晶体;当结晶完全后,将针状晶体用滤纸吸去水分,称重,得产品2.5 g。
已知:CO(NH2)2+H2O2=CO(NH2)2·H2O2。
(1)H2O2的电子式为________________________。
(2)水浴加热时温度控制在60 °C最好,其原因为___________________________。
(3)过氧化碳酰胺的产率为___________%(结果保留1位小数)。
II.过氧化碳酰胺的性质
称取0.50g过氧化碳酰胺于试管中,加5mL水溶解。
过氧化碳酰胺的鉴定反应步骤及现象如下:
在试管中加入5滴过氧化碳酰胺溶液、0.5 mL乙醚和2滴2 mol·L-1 H2SO4酸化,再加入2~3滴0.1 mol. L-1K2CrO4溶液.振荡试管,上层呈深蓝色,过氧化氢和重铬酸钾发生非氧化还原反应生成蓝色的CrO5,CrO5在乙醚中稳定,碳酰胺[CO(NH2)2]不和重铬酸钾反应,下层呈绿色,CrO5在水中不稳定,易分解生成Cr(OH)2+和O2。
(4)检验O3可用CrO3与O3反应,得蓝色晶体CrO5:CrO3+O3 →CrO5(未配平),则该反应中氧化剂与还原剂的个数比为_____________。
(5)CrO5在水中分解的离子方程式为_______________。
III.过氧化碳酰胺中活性氧含量的测定(以过氧化氢中氧原子的质量分数计)
准确称量7.5200 g产品,配制成100 mL溶液,用移液管移取10.00 mL溶液于250 mL锥形瓶中,加人适量水和硫酸,用0.1000mol·L-1的酸性高锰酸钾标准溶液平行滴定三次,平均消耗的体积为24.00mL。.
(6)配制100mL过氧化碳酰胺溶液所用到的玻璃仪器有____________,判断滴定至终点的现象为___________________,过氧化碳酰胺中活性氧含量为_____________(结果保留1位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,充分燃烧一定量的丁烷放出热量161.9kJ,经测定完全吸收生成的CO2需消耗5mol/L的KOH溶液100ml,恰好生成正盐,则此条件下热化学方程式:C4H10(g)+![]() O2(g)→4CO2(g)+5H2O(g)的△H为( )
O2(g)→4CO2(g)+5H2O(g)的△H为( )
A. +2590.4kJ/mol B. ﹣2590.4kJ/mol C. +1295.2kJ/mol D. ﹣1295.2kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】难溶性杂卤石(K2SO4MgSO42CaSO42H2O)属于“呆矿”,在水中存在如下平衡
K2SO4MgSO42CaSO42H2O(s)2Ca2++2K++Mg2++4![]() +2H2O
+2H2O
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如图1:
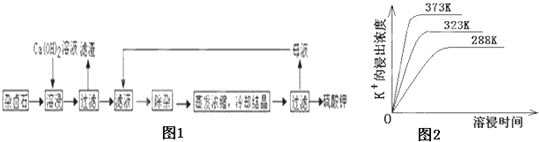
(1)滤渣主要成分有__________和___________以及未溶杂卤石.
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:_______________.
(3)“除杂”环节中,先加入_______溶液,经搅拌等操作后,过滤,再加入________溶液调滤液PH至中性.
(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图2,由图可得,随着温度升高,①__________________________②______________________________;
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+![]() CaCO3(s)+
CaCO3(s)+![]()
已知298K时,Ksp(CaCO3)=2.80×10﹣9,Ksp(CaSO4)=4.90×10﹣5,求此温度下该反应的平衡常数K_____________(计算结果保留三位有效数字).
查看答案和解析>>
科目: 来源: 题型:
【题目】第四周期元素在生产生活中具有重要的作用。请回答下列问题:
(1)基态Sc原子的价电子排布图为___________________。
(2)Zn2+和CN-、K+可组成化合物K2Zn(CN)4,其中存在的化学键类型有____________;Zn(CN)42-中的配体为_______,配位原子为_____ ,与该配离子中配体等电子体的分子为___。
(3)与Br同主族的短周期元素有F、Cl,这三种元素的简单氢化物HF、HCl、HBr的沸点从高到低的顺序为___________,理由为______。
(4)Fe-Cr-Al合金可作为汽车尾气催化剂的载体,汽车尾气催化剂可将NO2还原为无毒害的气体,防止HNO3型酸雨的形成,NO2的空间构型为_____。HNO3的酸性强于HNO2的原因为____________________。
(5)金属铜采用面心立方堆积方式,其晶胞结构如图所示。已知该晶胞的密度为ρg. cm-3,晶胞参数为anm,阿伏伽德罗常数为NA,则铜原子的相对原子质量的表达式为_______(用含有ρ、a、NA的表达式表示)。
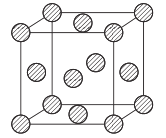
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2是一种常用的化工原料,可应用于化学和食品加工过程的惰性保护、焊接气体、植物生长刺激剂,在铸造中用于硬化模和芯子及用于气动器件,还应用于杀菌气的稀释剂。请回答下列问题:
I.我国中科院研究所利用CO2与环氧丙烷(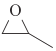 )合成生物降解聚碳酸酯(PPC)和聚(碳酸酯-醚)多元醇,则环氧丙烷中碳元素的平均化合价为____,CO2 的结构式为_________。
)合成生物降解聚碳酸酯(PPC)和聚(碳酸酯-醚)多元醇,则环氧丙烷中碳元素的平均化合价为____,CO2 的结构式为_________。
II.CO2 与H2反应可用于生产甲醇
(1)已知氢气与甲醇的燃烧热分别为a kJ·mol-1、b kJ·mol-1 , H2O(g)= H2O(l) △H=c kJ·mol-1 ,CH3OH(g)=CH3OH(l) H=d kJ·mol-1,则CO2与H2反应产生气态甲醇与气态水的热化学方程式为__________________________。
(2)取一定体积的CO2和H2的混合气体,加入恒容密闭容器中,发生上述反应,相同时间内,测得甲醇的体积分数![]() (CH3OH)与反应温度T的关系如图1所示,则该反应的
(CH3OH)与反应温度T的关系如图1所示,则该反应的![]() (CH3OH)随反应温度T变化的原因为_______________。
(CH3OH)随反应温度T变化的原因为_______________。
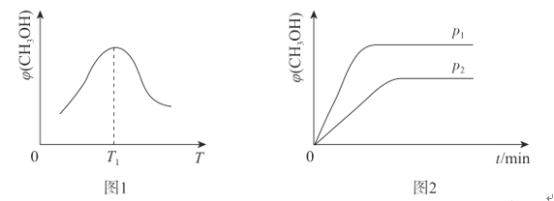
(3)温度为T时,向体积分别为V1、V2的甲.乙两容器中充人相同量的CO2和H2的混合气体,经过一段时间两容器均达到平衡,测得压强分别为p1、p2,如图2所示,则p1_____(填“>”“<”或“=”)p2。
(4)一定温度下,在1 L的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 kPa,发生上述反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
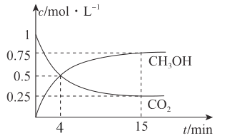
①反应进行到4 min 时,v(正)________ (填“>”“<"或“=”)v(逆)。0~4 min,H2 的平均反应速率v(H2)=______ mol· L-1·min- 1。
②CO2平衡时的体积分数为____________,该温度下Kp=________ (可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压代替平衡浓度计算,分压=总压×物质的量分数
查看答案和解析>>
科目: 来源: 题型:
【题目】H2A为二元弱酸,常温下,向一定体积的0.1 mol·L-1的H2A溶液中逐滴加入一定浓度的NaOH溶液,溶液中不同形态的粒子(H2A、HA-、A2- )的物质的量分数a(X)随pH的变化曲线如图所示,![]()
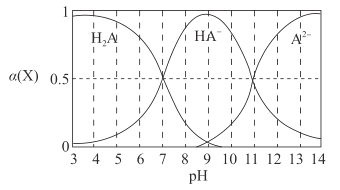
下列说法错误的是
A.K1(H2A)=1.0×10 -7B.K2(H2A)=1.0×10-11
C.pH=9时,c(Na+ )<c(HA- )+ 2c(H2A)D.pH=7时,c(Na+ )=c(H2A)+2c(A2- )
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨反应![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g) ![]() NH3(g) △H 的反应机理如图所示,图中“吸”表示各气态物质在催化剂表面吸附。下列说法错误的是
NH3(g) △H 的反应机理如图所示,图中“吸”表示各气态物质在催化剂表面吸附。下列说法错误的是
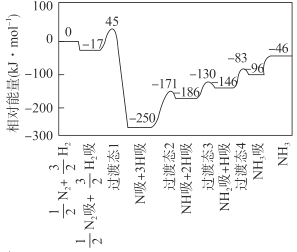
A.该反应的△H = -46 kJ·mol- 1
B.该反应机理中最大活化能为79 kJ·mol- 1
C.升高温度,该反应过渡态的能量会增大
D.该反应达到平衡后增大压强反应正向进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com