
科目: 来源: 题型:
【题目】亚甲基蓝(Methylnene Blue)在碱性条件下与葡萄糖作用生成亚甲基白(Methylene White),亚甲基蓝的结构简式:
著名的蓝瓶子实验操作步骤如下:
①如图示在250mL锥形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,搅拌溶解后,再加入3滴~5滴0.2%的亚甲基蓝溶液,振荡混合液呈现蓝色;
②塞紧橡皮塞(活塞a、b关闭),将溶液静置,溶液变为无色;
③再打开瓶塞,振荡,溶液又变为蓝色;
④再塞紧橡皮塞,将溶液静置,溶液又变为无色,以上③、④可重复多次。
试回答下列问题:

(1)某学生将起初配得的蓝色溶液分装在A,B两支试管中(如上图,A试管充满溶液,B中有少量溶液),塞上橡皮塞静置片刻,两溶液均显无色,若再同时振荡A,B试管,能显蓝色的是_________(填“A”或“B”);
(2)若塞紧锥形瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色_________(填“能”或“不能”);若塞紧锥形瓶塞并打开a、b通入足量氧气,溶液能否由无色变为蓝色_________(填“能”或“不能”);
(3)上述转化过程中,葡萄糖的作用是_________,亚甲基蓝的作用是_________;
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为维生素C具有_____;
(5)该实验中③、④操作能否无限次重复进行_________(填“能”或“不能”),理由是 _____。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )

A.Z单质与氢气反应较Y剧烈
B.X与W的原子核外电子数相差9
C.X单质氧化性强于Y单质
D.最高价氧化物对应水化物酸性W比Z强
查看答案和解析>>
科目: 来源: 题型:
【题目】硫化氢与浓硫酸发生如下反应:H2S+H2SO4(浓)→S↓+SO2↑+2H2O加热条件下,单质硫与浓硫酸又会发生如下反应:S+2H2SO4(浓)![]() 3SO2↑+2H2O
3SO2↑+2H2O
计算:
(1)若98%浓硫酸可表示为H2SO4aH2O,则a=__;若要把该浓硫酸转化为H2SO4H2O,则98%浓硫酸与加入水的质量比为_____。
(2)一定条件下,将0.1mol H2S气体通入足量浓硫酸中,生成b mol SO2,则 b的取值范围是_______。
(3)在50mL、4.0mol/L的NaOH溶液中,通入H2S气体并充分反应,然后,小心蒸发,得到不含结晶水的白色固体.通入H2S的物质的量为x mol,生成的白色固体的质量为7.9g,通过计算确定白色固体的可能成分及每种成分的质量(结果保留一位小数)_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外兴趣小组探究利用废铜屑制取CuSO4溶液,设计了以下几种实验方案。完成下列填空:
(1)方案一:以铜和浓硫酸反应制备硫酸铜溶液。方案二:将废铜屑在空气中灼烧后再投入稀硫酸中。和方案一相比,方案二的优点是________________________;方案二的实验中,发现容器底部残留少量紫红色固体,再加入稀硫酸依然不溶解,该固体为________。
(2)方案三的实验流程如图所示。
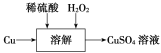
溶解过程中有气体放出,该气体是________。随着反应的进行,生成气体速率加快,推测可能的原因是________________________________________________________________________________。
(3)设计实验证明你的推测:______________________________。
方案四的实验流程如图所示。
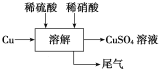
(4)为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为________;
(5)对方案四进行补充完善,设计一个既能防止污染,又能实现物料循环的实验方案(用流程图表示)__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,发生如下反应:4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)
完成下列填空:
(1)写出该反应的平衡常数表达式K=______。若只改变一个影响化学平衡的因素,则下列关于平衡常数K与化学平衡移动关系的叙述正确的是______(填序号)。
a.K值不变,平衡不移动
b.K值变化,平衡一定移动
c.平衡移动,K值可能不变
d.平衡移动,K值一定变化
(2)若反应在恒容密闭容器中进行,能说明该反应已达到平衡状态的是_____(填序号)。
a.υ正(NO2)=2υ正(NO)
b.NO和Cl2的物质的量之比不变
c.混合气体密度保持不变
d.c (NO2):c (NO):c (Cl2)=4:2:1
(3)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和适量NaCl固体,10min时反应达到平衡.测得10min内υ(NO2)=0.015mol/(Lmin),则平衡后n (Cl2)=______mol,此时NO2的转化率为а1;保持其它条件不变,扩大容器的体积,当反应再次达到平衡时NO2的转化率为а2,则а2_____а1(选填“>”、“<”或“=”)。
实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH→NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得到1L溶液A,溶液B为0.1mol/L的CH3COONa溶液。
(4)两溶液中c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为________________。
(5)可使溶液A和溶液B的pH相等的方法是__________(填序号)。
a.向溶液A中加适量水
b.向溶液A中加适量NaOH
c.向溶液B中加适量水
d.向溶液B中加适量NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表中第VIIA族元素的单质及其化合物的用途广泛.完成下列填空:
(1)与氯元素同族的短周期元素的原子核外有___种不同能量的电子.
(2)能作为溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是___(填序号).
a.IBr中溴为﹣1价 b.HBr、HI的酸性c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)海水提溴过程中,先向浓缩海水中通入_____,将其中的Br﹣氧化,再用“空气吹出法”吹出Br2,并用纯碱吸收.已知纯碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),则吸收1mol Br2,转移电子_____mol,反应中氧化产物为_____.
(4)已知:AlF3的熔点为1040℃,AlCl3在178℃升华.从物质结构的角度解释两者熔点相差较大的原因:__________
(5)HClO有很好的杀菌消毒效果.为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目: 来源: 题型:
【题目】浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
A | B | C | D | |
溶液(Ⅰ) | 盐酸 | 醋酸 | 氢氧化钠 | 氨水 |
溶液(Ⅱ) | 氢氧化钠 | 氢氧化钠 | 氨水 | 硝酸银 |
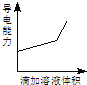
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度.则下列说法正确的是( )
A.物质的量:甲<乙B.气体体积:甲>乙
C.摩尔体积:甲>乙D.相对分子质量:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr![]() C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。
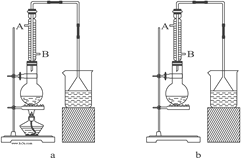
(2)反应装置中的烧瓶应选择下列哪种规格最合适(_____)
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是(_____)
A. A进B出 B. B进A出 C. 从A进或B进均可
(4)可能发生的副反应为:_____________、__________、______________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com