
科目: 来源: 题型:
【题目】已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.H2O(g)= H2(g)+![]() O2(g) ΔH=242 kJ·mol-1
O2(g) ΔH=242 kJ·mol-1
B.2H2(g)+O2(g)= 2H2O(l) ΔH=-484 kJ·mol-1
C.H2(g)+![]() O2(g)= H2O(g) ΔH=242 kJ·mol-1
O2(g)= H2O(g) ΔH=242 kJ·mol-1
D.2H2(g)+O2(g)= 2H2O(g) ΔH=484 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】高分子聚合物P的合成路线如图:

(1)写出反应所需试剂与条件。反应①___;反应⑦___。
(2)写出反应类型:反应③___;反应⑥___。
(3)写出结构简式.E___;P___。
(4)设计反应⑥⑦的目的是___。
(5)写出用1,3-丁二烯与乙酸为原料合成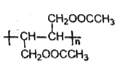 的合成路线(无机原料任选)___。
的合成路线(无机原料任选)___。
(合成路线的常用表示方法为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的定容容器中,当下列的物理量不再发生变化时,表明反应A(固)+2B(气)![]() C(气)+D(气)已达到平衡状态的是( )
C(气)+D(气)已达到平衡状态的是( )
A. 混合气体的压强 B. 混合气体的密度
C. 气体的总物质的量 D. A的物质的量浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】氯吡格雷(clopidogrel)是一种用于抑制血小板聚集的药物.以芳香族化合物A为原料合成的路线如下:
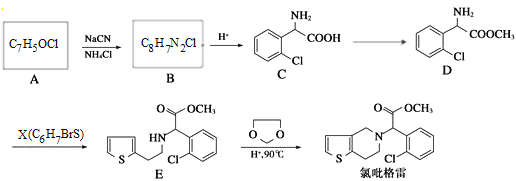
已知:①R-CHO![]() ,②R-CN
,②R-CN![]() RCOOH
RCOOH
(1)写出反应C→D的化学方程式______________,反应类型____________。
(2)写出结构简式.B____________,X____________。
(3)A属于芳香族化合物的同分异构体(含A)共有______种,写出其中与A不同类别的一种同分异构体的结构简式___________。
(4)两分子C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环,写出该反应的化学方程式________________。
(5)已知:![]() ,设计一条由乙烯、甲醇为有机原料制备化合物
,设计一条由乙烯、甲醇为有机原料制备化合物![]() 的合成路线流程图,无机试剂任选_____________。(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A
的合成路线流程图,无机试剂任选_____________。(合成路线常用的表反应试剂A反应条件B…反应试剂反应条件目标产物示方式为:A![]() B…
B…![]() 目标产物)
目标产物)
查看答案和解析>>
科目: 来源: 题型:
【题目】氯的原子序数为17,35Cl是氯元素的一种核素,下列说法正确的是
A.35Cl原子所含质子数为18B.![]() mol的1H35Cl分子所含中子数约为6.02×1023
mol的1H35Cl分子所含中子数约为6.02×1023
C.3.5 g的35Cl2气体的体积为2.24 LD.35Cl2气体的摩尔质量为71 g / mol
查看答案和解析>>
科目: 来源: 题型:
【题目】下列属于氧化还原反应的是( )
A.MgCl2 + Ba(OH)2 == BaCl2 + Mg(OH)2↓B.CO2 + 2NaOH == Na2CO3 + H2O
C.CaCO3 ![]() CaO + CO2↑D.H2 + CuO ==H2O + Cu
CaO + CO2↑D.H2 + CuO ==H2O + Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要用480mL0.1molL-1的硫酸铜溶液,以下配制方法正确的是( )
A. 称取![]() 胆矾(CuSO4·5H2O),配成500mL溶液
胆矾(CuSO4·5H2O),配成500mL溶液
B. 称取![]() 胆矾(CuSO4·5H2O),加入500mL水配成溶液
胆矾(CuSO4·5H2O),加入500mL水配成溶液
C. 称取![]() 无水硫酸铜粉末,加入480mL水配成溶液
无水硫酸铜粉末,加入480mL水配成溶液
D. 称取![]() 无水硫酸铜粉末,加入500mL水配成溶液
无水硫酸铜粉末,加入500mL水配成溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】诺贝尔奖获得者屠呦呦带领团队发现了青蒿素,为中医药科技创新和人类健康事业作出巨大贡献。我国化学家在确认青蒿素分子结构之后实现了青蒿素的全合成。根据信息(部分条件和步骤已省略)回答下列问题:
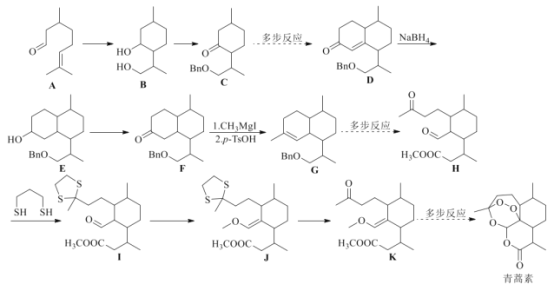
已知:![]() ,按要求回答下列问题:
,按要求回答下列问题:
(1)B的分子式为________________,所含官能团名称为________________________。![]() 的反应类型为________________。
的反应类型为________________。
(2)A的同系物中含碳原子数目最少的物质的结构简式为________________。A的同分异构体X含有醛基和六元碳环,且环上只有一个支链,满足上述条件的X有________种,其中核磁共振氢谱峰数最少的物质的结构简式为________________。
(3)写出A与银氨溶液反应的化学方程式________________________________。
(4)通过![]() 的反应,分子中引入了硫醚基团,而
的反应,分子中引入了硫醚基团,而![]()
![]() 的反应,分子中硫醚基团又被脱去,这样做的目的是________________。
的反应,分子中硫醚基团又被脱去,这样做的目的是________________。
(5)根据青蒿素所含官能团,推测其可能具有的性质________。
a.具有氧化性 b.可发生水解反应 c.易溶于水
(6)参照上述合成路线,写出以![]() 为主要原料,经四步反应制备
为主要原料,经四步反应制备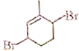 的流程。_____________
的流程。_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠等等,这些物质在实际生活中有广泛的应用,一定条件下相互间能进行转化。
完成下列计算:
(1)将7.8克Na2O2完全溶解于93.8克水中,所得溶液的质量百分比浓度为______。
(2)将11.6克二氧化碳和水蒸汽的混合物与足量的Na2O2充分反应,固体质量增加了3.6克,则原混合气体的平均分子量为______。
(3)向100 mL NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M(不含结晶水)。通入二氧化碳的体积V(标准状况下)与M的质量W的关系如下图所示。
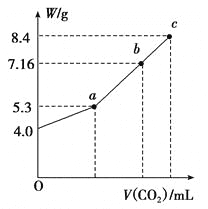
①推断b点时M的组成成份(写出计算过程)____________。
②若向b点的盐溶液中只加入0.03mol某钠的化合物,充分反应后,减压低温蒸发得到无水Na2CO3 8.48g,则加入的物质可以是________或_______。
(4)由31g NaOH和NaHCO3的固体混合物,在密闭密器中加热到250℃,经充分反应后排出气体、冷却,称得剩余固体的质量为N g,试分析不同N值时,剩余固体的组成成份(已知NaHCO3的分解温度低于250℃)。_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,但使用过量会使人中毒.某学习小组针对亚硝酸钠设计了如下实验:
(实验一)制取NaNO2
该小组先查阅资料知:①2NO+Na2O2→2NaNO2;2NO2+Na2O2→2NaNO3;②NO能被酸性高锰酸钾氧化为NO3-,然后设计制取装置如图(夹持装置略去):
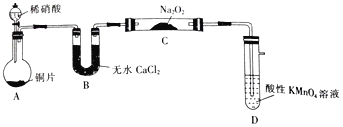
(1)装置D的作用是_______________;如果没有B装置,C中发生的副反应有_______________。
(2)就算在装置气密性良好的情况下进行实验,该小组发现制得的NaNO2的纯度也不高,可能的原因是由_____________;设计一种提高NaNO2纯度的改进措施_________。
(实验二)测定NaNO2样品(含NaNO3杂质)的纯度
先查阅资料知:①5NO2-+2MnO4-+6H+→5NO3-+3Mn2++3H2O;
②MnO4-+5Fe2++8H+→Mn2++5Fe3++4H2O
然后,设计如下方案测定样品的纯度:
样品→溶液A ![]() 溶液B
溶液B ![]() 数据处理
数据处理
(3)取样品2.3 g经溶解后得到溶液A 100 mL,准确量取10.00 mL A与24.00 mL 0.0500 mol/L的酸性高锰酸钾溶液在锥形瓶中充分反应.反应后的溶液用0.1000 mol/L (NH4)2Fe(SO4)2标准溶液滴定至紫色刚好褪去;重复上述实验3次,平均消耗(NH4)2Fe(SO4)2溶液10.00 mL,则样品中NaNO2的纯度为_________.
(4)通过上述实验测得样品中NaNO2的纯度偏高,该小组讨论的原因错误的是_________。(填字母编号)
a.滴定至溶液紫色刚好褪去,立即停止滴定
b.加入A与KMnO4溶液前的锥形瓶未经干燥
c.实验中使用的(NH4)2Fe(SO4)2溶液暴露在空气中的时间过长
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com