
【题目】高分子聚合物P的合成路线如图:

(1)写出反应所需试剂与条件。反应①___;反应⑦___。
(2)写出反应类型:反应③___;反应⑥___。
(3)写出结构简式.E___;P___。
(4)设计反应⑥⑦的目的是___。
(5)写出用1,3-丁二烯与乙酸为原料合成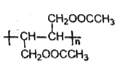 的合成路线(无机原料任选)___。
的合成路线(无机原料任选)___。
(合成路线的常用表示方法为:A![]() B……
B……![]() 目标产物)
目标产物)
【答案】氯气、光照 氢氧化钠的醇溶液、加热 消去反应 加成反应 HOCH2CH=CHCH2OH  或
或 防止碳碳双键被氧化
防止碳碳双键被氧化 
【解析】
结合C的结构简式可知C7H8为![]() ,由转化关系可知,甲苯与氯气在光照条件下发生取代反应生成C7H7Cl为
,由转化关系可知,甲苯与氯气在光照条件下发生取代反应生成C7H7Cl为![]() ,再发生水解反应得到A为
,再发生水解反应得到A为![]() ,苯甲醇与乙二醇褪去1分子式水得到B为
,苯甲醇与乙二醇褪去1分子式水得到B为![]() ,B发生消去反应生成C(
,B发生消去反应生成C(![]() ).根据G的结构简式与转化关系可知,C4H6为CH2=CHCH=CH2,与溴发生1,4-加成生成D为BrCH2CH=CHCH2Br,D发生水解反应得到E为HOCH2CH=CHCH2OH,E发生与HCl发生加成反应得到F为HOCH2CH2CHClCH2OH,F发生氧化反应得到G,G发生消去反应、酸化得到I为HOOCCH=CHCOOH,则H为NaOOCCH=CHCOONa,H和C发生加聚反应生成P,则P的结构简式为:
).根据G的结构简式与转化关系可知,C4H6为CH2=CHCH=CH2,与溴发生1,4-加成生成D为BrCH2CH=CHCH2Br,D发生水解反应得到E为HOCH2CH=CHCH2OH,E发生与HCl发生加成反应得到F为HOCH2CH2CHClCH2OH,F发生氧化反应得到G,G发生消去反应、酸化得到I为HOOCCH=CHCOOH,则H为NaOOCCH=CHCOONa,H和C发生加聚反应生成P,则P的结构简式为: ;
;
(5)要合成 ,可有CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH可与CH3COOH发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,而CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,由此确定合成流程路线。
,可有CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH可与CH3COOH发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,而CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,由此确定合成流程路线。
(1)反应①是甲苯与氯气在光照条件下生成![]() ,反应⑦是HOOCCH2CHClCOOH在氢氧化钠醇溶液、加热条件下发生的消去反应;
,反应⑦是HOOCCH2CHClCOOH在氢氧化钠醇溶液、加热条件下发生的消去反应;
(2)反应③为![]() 发生消去反应生成
发生消去反应生成![]() ;反应⑥为HOCH2CH=CHCH2OH与HCl发生加成反应得到HOCH2CH2CHClCH2OH,;
;反应⑥为HOCH2CH=CHCH2OH与HCl发生加成反应得到HOCH2CH2CHClCH2OH,;
(3)E的结构简式为HOCH2CH=CHCH2OH,P的结构简式为: ;
;
(4)反应中⑦中将羟基氧化为羧基,也可以氧化碳碳双键,设计反应⑥⑦的目的是:保护碳碳双键,防止被氧化;
(6)要合成 ,可由CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH与CH3COO发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,另外CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,则用1,3-丁二烯与乙酸为原料合成
,可由CH3COOCH2CH=CHCH2OCOCH3发生加聚反应得到,而HOCH2CH=CHCH2OH与CH3COO发生酸化反应得到CH3COOCH2CH=CHCH2OCOCH3,另外CH2=CH-CH=CH2与Br2发生1,4-加成后,再水解即可制得HOCH2CH=CHCH2OH,则用1,3-丁二烯与乙酸为原料合成 的合成路线为
的合成路线为 。
。


科目:高中化学 来源: 题型:
【题目】某科研团队研究将磷钨酸(H3PW12O40,以下简称HPW)代替浓硫酸作为酯化反应的催化剂,但HPW自身存在比表面积小、易溶于有机溶剂而难以重复使用等缺点,将其负载在多孔载体(如硅藻土、C等)上则能有效克服以上不足,提高其催化活性。用HPW负载在硅藻土上催化制取乙酸正丁酯的酯化率与HPW负载量的关系(温度:120℃,时间:2h)如图所示,下列说法不正确的是
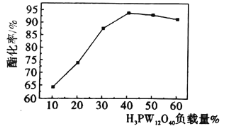
A.与HPW相比,HPW/硅藻土比表面积显著增加,有助于提高其催化性能
B.当HPW负载量为40%时达到饱和,酯化率最高
C.用HPW/硅藻土代替传统催化剂,可减少设备腐蚀等不足
D.不同催化剂对酯化率的影响程度主要取决于化学反应正向进行的程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积)。关于该固体混合物,下列说法正确的是

A. 一定含有Al,其质量为4.05g
B. 一定不含FeCl2,可能含有MgCl2和AlCl3
C. 一定含有MgCl2 和FeCl2
D. 一定含有(NH4)2SO4 和MgCl2,且物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最高的金属元素,其单质及其化合物在生产生活中的应用十分广泛。
(1)铝原子最外层电子排布式是________,铝原子核外有___种能量不同的电子。
(2)1827年,德国化学家维勒用金属钾与无水氯化铝反应而制得了金属铝。不用钾与氯化铝溶液制铝的理由是_________;现代工业炼铝是以Al2O3为原料,与冰晶石(Na3A1F6)在熔融状态下进行电解,其阴极电极反应式为___________________________。
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:2Al+4BaO![]() 3Ba↑+BaO·Al2O3,用化学平衡移动原理解释上述方法可制取金属Ba的原因是________。
3Ba↑+BaO·Al2O3,用化学平衡移动原理解释上述方法可制取金属Ba的原因是________。
(4)LiAlH4由Li+、A1H4-构成,是有机合成中常用的试剂,LiAlH4在125℃分解为LiH、H2和Al。
①比较Li+、 H-、Al3+、H+离子半径大小____________。
②写出LiAlH4分解的方程式(需配平)_______,若反应生成3.36 L氢气(标准状况下),则有____g铝生成。
③LiAlH4与乙醛反应可生成乙醇,推断LiAlH4是反应的_________剂。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要用480mL0.1molL-1的硫酸铜溶液,以下配制方法正确的是( )
A. 称取![]() 胆矾(CuSO4·5H2O),配成500mL溶液
胆矾(CuSO4·5H2O),配成500mL溶液
B. 称取![]() 胆矾(CuSO4·5H2O),加入500mL水配成溶液
胆矾(CuSO4·5H2O),加入500mL水配成溶液
C. 称取![]() 无水硫酸铜粉末,加入480mL水配成溶液
无水硫酸铜粉末,加入480mL水配成溶液
D. 称取![]() 无水硫酸铜粉末,加入500mL水配成溶液
无水硫酸铜粉末,加入500mL水配成溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO![]() 2CO2+N2(降温后该反应的平衡常数变大)为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2(降温后该反应的平衡常数变大)为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 1.00×10﹣3 | 4.50×10﹣4 | 2.50×10﹣4 | 1.50×10﹣4 | 1.00×10﹣4 | 1.00×10﹣4 |
c(CO)(mol/L) | 3.60×10﹣3 | 3.05×10﹣3 | 2.85×10﹣3 | 2.75×10﹣3 | 2.70×10﹣3 | 2.70×10﹣3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)反应的Q___0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=___。
(3)计算在该温度下,反应的平衡常数K=___。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是___。
A.选用更有效的催化剂
B.升高反应体系的温度
C.降低反应体系的温度
D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | ___ | ___ | ___ | 124 |
Ⅲ | 350 | ___ | ___ | 124 |
①请在上表空格中填入剩余的实验条件数据。
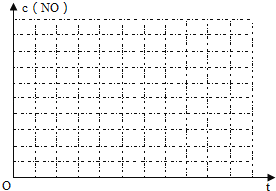
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水硫酸铜在加热条件下能发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气。某学生试图用如图所示装置来确定该化学反应中各物质的计量关系。
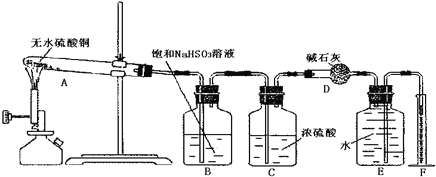
试回答:
(1)加热过程中,试管A中发生的实验现象可能有___。
(2)装置E和F的作用是___;
(3)该学生使用装置B的本意是除去混合气体中的三氧化硫以提纯氧气,他的做法正确吗?为什么?___。
(4)另一学生将9.6g无水硫酸铜充分加热使其完全分解后,用正确的实验方法除去了生成物中的二氧化硫和三氧化硫,最后测出氧气的体积为448mL(标准状况)。据此可计算出二氧化硫为___mol,三氧化硫为___mol。
(5)由上述实验数据可知无水硫酸铜受热分解的化学方程式:___。
(6)上述装置可以简化而不影响实验效果。请你提出一个简化方案,达到使装置最简单而不影响实验效果的目的:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬是一种氧气吸收剂, 通常以二水盐[Cr(CH3COO)2]2 ·2H2O(式量:376)的形式存在,难溶于冷水,易溶于盐酸。其制备原理和实验装置:
制备原理:![]()
实验装置:(如图所示)
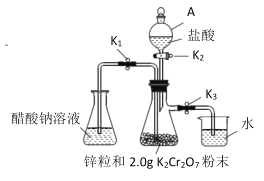
(1)仪器 A 的名称是__________。
(2)装好试剂后按上述装置进行实验,完成下表内容。
操作步骤 | 实验现象 | 发生反应的离子方程式 |
关闭①___________________,打开②_______________,(用K1、K2、K3填写,下同)使盐酸缓慢加入至抽滤瓶中 | 抽滤瓶中锌粒溶解,溶液由橙色逐渐变成蓝色,有少量气泡 | ③________,Zn+2H+=Zn2++H2↑ |
抽滤瓶中产生大量气体时快速加入适量盐酸,关闭K2和④__________________,打开⑤_________ | 抽滤瓶中⑥____________ | Zn+2H+=Zn2++H2↑ |
当溶液完全转移后,迅速塞紧锥形瓶,用冷水冷却 | 锥形瓶中有深红色晶体析出 | ⑦_____________ |
(3)洗涤产品后干燥、称量,得到 1.0g 固体。列式表示产率:____(不必计算出结果,K2Cr2O7 式量:294)。在实验中如果盐酸过量,会导致产率偏________。(填“高”或“低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁元素是最重要的金属元素之一,其不仅是各种钢材的主要成分,很多含铁化合物也具有重要意义。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于_________区。
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:_________。Mn2+的半径_________ Fe3+的半径(填“>”、“<”或“=”)。
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为_________(用含π的式子表示)。
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为_________;[Fe(SCN)(H2O)5]2+中Fe3+的配位数为_________,H2O中氧原子的杂化方式为_________。
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H![]() )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π),则C5H
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π),则C5H![]() 的大π键表示为________。二茂铁是黄色针状晶体,熔点173 ℃(在100 ℃时开始升华),沸点249 ℃,在水中难溶,但可溶于很多有机溶剂。下列相互作用中,二茂铁晶体中不存在的是________(填标号)。
的大π键表示为________。二茂铁是黄色针状晶体,熔点173 ℃(在100 ℃时开始升华),沸点249 ℃,在水中难溶,但可溶于很多有机溶剂。下列相互作用中,二茂铁晶体中不存在的是________(填标号)。
A 离子键 B 配位键 C σ 键 D 范德华力
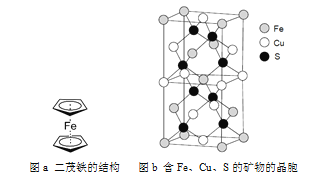
(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为_________。若晶胞的底面边长为A pm,高为C pm,阿伏伽德罗常数为NA,则该晶体的密度为__________ g/cm3(写出表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com