
科目: 来源: 题型:
【题目】由1.3-丁二烯可制备醇酸树脂的原料M以及杀菌剂N,其合成路线如图:
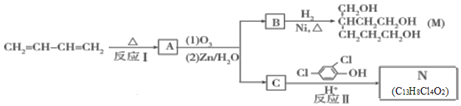
已知:i.Diels-AIder反应: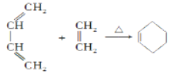
ii.RHC=CHR′![]() RCHO+ R′CHO(R、R′代表羟基或氢)
RCHO+ R′CHO(R、R′代表羟基或氢)
iii.A是一个六元环状化合物;lmol C能与2mol![]() 反应生成N。
反应生成N。
(1)N中含有的官能团名称为_______。
(2)CH2=CH—CH=CH2 能发生加聚反应生成顺式聚合物,请写出该顺式聚合物的结构简式:________。
(3)反应I的化学方程式是__________;该反应的反应类型为_________。
(4)lmol B完全转化成M所消耗的H2的质量是______g。
(5)反应II的化学方程式是________.
(6)A的某些同分异构体在相同的反应条件下也能生成B和C,写出其中一种同分异构体的结构简式:_____。
(7)已知:乙快与1, 3-丁二烯也能发生Diels-AIder反应。请以1, 3-丁二烯和乙炔为原料,选用必要的无机试剂合成丙二酸,写出合成路线________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件。
查看答案和解析>>
科目: 来源: 题型:
【题目】含镁、氮、磷、砷等元素的化合物在化工生产、药物化学及催化化学等领域应用广泛。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_____(填序号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(2)晶格能又叫点阵能。它是1mol 离子化合物中的正、负离子从相互分离的气态结合成离子晶体时所放出的能量。MgO 晶格能可通过如图所示的Borm Haber循环计算得到。
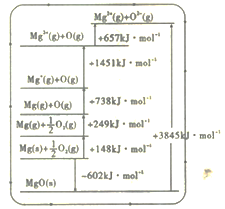
Mg的第二电离能为______kJ·mol-1;MgO的晶格能为___________kJ·mol-1。
(3)乙二胺(H2NCH2CH2NH2) 是一种有机化合物,其中N原子的杂化类型是____,该有机化合物能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是______,其中与乙二胺形成的化合物稳定性相对较高的是_______(填 “Mg2+ ”或“Cu2+” )。
(4) PCl5是一种白色固体,加热到160°C不经过液态阶段就变成蒸气,测得180°C下的蒸气密度(折合成标准状况)为9.3g·L-1,分子的极性为零,P-Cl键长为204pm和211pm两种。在180°C下PCl5蒸气中存在的分子形式为____(填化学式),分子的空间构型为______,P、Cl的电负性由大到小顺序为________。
(5)砷和铟组成的一种化合物属于半导体材料,其晶胞结构如图所示。已知晶胞的参数为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_____g. cm-3 (用含a和NA的代数式表示)。
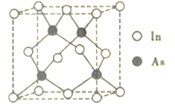
查看答案和解析>>
科目: 来源: 题型:
【题目】5﹣二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5﹣二甲氧基苯酚的部分物理性质见下表:
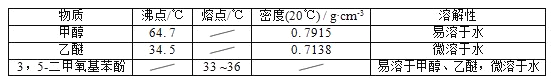
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取,①分离出甲醇的操作是的______;②萃取用到的分液漏斗使用前需__________________并洗净,分液时有机层在分液漏斗的________填(“上”或“下”)层;
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3溶液洗涤的目的是__,用饱和食盐水洗涤的目的是______;
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是__(填字母);
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤.为了防止倒吸,减压过滤完成后应先________________,再______。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:含C=C的物质(烯烃)一定条件下能与水发生加成反应,生成醇(含羟基的烃的衍生物);有机物A-D间存在图示的转化关系。下列说法不正确的是
![]()
A.D结构简式为CH3COOCH2CH3B.A能使酸性高锰酸钾溶液褪色
C.B与乙酸发生了取代反应D.可用B萃取碘水中的碘单质
查看答案和解析>>
科目: 来源: 题型:
【题目】在合成氨工业和硝酸制备工业中,常产生N2O、NO和NO2等氮氧化物造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)在2L密闭容器中通入3mol H2和1mol N2,测得不同温度下,NH3的产率随时间的变化如图所示。
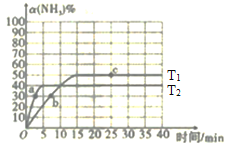
①下列有关说法正确的是________(填序号)。
A.a处的v正>0
B.e点的v净=0
C.由b点到c点混合气体相对分子质量逐渐增大
D.平衡时,通入氩气平衡正向移动
②T2温度时,0~5min内v(N2)=___mol·L-1·min-l
③已知:瞬时速率表达式v正=k正c3(H2)c(N2),v逆=k逆c2(NH3)(k为速率常数,只与温度有关)。温度由T1调到T2,活化分子百分率________。(填“增大”“减小”或“不变”),
k正增大倍数____k逆增大倍数(填“大于”“小于”或“等于”)。T1°C时,![]() ____
____
(2)工业生产尾气中产生的N2O需进行分解处理,用碘蒸气可大大提高N2O的分解速率,反应历程如下:
第一步:I2(g)=2I(g) (快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g) (慢反应)
第三步: IO(g)+N2O(g)→N2(g)+O2(g)+I(g) ( 快反应)
在反应过程中,I2的浓度与N2O分解速率_____ (填“有关”或“无关”);第___步反应对总反应速率起决定性作用;第二步的活化能比第三步____(填 “大”“小”或“相等”)。
(3)已除去N2O的硝酸尾气NO和NO2可用NaOH溶液吸收,写出NO和NO2与NaOH反应生成一种盐的反应方程式:_______;已知,常温下HNO2的电离常数Ka=5×10-4,则0.5mol/L对应钠盐的pH值为_______
查看答案和解析>>
科目: 来源: 题型:
【题目】锰是重要的合金材料和催化剂,在工农业生产和科技领域有广泛的用途。将废旧锌锰电池回收处理后,将含MnO2、MnOOH、Zn(OH)2及少量Fe的废料进行回收处理,能实现资源的再生利用。用该废料制备Zn和MnO2的一种工艺流程如图:

已知:Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
回答下列问题:
(1)还原焙烧过程中,MnOOH与炭黑反应,锰元素被还原为MnO,该反应的化学方程式为_____。
(2)滤渣1主要成分的化学式是________。
(3)净化阶段
①为了除掉滤渣2中的元素,选择最佳的加入试剂为______(填序号)。
A.氯水 B.O2 C.氨水 D.MnCO3
②已知:室温下,Ksp[Mn(OH)2]=10-13,Ksp[Fe(OH)3]=1×10-38,Ksp[Zn(OH)2]=10-17。净化时溶液中Mn2+、Zn2+的浓度约为0. 1mol·L-1,调节pH的合理范围是______。
(4)将MnO2和Li2CO3按4:1的物质的量比配料,混合搅拌,然后升温至600C~750°C, 制取产品LiMn2O4。写出该反应的化学方程式:________。
(5)LiMn2O4材料常制作成可充电电池(如图),该电池的总反应为![]()
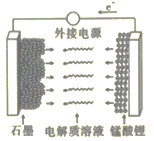
①充电时,锰酸锂为电池的_______(填“正极”“负极”“阴极”或“阳极”);该电极上发生的电极反应式为______________。
②该电池作为电源放电时,若电路中转移0.2mol e-,则石墨电极将减重____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将![]() 转变为
转变为![]() 的方法为( )
的方法为( )
A.与足量的NaOH溶液共热后,再通入CO2
B.溶液加热,通入足量的HCl
C.与稀H2SO4共热后,加入足量的Na2CO3
D.与稀H2SO4共热后,加入足量的NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中的没食子儿茶素(EGC)结构如图所示.关于EGC的下列叙述中正确的是( )
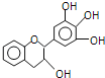
A.EGC的分子式为C15H14O5,属于芳香烃类化合物
B.1molEGC与4molNaOH恰好完全反应
C.该物质能够发生取代反应、加成反应、氧化反应、还原反应、显色反应
D.分子中所有的原子处在同一个平面上
查看答案和解析>>
科目: 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0. 100mol·L-1的NaOH溶液分别滴定10.00mL浓度均为0.100mol·L-1的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
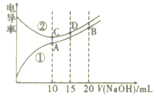
A.曲线②代表滴定CH3COOH溶液的曲线
B.在相同温度下,C、D两点溶液中水的电离程度: C>D
C.取A点溶液1mL加水稀释,溶液中的所有离子浓度都减小
D.B点溶液中: c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
A.异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B.2氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应
C.甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应
D.邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com