科目:gzhx 来源:2015届广东省佛山市质量检测化学试卷(解析版) 题型:填空题
(1)在101kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3kJ•mo1—1、285.8kJ•mo1—1和393.5kJ•mo1—1,则反应C(s)+2H2(g)=CH4(g)的反应热ΔH= 。
(2)已知:2H2(g)+O2(g)=2H2O(g) ΔH1
2H2(g)+O2(g)=2H2O(l) ΔH2
2CO(g)+O2(g)=2CO2(g) ΔH3
①液态水转化为气态水的热化学方程式为 。
②CO和H2分别燃烧生成CO2 (g)和H2O(g),欲得到相同热量,所需CO和H2的体积比是 。
科目:gzhx 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| △H1-△H2 |
| 2 |
| △H1-△H2 |
| 2 |
| △H1 |
| △H3 |
| △H1 |
| △H3 |
科目:gzhx 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:填空题
(16分)
(1)1840年前后,瑞士科学家盖斯(Hess)指出,一个化学反应的热效应,仅与反应物的最初状态及生成物的最终状态有关,而与中间步骤无关,这就是著名的“盖斯定理”。现已知,在101 kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1和393.5 kJ·mol-1,则反应C(s)+2H2(g)= CH4(g)的反应热ΔH=__________,根据以上信息,你认为“盖斯定理”在我们确定一些化学反应的反应热时有何重要意义?__________。
(2)已知:2H2(g)+O2(g)====2H2O(g) ΔH1
2H2(g)+O2(g) ====2H2O(l) ΔH2
2CO(g)+O2(g)====2CO2(g) ΔH3
①写出液态水转化为气态水的热化学方程式:___________________________________。
②CO和H2分别燃烧生成CO2(g)和H2O(g),欲得到相同热量,所需CO和H2的体积比是__________。
科目:gzhx 来源:2012-2013学年广东省汕头市金平区天竺中学高二(上)期中化学试卷(解析版) 题型:解答题
科目:gzhx 来源: 题型:
(16分)
(1)1840年前后,瑞士科学家盖斯(Hess)指出,一个化学反应的热效应,仅与反应物的最初状态及生成物的最终状态有关,而与中间步骤无关,这就是著名的“盖斯定理”。现已知,在101 kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1和393.5 kJ·mol-1,则反应C(s)+2H2(g)= CH4(g)的反应热ΔH=__________,根据以上信息,你认为“盖斯定理”在我们确定一些化学反应的反应热时有何重要意义?__________。
(2)已知:2H2(g)+O2(g)====2H2O(g) ΔH1
2H2(g)+O2(g) ====2H2O(l) ΔH2
2CO(g)+O2(g)====2CO2(g) ΔH3
①写出液态水转化为气态水的热化学方程式:___________________________________。
②CO和H2分别燃烧生成CO2(g)和H2O(g),欲得到相同热量,所需CO和H2的体积比是__________。
科目:gzhx 来源:2011-2012学年广东省梅州市曾宪梓中学高二上学期中考试理综试题(化学部分) 题型:填空题
(16分)
(1)1840年前后,瑞士科学家盖斯(Hess)指出,一个化学反应的热效应,仅与反应物的最初状态及生成物的最终状态有关,而与中间步骤无关,这就是著名的“盖斯定理”。现已知,在101 kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1和393.5 kJ·mol-1,则反应C(s)+2H2(g)= CH4(g)的反应热ΔH=__________,根据以上信息,你认为“盖斯定理”在我们确定一些化学反应的反应热时有何重要意义?__________。
(2)已知:2H2(g)+O2(g)====2H2O(g) ΔH1
2H2(g)+O2(g) ====2H2O(l) ΔH2
2CO(g)+O2(g)====2CO2(g) ΔH3
①写出液态水转化为气态水的热化学方程式:___________________________________。
②CO和H2分别燃烧生成CO2(g)和H2O(g),欲得到相同热量,所需CO和H2的体积比是__________。
科目:gzhx 来源: 题型:
科目:gzhx 来源:2014届河南省平顶山市高二上学期期末考试化学试卷(解析版) 题型:计算题
(1)H2S的燃烧热ΔH = -a kJ·mol-1 ,则H2S燃烧反应的热化学方程式为 。
(2)已知:高温下,在密闭容器中用H2还原WO2可得到金属钨。当温度过高时,WO2(s)会转变为WO2 (g)。请根据以下反应:
WO2 (s) + 2H2 (g) 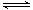 W (s) + 2H2O (g);ΔH = +66.0 kJ· mol-1
W (s) + 2H2O (g);ΔH = +66.0 kJ· mol-1
WO2 (g) + 2H2 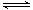 W (s) + 2H2O (g);ΔH =
-137.9 kJ·
mol-1
W (s) + 2H2O (g);ΔH =
-137.9 kJ·
mol-1
计算出WO2
(s) 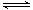 WO2
(g) 的ΔH = ______________________。
WO2
(g) 的ΔH = ______________________。
(3)工业上常利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,反应的化学方程式为:
CH4 + CO2 = 2CO + 2H2
已知CH4、H2和CO的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1、283.0 kJ· mol-1,则生成1 m3(标准状况)CO所需热量为 ;
科目:gzhx 来源: 题型:
| 1 | 2 |
科目:gzhx 来源:2013-2014学年湖北省八校高三第一次联考理综化学试卷(解析版) 题型:选择题
CH4、H2、CO的燃烧热分别为890.31kJ/mol、285.8kJ/mol、110.5 kJ/mol,下列热化学方程式书写正确的是
A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.31kJ/mol
B.2H2(g)+ O2(g)= 2H2O(l) ΔH=-285.8kJ/mol
C.CO (g)+ H2O(g)= CO2(g)+ H2 (g) ΔH=+175.3kJ/mol
D.2CO (g)+ O2(g) = 2CO2(g) ΔH=-221 kJ/mol
科目:gzhx 来源: 题型:
| 光合作用 |
| 催化剂 |
| △ |
| 催化剂 |
| △ |
科目:gzhx 来源: 题型:
| 催化剂 | △ |
科目:gzhx 来源: 题型:
(10分)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I ,II,III)作用下,CH4的产量随光照时间的变化如下图所示。
(1)在O〜30小时内,CH4的平均生成速率和
由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH4最多。
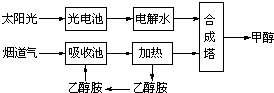
(2) 将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应
CH4(g)+H2O(g)CO(g)+3H2(g) △H=+206kJ·mol-1。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。
(3)该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH⑴的燃烧热分别为
和
,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为_________。
(4)工业上常利用反应CO(g)+2H2(g) CH3OH (g), △H<0合成甲醇,在230°C〜270°C最为有利。为研究合成气最合适的起始组成比n(H2):n(C0),分别在230°C、2500C和2700C进行实验,结果如图。
①2700C的实验结果所对应的曲线是_________(填字母);
②2300C时,工业生产适宜釆用的合成气组成n(H2):n(CO)的比值范围是_________(填字母)。
A. 1 〜1.5 B. 2. 5〜3 C. 3. 5〜4. 5
(5)某同学以石墨为电极,以KOH溶液为电解质设计甲醇燃料电池,其负极的电极反应式为_________。
科目:gzhx 来源:2012届河南省郑州市高三第一次质量预测化学试卷(解析版) 题型:填空题
(10分)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I ,II,III)作用下,CH4的产量随光照时间的变化如下图所示。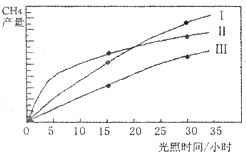
(1) 在O〜30小时内,CH4的平均生成速率 和
和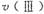 由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH4最多。
由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH4最多。
(2) 将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应
CH4(g)+H2O(g)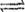 CO(g) +3H2(g) △H=+206kJ·mol-1。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。
CO(g) +3H2(g) △H=+206kJ·mol-1。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。
(3) 该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH⑴的燃烧热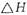 分别为
分别为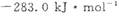 和
和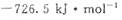 ,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为_________。
,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为_________。
(4)工业上常利用反应CO(g)+2H2(g) 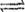 CH3OH (g), △H<0合成甲醇,在230°C〜270°C最为有利。为研究合成气最合适的起始组成比n(H2):n(C0),分别在230°C、2500C和2700C进行实验,结果如图。
CH3OH (g), △H<0合成甲醇,在230°C〜270°C最为有利。为研究合成气最合适的起始组成比n(H2):n(C0),分别在230°C、2500C和2700C进行实验,结果如图。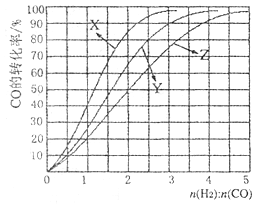
①2700C的实验结果所对应的曲线是_________ (填字母);
②2300C时,工业生产适宜釆用的合成气组成n(H2):n(CO)的比值范围是_________ (填字母)。
A. 1 〜1.5 B. 2. 5〜3 C. 3. 5〜4. 5
(5) 某同学以石墨为电极,以KOH溶液为电解质设计甲醇燃料电池,其负极的电极反应式为_________。
科目:gzhx 来源:2011-2012学年河南省郑州市高三第一次质量预测化学试卷(解析版) 题型:填空题
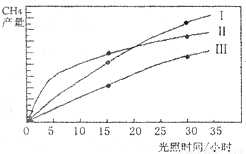
(10分)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I ,II,III)作用下,CH4的产量随光照时间的变化如下图所示。
(1)
在O〜30小时内,CH4的平均生成速率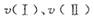 和
和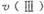 由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH4最多。
由大到小的顺序为_________;反应开始后的15小时内,在第_________种催化剂的作用下,收集的CH4最多。
(2) 将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应
CH4(g)+H2O(g)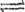 CO(g)
+3H2(g) △H=+206kJ·mol-1。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。
CO(g)
+3H2(g) △H=+206kJ·mol-1。将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,此时测得CO的物质的量为O.10 mol,CH4的平衡转化率为91 %,则此温度下该反应的平衡常数为_________ (计算结果取整数)。
(3)
该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH⑴的燃烧热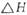 分别为
分别为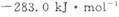 和
和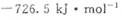 ,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为_________。
,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为_________。
(4)工业上常利用反应CO(g)+2H2(g)
 CH3OH (g), △H<0合成甲醇,在230°C〜270°C最为有利。为研究合成气最合适的起始组成比n(H2):n(C0),分别在230°C、2500C和2700C进行实验,结果如图。
CH3OH (g), △H<0合成甲醇,在230°C〜270°C最为有利。为研究合成气最合适的起始组成比n(H2):n(C0),分别在230°C、2500C和2700C进行实验,结果如图。
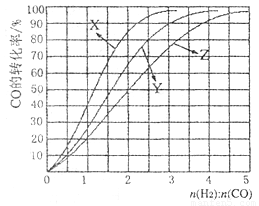
①2700C的实验结果所对应的曲线是_________ (填字母);
②2300C时,工业生产适宜釆用的合成气组成n(H2):n(CO)的比值范围是_________ (填字母)。
A. 1 〜1.5 B. 2. 5〜3 C. 3. 5〜4. 5
(5) 某同学以石墨为电极,以KOH溶液为电解质设计甲醇燃料电池,其负极的电极反应式为_________。
科目:gzhx 来源:2012-2013学年江苏省扬州、南通、泰州、宿迁四市高三第二次调研测试化学试卷(解析版) 题型:简答题
在高温高压下CO具有极高的化学活性,能与多种单质或化合物反应。
(1)若在恒温恒容的容器内进行反应C(s)+H2O(g)  CO(g)+H2(g),则可用来判断该反应达到平衡状态的标志有 。(填字母)
CO(g)+H2(g),则可用来判断该反应达到平衡状态的标志有 。(填字母)
a.容器内的压强保持不变 b.容器中H2浓度与CO浓度相等
c.容器中混合气体的密度保持不变 d.CO的生成速率与H2的生成速率相等
(2)CO一空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2。该电池负极的电极反应式为 。
(3)一定条件下,CO与H2可合成甲烷,反应方程式为:CO(g)+3H2(g)  CH4(g)+ H2O (g)
CH4(g)+ H2O (g)
①一定条件下,该反应能够自发进行的原因是 。
②已知H2(g)、CO(g)和 CH4(g)的燃烧热分别为285.8 kJ·mol-1、283.0 kJ·mol-1和890,0 kJ·mol-1。
写出CO与H2反应生成CH4和CO2的热化学方程式: 。
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为: .
CH3OH(g)+CO(g)  HCOOCH3(g) △H=-29.1 kJ·mol-1
HCOOCH3(g) △H=-29.1 kJ·mol-1
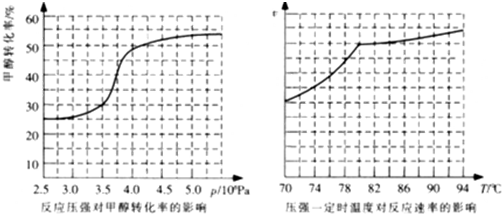
科研人员对该反应进行了研究.部分研究结果如下:
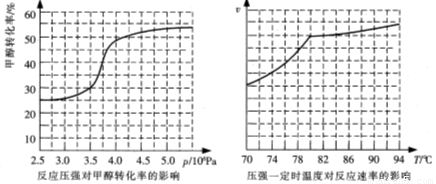
①从反应压强对甲醇转化率的影响“效率"看,工业制取甲酸甲酯应选择的压强是 。
②实际工业生产中采用的温度是80℃,其理由是 。
科目:gzhx 来源: 题型:阅读理解
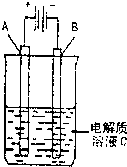 (2011•太原二模)现已确认,CO、SO2和NOx的排放是造成大气污染的重要原因.
(2011•太原二模)现已确认,CO、SO2和NOx的排放是造成大气污染的重要原因.科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:阅读理解
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
科目:gzhx 来源: 题型: