
科目:gzhx 来源:2013-2014学年河北衡水中学高三上学期期中考试化学试卷(解析版) 题型:选择题
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )
A.AlON和石英的化学键类型相同
B.AlON和石英晶体类型相同
C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同
D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同
科目:gzhx 来源: 题型:单选题
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是( )
| A.AlON和石英的化学键类型相同 |
| B.AlON和石英晶体类型相同 |
| C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同 |
科目:gzhx 来源: 题型:单选题
科目:gzhx 来源:不详 题型:单选题
| A.AlON和石英的化学键类型相同 |
| B.AlON和石英晶体类型相同 |
| C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同 |
科目:gzhx 来源: 题型:
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是 ( )
A.AlON和石英的化学键类型相同 B.AlON和石英晶体类型相同
C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同
D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体 类型相同
科目:gzhx 来源: 题型:
| A、AlON和石英的化学键类型相同 |
| B、AlON和石英晶体类型相同 |
| C、AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| D、AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同 |
科目:gzhx 来源: 题型:
| ||
| A、氮氧化铝中氮的化合价是-3 |
| B、AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| C、反应中每生成5.7gAlON同时生成1.12LCO |
| D、反应中氧化产物和还原产物的物质的量之比是2:1 |
科目:gzhx 来源: 题型:
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是 ( )
A.AlON和石英的化学键类型相同 B.AlON和石英晶体类型相同
C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同
D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同
科目:gzhx 来源:2016届浙江省高三上学期第二次月考化学试卷(解析版) 题型:选择题
氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是
A.AlON和石英的化学键类型相同
B.AlON和石英晶体类型相同
C.AlON中N元素的化合价为-1
D.电解熔融AlON或电解熔融Al2O3都能得到Al
科目:gzhx 来源: 题型:

科目:gzhx 来源: 题型:解答题
科目:gzhx 来源: 题型:
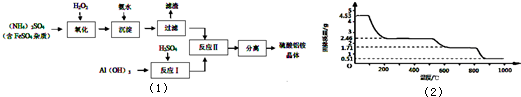
纳米氧化铝在陶瓷材料、电子工业、生物医药等方面有广阔的应用前景,它可通过硫酸铝铵晶体热分解得到。[已知:硫酸铝铵晶体的化学式为(NH4)Al (SO4)n·12H2O]
制备硫酸铝铵晶体的实验流程如下:
 |
(1)检验上述流程中“过滤”后杂质是否除尽的实验方法是 。
(2)上述流程中,“分离”所包含的操作依次为: 、 、过滤、洗涤、干燥。
(3)硫酸铝铵水溶液呈酸性的原因是 (用离子方程式表示)。
(4)写出上述“反应Ⅱ”中获得硫酸铝铵晶体的化学方程式 。
(5)向硫酸铝铵溶液中加入氢氧化钡溶液至Al3+刚好沉淀完全,写出反应的离子方程式 。
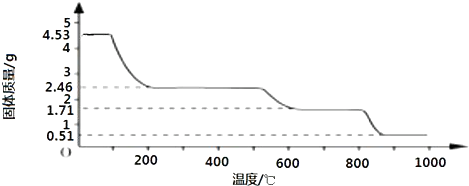
(6)取4.53 g硫酸铝铵晶体加热分解,加热过程中,固体质量随时间的变化如下图所示:

写出400℃时剩余固体成分的化学式 。
科目:gzhx 来源:2012-2013学年安徽省蚌埠二中高三暑期测试化学试卷(解析版) 题型:填空题

科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:

科目:gzhx 来源: 题型:
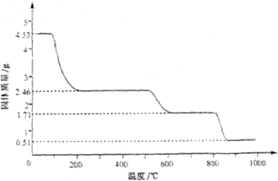 4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).
4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).科目:gzhx 来源: 题型:
纳米氧化铝在人工晶体、微电子器件等方面有重要应用,实验室制取纳米氧化铝方法之一是:将一定体积的0.3mol·L-1Al(NO3)3溶液匀速滴加到2.0mol·L-1 (NH4)2CO3溶液中,搅拌30min,过滤、纯水洗涤、乙醇洗涤、室温真空干燥,得碱式碳酸铝铵[化学式可表示为:(NH4)aAlb(OH)c(CO3)d],然后热分解得到纳米氧化铝。
(1)制取纳米氧化铝时匀速滴加Al(NO3)3溶液并不断搅拌,其主要目的是
。
(2)(NH4)aAlb(OH)c(CO3)d中a、b、c、d的代数关系式为 。
(3)为确定碱式碳酸铝铵的组成,进行如下实验:
①准确称取5.560g样品,在密闭体系中充分加热到300℃使其完全分解且固体质量不再变化;
②产生的气态物质依次通过足量浓硫酸和碱石灰装置吸收,碱石灰装置增重1.760g;
③最后称得剩余固体质量为2.040g。
根据以上实验数据计算碱式碳酸铝铵样品的化学组成(写出计算过程)。
科目:gzhx 来源: 题型:
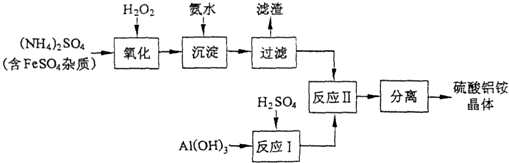
纳米氧化铝在陶瓷、电子、生物医药等方面有广泛的用途,它可通过硫酸铝铵晶体热分解得到.制备硫酸铝铵晶体的实验流程如下: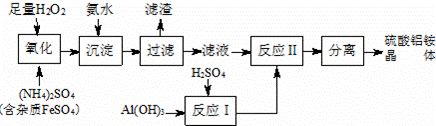
(1)H2O2氧化FeSO4的离子方程式为 2Fe2++H2O2+2H+=2Fe3++2H2O .
(2)加入氨水的目的是 Fe3+使转化为Fe(OH)3 ,其化学反应方程式为 Fe2(SO4)3+6NH3•H2O=2Fe(OH)3↓+3(NH4)2SO4 .
(3)若要保证产品的纯度,必须检验加入氨水后杂质是否除尽?其实验操作是:用试管取少量洗涤液, 加几滴KSCN溶液,若溶液不变红色 ,则说明滤渣已洗净.
(4)上述流程中,“分离”所包含的操作依次为: 蒸发浓缩 、 冷却结晶 、过滤、洗涤、干燥;请完成硫酸铝铵晶体高温分解的化学
方程式:2Al2(NH4)2(SO4)4•24H2O 2 Al2O3+ 4 NH3↑+ 8 SO3↑+ 26H2O .
2 Al2O3+ 4 NH3↑+ 8 SO3↑+ 26H2O .
(5)取4.53g 硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请计算确定400℃时(硫酸铵未分解)剩余固体成分的化学式为 (NH4)2Al2(SO4)4•H2O (不必写出计算过程).
科目:gzhx 来源: 题型:解答题