
科目:gzhx 来源: 题型:解答题
| 物质 | H2(g) | CO2(g) | CH2=CH2 | H2O(g) |
| 能量:KJ/mol | 0 | -394 | 52 | -242 |
 ;△H<0
;△H<0科目:gzhx 来源: 题型:

 (g)+CO2(g)⇌
(g)+CO2(g)⇌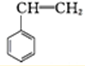 (g)+CO(g)+H2O(g)的△H=
(g)+CO(g)+H2O(g)的△H= )的影响,并设计了如下实验:
)的影响,并设计了如下实验:| 试验编号 | 乙苯 | CO(g)/mol | H(g)/mol | 温度/℃ |
| Ⅰ | 3.0 | 9.0 | 0 | 550 |
| Ⅱ | 3.0 | 9.0 | 0 | 600 |
| Ⅲ | 3.0 | 0 | 9.0 | 550 |
科目:gzhx 来源: 题型:
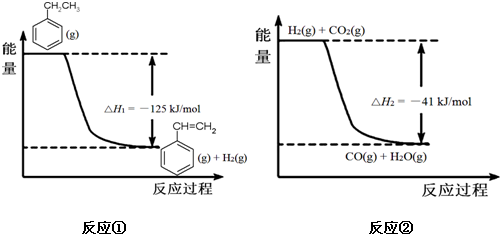
 △H=
△H=| 试验编号 | 乙苯/mol | CO2/mol | He/mol | 温度/℃ |
| Ⅰ | 3.0 | 9.0 | 0 | 550 |
| Ⅱ | 3.0 | 9.0 | 0 | 600 |
| Ⅲ | 3.0 | 0 | a | 550 |

科目:gzhx 来源: 题型:
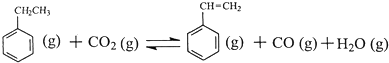
 △H1=-125KJ/mol
△H1=-125KJ/mol
科目:gzhx 来源: 题型:

 △H=
△H= )的影响,并设计了如下实验:
)的影响,并设计了如下实验:| 试验编号 | 乙苯 | CO(g)/mol | H(g)/mol | 温度/℃ |
| Ⅰ | 3.0 | 9.0 | 0 | 550 |
| Ⅱ | 3.0 | 9.0 | 0 | 600 |
| Ⅲ | 3.0 | 0 | 9.0 | 550 |
科目:gzhx 来源:2015-2016学年山西重点中学协作体高二下学期期末化学试卷(解析版) 题型:填空题
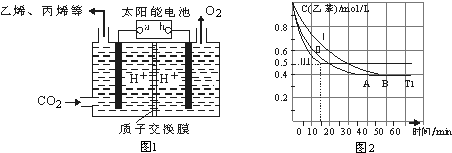
工业上采用乙苯脱氢制备苯乙烯,反应体系同时发生两步可逆反应,其能量变化情况如下:
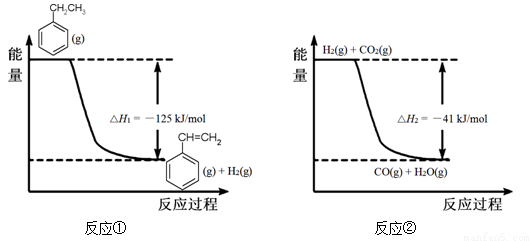
(1)总反应 △H = _______。
△H = _______。
(2)下列叙述不能说明反应体系已达到平衡状态的是___________。
A.v正(CO) = v逆(CO)
B.消耗1 mol CO2同时生成1 mol H2O
C.c(CO2) = c(CO)
D.混合气体的平均相对分子质量保持不变
(3)某化学兴趣小组欲探究在相同压强条件下,CO2用量和温度条件对乙苯脱氢反应
( )的影响,并设计了如下实验:
)的影响,并设计了如下实验:
实验编号 | 乙苯(g) / mol | CO2(g) / mol | He (g) / mol | 温度 / ℃ |
I | 3.0 | 9.0 | 0 | 550 |
Ⅱ | 3.0 | 9.0 | 0 | 600 |
III | 3.0 | 0 | 9.0 | 550 |
①乙苯脱氢反应的化学平衡常数表达式为 。
② 实验III使用9.0molHe的目的是___________________。
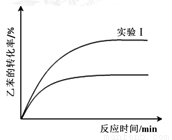
③ 经实验测得,三组实验中乙苯的转化随时间变化如图所示。其中未知曲线代表的是实验______(填“Ⅱ”或“III”)。请用平衡移动原理解释该条件改变对乙苯转化率产生影响的原因:__________________________________________。
科目:gzhx 来源: 题型:解答题
 (g)+CO2(g)⇌
(g)+CO2(g)⇌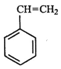 (g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行
(g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行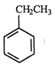 (g)⇌
(g)⇌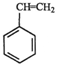 (g)+H2(g)△H1=-125KJ/mol
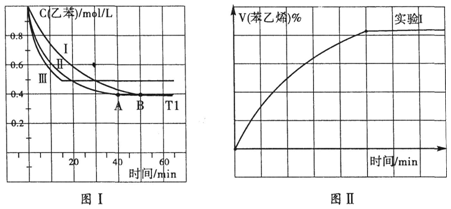
(g)+H2(g)△H1=-125KJ/mol .
.
科目:gzhx 来源:2015-2016学年湖南衡阳八中高二第二学期期末考化学卷(解析版) 题型:填空题
(12分)工业上采用乙苯脱氢制备苯乙烯,反应体系同时发生两步可逆反应,其能量变化情况如下:
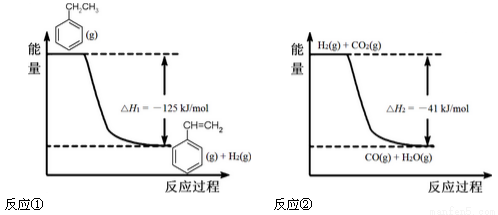
(1)总反应 , △H = _________。
, △H = _________。
(2)下列叙述不能说明反应体系已达到平衡状态的是_______。
A.v正(CO) = v逆(CO) B.消耗1molCO2同时生成1molH2O
C.c(CO2) = c(CO) D.混合气体的平均相对分子质量保持不变
(3)某化学兴趣小组欲探究在相同压强条件下,CO2用量和温度条件对乙苯脱氢反应
( )的影响,并设计了如下实验:
)的影响,并设计了如下实验:

①乙苯脱氢反应的化学平衡常数表达式为______________。
②a=___________________。
③ 经实验测得,三组实验中乙苯的转化随时间变化如右图所示。其中未知曲线代表的是实验____(填“Ⅱ”或“III”)。请用平衡移动原理解释该条件改变对乙苯转化率产生影响的原因:______________。

科目:gzhx 来源: 题型:解答题
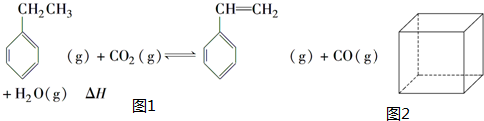
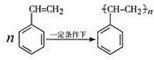 .立方烷(C8H8)的键线式结构如图2所示,它和苯乙烯的关系是同分异构体(填“同位素”、“同素异形体”、“同分异构体”或“同系物”).
.立方烷(C8H8)的键线式结构如图2所示,它和苯乙烯的关系是同分异构体(填“同位素”、“同素异形体”、“同分异构体”或“同系物”).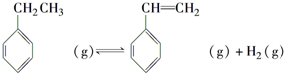 △H1=+117.6kJ•mol-1
△H1=+117.6kJ•mol-1科目:gzhx 来源:江苏高考真题 题型:填空题

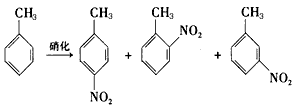
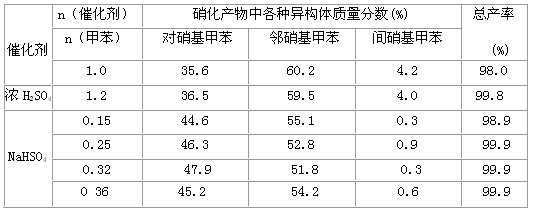
科目:gzhx 来源:模拟题 题型:实验题

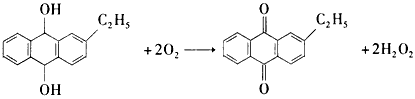
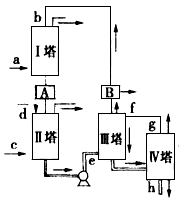
科目:gzhx 来源:2012-2013学年广东省深圳市高三上学期第一次调研考试理综化学试卷(解析版) 题型:实验题
工业上用异丙苯氧化法合成苯酚,其生产流程如下图:

有关物质的性质如下表:
|
物质 |
沸点 |
溶解性 |
主要化学性质 |
|
异丙苯 |
152.4℃ |
不溶于水,易溶于酒精。 |
可被强氧化剂氧化 |
|
苯酚 |
181.8℃ |
微溶于冷水,易溶于热水和酒精等有机溶剂。 |
易被氧化 |
|
丙酮 |
56.2℃ |
易溶于水和有机溶剂 |
不易被氧化 |
(1)检验有机相中是否含有水的方法是 ;
(2)“操作2”的名称是 ;
(3)丙酮中常含有苯酚和异丙苯中的一种或者两种有机物杂质,某同学做了如下检验。
|
检验项目 |
实验方案 |
|
检验丙酮中一定存在有机杂质的方法是 |
A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
|
检验丙酮中一定含有苯酚的方案是: |
取少许待测液置于试管中,滴加1~2滴FeCl3溶液。预期的实验现象和结论是 。 |
(4)某同学对该厂废水进行定量分析。取20.00mL废水于锥形瓶中,水浴加热,用0.1000mol·L-1酸性KMnO4溶液滴定(假定只有苯酚与KMnO4反应)。达到滴定终点时,消耗KMnO4溶液的体积为10.00mL。有关反应方程式为:
5  +
28KMnO4 + 42H2SO4
+
28KMnO4 + 42H2SO4 28MnSO4
+ 14K2SO4 + 30CO2↑+ 57H2O
28MnSO4
+ 14K2SO4 + 30CO2↑+ 57H2O
①滴定终点的现象为 。
②该废水中苯酚的含量为 mg·mL-1。(保留二位有效数字)。
科目:gzhx 来源: 题型:实验题
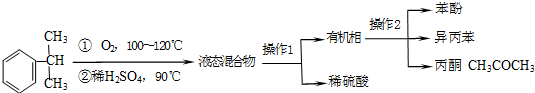
工业上用异丙苯氧化法合成苯酚,其生产流程如下图: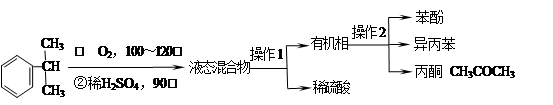
有关物质的性质如下表:
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精。 | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水和酒精等有机溶剂。 | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机杂质的方法是 | A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯酚的方案是: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液。预期的实验现象和结论是 。 |
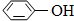 + 28KMnO4 + 42H2SO4
+ 28KMnO4 + 42H2SO4 28MnSO4 + 14K2SO4 + 30CO2↑+ 57H2O
28MnSO4 + 14K2SO4 + 30CO2↑+ 57H2O科目:gzhx 来源:不详 题型:实验题

| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精。 | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水和酒精等有机溶剂。 | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机杂质的方法是 | A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯酚的方案是: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液。预期的实验现象和结论是 。 |
 + 28KMnO4 + 42H2SO4
+ 28KMnO4 + 42H2SO4 28MnSO4 + 14K2SO4 + 30CO2↑+ 57H2O
28MnSO4 + 14K2SO4 + 30CO2↑+ 57H2O科目:gzhx 来源: 题型:
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精. | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水和酒精等有机溶剂. | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机杂质的方法是 | A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯酚的方案是: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液.预期的实验现象和结论是 |
科目:gzhx 来源: 题型:解答题
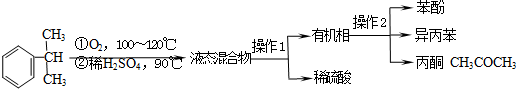
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精. | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水 和酒精等有机溶剂. | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机 杂质的试剂是①A.(填写右边字母) | A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯 酚的方案: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液,若试管中溶液颜色变为②紫色,则丙酮中含有苯酚,反之则没有. |
科目:gzhx 来源: 题型:
【实验化学】
工业上用异丙苯氧化法合成苯酚,其生产流程如下图:

有关物质的性质如下表:
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精。 | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水和酒精等有机溶剂。 | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
(1)检验有机相中是否含有水的方法是 ▲ ;
(2)“操作2”的名称是 ▲ ;
(3)丙酮中常含有苯酚和异丙苯中的一种或者两种有机物杂质,某同学做了如下检验。
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机杂质的方法是 ▲ | A. 酸性KMnO4溶液,加热 B. 乙醇,溶解 C. NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯酚的方案是: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液。预期的实验现象和结论是 ▲ 。 |
(4)为测定某工厂排放的污水中苯酚的含量,进行如下实验:取污水试样10.00mL加水稀释至100mL,加入10.0mL一定浓度的KBrO3和KBr的混合溶液,立即加入5mL盐酸,摇匀后加入1gKI固体(足量),再摇匀,放置5min。用0.01000mol/LNa2S2O3标准溶液滴定至淡黄色,加入1mL淀粉溶液,继续滴定至蓝色刚好褪去,用去Na2S2O3标准溶液14.46mL。同时以水代替污水试样做对比实验,用去Na2S2O3标准溶液38.46 mL。已知上述实验中发生的反应有:
KBrO3+5KBr+6HCl=3Br2+3H2O+6KCl 2Na2S2O3+I2=Na2S4O6+2NaI
则此污水中苯酚的含量(以mg/L表示) ▲ 。
科目:gzhx 来源: 题型:阅读理解
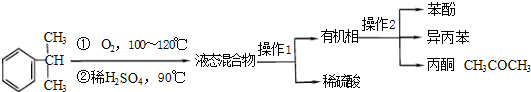
| 物质 | 沸点 | 溶解性 | 主要化学性质 |
| 异丙苯 | 152.4℃ | 不溶于水,易溶于酒精. | 可被强氧化剂氧化 |
| 苯酚 | 181.8℃ | 微溶于冷水,易溶于热水和酒精等有机溶剂. | 易被氧化 |
| 丙酮 | 56.2℃ | 易溶于水和有机溶剂 | 不易被氧化 |
| 检验项目 | 实验方案 |
| 检验丙酮中一定存在有机杂质的方法是 A A |
A.酸性KMnO4溶液,加热 B.乙醇,溶解 C.NaOH溶液(酚酞),加热 |
| 检验丙酮中一定含有苯酚的方案是: | 取少许待测液置于试管中,滴加1~2滴FeCl3溶液.预期的实验现象和结论是 滴加FeCl3溶液后,若试管中溶液变为紫色,则丙酮中含有苯酚;若试管中溶液不变为紫色,则丙酮不含苯酚 滴加FeCl3溶液后,若试管中溶液变为紫色,则丙酮中含有苯酚;若试管中溶液不变为紫色,则丙酮不含苯酚 . |
科目:gzhx 来源: 题型:

科目:gzhx 来源: 题型:
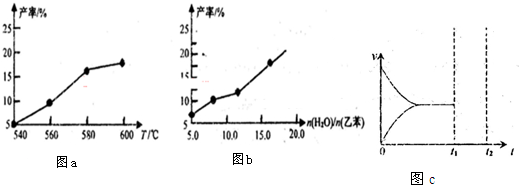
| n(H2O) |
| n(乙苯) |