
科目:gzhx 来源: 题型:阅读理解
| 14×6 |
| 126 |
| 14×6 |
| 126 |
| 2562 |
| 1000 |
| 2562 |
| 1000 |
科目:gzhx 来源: 题型:阅读理解
奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是:食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
(1)样品处理:准确称取一定量的固体样品奶粉,移入干燥的凯氏烧瓶中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
(2)NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸氨,再经过再经过碱化蒸馏后,氨即成为游离状态,游离氨经硼酸吸收。
(3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?
。
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
A.凯氏烧瓶中溶液转移移到容量瓶中时,未洗涤凯氏烧瓶
B.定容时,俯视刻度线
C.定容时,仰视刻度线![]()
D.移液时,有少量液体溅出
(3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。![]() 已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3。
已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3。
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。则三聚氰胺中氮的含量为 。
科目:gzhx 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第13期 总第169期 人教课标版(选修4) 题型:058
| |||||||||||||||||||||||||||||||||||
科目:gzhx 来源:宜宾模拟 题型:问答题
科目:gzhx 来源: 题型:阅读理解
(8分)、奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是:食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。实验操作步骤:
(1)样品处理:准确称取一定量的固体样品奶粉,移入干燥的凯氏烧瓶中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
(2)NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸铵,再经过碱化蒸馏后,氨即成为游离状态,游离氨经硼酸吸收。
(3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
A、凯氏烧瓶中溶液转移移到容量瓶中时,未洗涤凯氏烧瓶
B、定容时,俯视刻度线 C、定容时,仰视刻度线 D、移液时,有少量液体溅出
 (3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。(已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3)
(3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。(已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3)
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。其实凯氏定氮法的缺陷并不难弥补,只要先用三氯乙酸处理样品。三氯乙酸能让蛋白质形成沉淀,过滤后,分别测定沉淀和滤液中的氮含量,就可以知道蛋白质的真正含量和冒充蛋白质的氮含量。试求三聚氰胺中氮的含量为 。
科目:gzhx 来源:浙江省杭州高级中学2012届高三第三次月考化学试题 题型:022
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.
(1)合成氨反应N2(g)+3H2(g)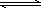 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡________移动(填“向左”“向右”或“不”);使用催化剂,上述反应的ΔH________(填“增大”“减小”或“不改变”).
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡________移动(填“向左”“向右”或“不”);使用催化剂,上述反应的ΔH________(填“增大”“减小”或“不改变”).
(2)一氧化碳在高温下与水蒸气反应的方程式为:CO+H2O=CO2+H2.已知部分物质燃烧的热化学方程式如下:
2H2(g)+O2(g)=2H2O(l);ΔH=-571.6 kJ·mol-
2CO(g)+O2(g)=2CO2(g);ΔH=-566 kJ·mol-1
又知1 mol H2O(g)转变为1 mol H2O(l)时放出44.0 kJ热量.写出CO和水蒸气在高温催化剂下反应的热化学方程式________.
(3)在25℃下,向浓度均为0.1 mol?L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________.已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20.
(4)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造新型燃烧电池,放电过程中,溶液中铵根离子浓度逐渐增大.请写出该电池的正极反应式________.
(5)某温度(t℃)时,测得0.01 mol·L-1的NaOH溶液的pH=11.在此温度下,将pH=1的H2SO4溶液VaL与pH=11的NaOH溶液VbL混合,若所得混合液为中性,则Va∶Vb=________.
(6)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-).则溶液显________性(填“酸”“碱”或“中”);
(7)NH4Cl是一种重要的化肥.
①用0.1 mol·L-1的盐酸滴定0.1 mol·L-1的氨水,滴定过程中不可能出现的结果是:
a.c(NH![]() )=c(Cl-),c(OH-)=c(H+)
)=c(Cl-),c(OH-)=c(H+)
b.c(NH![]() )>c(Cl-),c(OH-)<c(H+)
)>c(Cl-),c(OH-)<c(H+)
c.c(NH![]() )>c(Cl-),c(OH-)>c(H+)
)>c(Cl-),c(OH-)>c(H+)
d.c(NH![]() )<c(Cl-),c(OH-)>c(H+)
)<c(Cl-),c(OH-)>c(H+)
②NH4Cl溶液中存在:NH4++H2O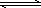 NH3·H2O+H+,则该反应常温下的平衡常数K=________(已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10-5 mol·L-1)
NH3·H2O+H+,则该反应常温下的平衡常数K=________(已知:常温下,NH3·H2O的电离平衡常数Kb=1.7×10-5 mol·L-1)
科目:gzhx 来源:2009年四川省宜宾市高考化学二诊试卷(解析版) 题型:解答题
科目:gzhx 来源: 题型:阅读理解
(12分)奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是:食品与硫酸和催化剂一同加热消化,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
(1)样品处理:准确称取一定量的固体样品奶粉,移入干燥的凯氏烧瓶中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
(2)NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸氨,再经过再经过碱化蒸馏后,氨即成为游离状态,游离氨经硼酸吸收。
(3)氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,从消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?
。
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
A、凯氏烧瓶中溶液转移移到容量瓶中时,未洗涤凯氏烧瓶
B、定容时,俯视刻度线
C、定容时,仰视刻度线
D、移液时,有少量液体溅出
(3)若称取样品的质量为1.5g,共配制100毫升的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol/L盐酸滴定,共用去盐酸的体积为23.0mL,则该样品中N的含量为 。
已知:滴定过程中涉及到的反应方程式:(NH4)2 B4O7 + 2HCl + 5H2O = 2NH4Cl + 4H3BO3
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。则三聚氰胺中氮的含量为 。
科目:gzhx 来源: 题型:阅读理解
 测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:
测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:| 106n |
| 197m |
| 106n |
| 197m |
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:
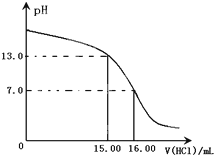
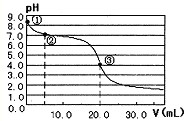 (2011•龙岩模拟)取20mL NaHCO3溶液于锥形瓶中,用0.1mol/L盐酸滴定.滴定过程中,混合液pH的变化如图所示.下列叙述正确的是( )
(2011•龙岩模拟)取20mL NaHCO3溶液于锥形瓶中,用0.1mol/L盐酸滴定.滴定过程中,混合液pH的变化如图所示.下列叙述正确的是( )科目:gzhx 来源: 题型:阅读理解

| ||
| ||
| 方案 质量 |
方案甲 | 方案乙 |
| U型管+固体 | 硬质玻璃管+固体 | |
| 反应前质量/g | a | c |
| 完全反应后质量/g | b | d |
| 16(d+w-c) |
| c-d |
| 16(d+w-c) |
| c-d |
科目:gzhx 来源: 题型:
科目:gzhx 来源: 题型:阅读理解
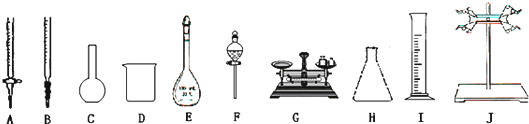
| 实验步骤 | 设计这一步骤的目的 |
| 1.将配制的氢氧化钠溶液加热 | ① 除去溶液的氧气 除去溶液的氧气 |
| 2.在加热后的溶液中滴加酚酞,并在上方滴一些植物油 | ②利用植物油隔绝 |
| 实验方法 | 观察到的现象和结论 |
| 方案一:分别配制不同物质的量浓度的氢氧化钠溶液,然后各滴加数滴酚酞溶液. | 浓度大的溶液中酚酞红色会消失,则证明红色消失与氢氧化钠溶液的浓度大小有关 |
| 方案二:向原红色消失的溶液中加 水 水 (填试剂名称) |
红色重新出现,则说明红色消失与氢氧化钠溶液浓度大小有关 红色重新出现,则说明红色消失与氢氧化钠溶液浓度大小有关 |
科目:gzhx 来源: 题型:阅读理解
| 温度℃ 溶解度 溶质 g/100g水 |
10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ||||
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | 14.4 | 16.4 | |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
| c×V1 ×10-3×M(Na2CO3)g |
| Gg |
| c×V1 ×10-3×M(Na2CO3)g |
| Gg |
科目:gzhx 来源: 题型:
| A、测定某溶液的pH时,用pH试纸蘸取待测液,然后和标准比色卡对比得出pH | B、锌与稀硫酸反应制取氢气,加入少量硫酸铜粉末会使产生氢气的速率加快 | C、测定硫酸铜晶体中结晶水含量时,加热后的硫酸铜粉末要放在空气中冷却再称量 | D、用标准盐酸滴定未知浓度的氢氧化钠溶液,用待测液润洗锥形瓶 |
科目:gzhx 来源: 题型:阅读理解
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.52 | 25.42 |
| 第二次 | 20.00 | 4.07 | 29.17 |
科目:gzhx 来源: 题型:
| 滴定次数 | 待测NaOH溶液体积(mL) | 0.1000mol/L HCl溶液的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
科目:gzhx 来源: 题型:阅读理解
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |