
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
Ạ́¼°Æ仯ºÏÎïÓĐ¹ă·ºµÄÓ¦ÓĂ£¬¶ÔSO2ĐÔÖʵÄÑĐ¾¿ÊǸßÖĐ»¯Ñ§½̀ѧµÄ̉»ÏîÖØ̉ªÄÚÈƯ¡£
I£®¶Ô±ÈÑĐ¾¿ÊÇ̉»ÖÖÖØ̉ªµÄÑĐ¾¿·½·¨¡£Èô½«Ạ́µÄµ¥Öʼ°²¿·Ö»¯ºÏÎï°´ÈçϱíËùʾ·Ö³É3 ×飬ỘµÚ2×éÖĐÎïÖÊMµÄ»¯Ñ§Ê½ÊÇ ¡£
|
µÚ1×é |
µÚ2×é |
µÚ3×é |
|
S (µ¥ÖÊ) |
SO2¡¢H2SO3¡¢M¡¢NaHSO3 |
SO3¡¢H2SO4¡¢Na2SO4¡¢ NaHSO4 |
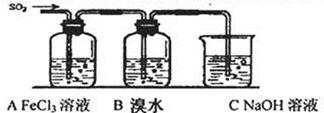
¢̣£®Ä³Đ£»¯Ñ§Ñ§Ï°Đ¡×éÓĂÏÂͼËùʾµÄʵÑé×°ÖĂÑĐ¾¿SO2Æø̀廹ÔFe3+¡¢Br2µÄ·´Ó¦¡£

£¨1£©ÏÂÁĐʵÑé·½°¸¿É̉ÔÓĂÓÚÔÚʵÑéỂÖÆÈ¡ËùĐèSO2µÄÊÇ ¡£
A£®Na2SO3ÈÜ̉ºÓëHNO3 B£®Na2SO3¹̀̀åŨẠ́Ëá
C£®¹̀̀åẠ́ÔÚ´¿ÑơÖĐȼÉƠ D£®ÍÓëÈȵÄŨẠ́Ëá
£¨2£©×°ÖĂCµÄ×÷ÓĂÊdzưÈ¥¶àÓàµÄSO2£¬·ÀÖ¹ÎÛȾ¿ƠÆø¡£̉ÑÖªÔÚÓĂÇâÑơ»¯ÄÆÈÜ̉ºÎüÊƠSO2µÄ ¹ư³̀ÖĐ£¬ÍùÍùµĂµ½Na2SO3ºÍNaHSO3µÄ»́ºÏÈÜ̉º£¬³£ÎÂÏ£¬ÈÜ̉ºpHËæn(SO32¡ª)£ºn(HSO3¡ª)±ä»¯¹ØϵÈçϱí
|
n(SO32¡ª)£ºn(HSO3¡ª) |
91£º9 |
1£º1 |
9£º91 |
|
pH |
8.2 |
7.2 |
6.2 |
µ±ÎüÊỞºÖĐn(SO32¡ª)£ºn(HSO3¡ª) =10£º1ʱ£¬ÈÜ̉ºÖĐÀë×ÓŨ¶È¹ØϵƠưÈ·µÄÊÇ ¡£
A£®c(Na+)+ c(H+)= 2c(SO32¡ª)+ c(HSO3¡ª)+ c(OH¡ª)
B£®c(Na+)£¾c(HSO3¡ª)£¾c(SO32¡ª)£¾c(OH¡ª)£¾c(H+)
C£®c(Na+)£¾c(SO32¡ª)£¾c(HSO3¡ª)£¾c(OH¡ª)£¾c(H+)
£¨3£©ÔÚÉÏÊö×°ÖĂÖĐͨÈë¹ưÁ¿µÄSO2£¬ÎªÁËÑéÖ¤AÖĐSO2ÓëFe3+·¢ÉúÁËÑơ»¯»¹Ô·´Ó¦£¬ËûĂÇÈ¡AÖĐ·´Ó¦ºóµÄÈÜ̉º·Ö³ÉÈư·Ư£¬²¢Éè¼ÆÁËÈçÏẦ½¾¿ÊµÑ飬ÇëÄăÆÀ¼Û²¢²ÎÓëËûĂǵÄ̀½¾¿¹ư³̀£¨Ï̃Ñ¡ÊÔ¼Á£ºKMnO4ÈÜ̉º¡¢KSCNÈÜ̉º¡¢BaCl2ÈÜ̉º¡¢Ï¡Ạ́ËᡢϡÑÎËᡢϡÏơ Ëá¡¢Ba(NO3)2ÈÜ̉º¡¢ĐÂÖƵÄÂÈË®£©
|
Đ̣ºÅ |
ʵÑé·½°¸ |
ʵÑéÏÖÏó |
½áÂÛ |
|
·½°¸¢Ù |
ÍùµÚ̉»·ƯÊỔºÖĐ¼ÓÈëKMnO4ÈÜ̉ºÈÜ̉º |
×Ϻ́É«ÍÊÈ¥ |
SO2ÓëFe3+·´Ó¦Éú³ÉÁËFe2+ |
|
·½°¸¢Ú |
ÍùµÚ¶₫·ƯÊỔºÖĐ¼ÓÈë |
|
SO2ÓëFe3+·´Ó¦Éú³ÉÁËFe2+ |
|
·½°¸¢Û |
ÍùµÚ¶₫·ƯÊỔºÖĐ¼ÓÈë |
|
SO2ÓëFe3+·´Ó¦Éú³ÉÁËSO42¡ª |
ÉÏÊö·½°¸¢ÙµĂ³öµÄ½áÂÛÊÇ·ñºÏÀí £¬Ộ̉ ¡£
Èç¹ûËûĂÇÉè¼ÆµÄ·½°¸¢ÚÓë·½°¸¢Û¾ùºÏÀí²¢Ç̉µĂµ½ÏàÓ¦½áÂÛ£¬ÇëÄă½«ÉÏĂæ±í¸ñ²¹³äÍêƠû¡£
£¨4£©×°ÖĂBÖĐÄܱíĂ÷Br¡ªµÄ»¹ÔĐÔÈơÓÚSO2µÄÏÖÏóÊÇ ¡£
Ạ́¼°Æ仯ºÏÎïÓĐ¹ă·ºµÄÓ¦ÓĂ£¬¶ÔSO2ĐÔÖʵÄÑĐ¾¿ÊǸßÖĐ»¯Ñ§½̀ѧµÄ̉»ÏîÖØ̉ªÄÚÈƯ¡£
I£®¶Ô±ÈÑĐ¾¿ÊÇ̉»ÖÖÖØ̉ªµÄÑĐ¾¿·½·¨¡£Èô½«Ạ́µÄµ¥Öʼ°²¿·Ö»¯ºÏÎï°´ÈçϱíËùʾ·Ö³É3 ×飬ỘµÚ2×éÖĐÎïÖÊMµÄ»¯Ñ§Ê½ÊÇ ¡£
|
µÚ1×é |
µÚ2×é |
µÚ3×é |
|
S (µ¥ÖÊ) |
SO2¡¢H2SO3¡¢M¡¢NaHSO3 |
SO3¡¢H2SO4¡¢Na2SO4¡¢ NaHSO4 |
¢̣£®Ä³Đ£»¯Ñ§Ñ§Ï°Đ¡×éÓĂÏÂͼËùʾµÄʵÑé×°ÖĂÑĐ¾¿SO2Æø̀廹ÔFe3+¡¢Br2µÄ·´Ó¦¡£

£¨1£©ÏÂÁĐʵÑé·½°¸¿É̉ÔÓĂÓÚÔÚʵÑéỂÖÆÈ¡ËùĐèSO2µÄÊÇ ¡£
A£®Na2SO3ÈÜ̉ºÓëHNO3 B£®Na2SO3¹̀̀åŨẠ́Ëá
C£®¹̀̀åẠ́ÔÚ´¿ÑơÖĐȼÉƠ D£®ÍÓëÈȵÄŨẠ́Ëá
£¨2£©×°ÖĂCµÄ×÷ÓĂÊdzưÈ¥¶àÓàµÄSO2£¬·ÀÖ¹ÎÛȾ¿ƠÆø¡£̉ÑÖªÔÚÓĂÇâÑơ»¯ÄÆÈÜ̉ºÎüÊƠSO2µÄ ¹ư³̀ÖĐ£¬ÍùÍùµĂµ½Na2SO3ºÍNaHSO3µÄ»́ºÏÈÜ̉º£¬³£ÎÂÏ£¬ÈÜ̉ºpHËæn(SO32¡ª)£ºn(HSO3¡ª)±ä»¯¹ØϵÈçϱí
|
n(SO32¡ª)£ºn(HSO3¡ª) |
91£º9 |
1£º1 |
9£º91 |
|
pH |
8.2 |
7.2 |
6.2 |
µ±ÎüÊỞºÖĐn(SO32¡ª)£ºn(HSO3¡ª) =10£º1ʱ£¬ÈÜ̉ºÖĐÀë×ÓŨ¶È¹ØϵƠưÈ·µÄÊÇ ¡£
A£®c(Na+)+ c(H+)= 2c(SO32¡ª)+ c(HSO3¡ª)+ c(OH¡ª)
B£®c(Na+)£¾c(HSO3¡ª)£¾c(SO32¡ª)£¾c(OH¡ª)£¾c(H+)
C£®c(Na+)£¾c(SO32¡ª)£¾c(HSO3¡ª)£¾c(OH¡ª)£¾c(H+)
£¨3£©ÔÚÉÏÊö×°ÖĂÖĐͨÈë¹ưÁ¿µÄSO2£¬ÎªÁËÑéÖ¤AÖĐSO2ÓëFe3+·¢ÉúÁËÑơ»¯»¹Ô·´Ó¦£¬ËûĂÇÈ¡AÖĐ·´Ó¦ºóµÄÈÜ̉º·Ö³ÉÈư·Ư£¬²¢Éè¼ÆÁËÈçÏẦ½¾¿ÊµÑ飬ÇëÄăÆÀ¼Û²¢²ÎÓëËûĂǵÄ̀½¾¿¹ư³̀£¨Ï̃Ñ¡ÊÔ¼Á£ºKMnO4ÈÜ̉º¡¢KSCNÈÜ̉º¡¢BaCl2ÈÜ̉º¡¢Ï¡Ạ́ËᡢϡÑÎËᡢϡÏơ Ëá¡¢Ba(NO3)2ÈÜ̉º¡¢ĐÂÖƵÄÂÈË®£©
|
Đ̣ºÅ |
ʵÑé·½°¸ |
ʵÑéÏÖÏó |
½áÂÛ |
|
·½°¸¢Ù |
ÍùµÚ̉»·ƯÊỔºÖĐ¼ÓÈëKMnO4ÈÜ̉ºÈÜ̉º |
×Ϻ́É«ÍÊÈ¥ |
SO2ÓëFe3+·´Ó¦Éú³ÉÁËFe2+ |
|
·½°¸¢Ú |
ÍùµÚ¶₫·ƯÊỔºÖĐ¼ÓÈë |
|
SO2ÓëFe3+·´Ó¦Éú³ÉÁËFe2+ |
|
·½°¸¢Û |
ÍùµÚ¶₫·ƯÊỔºÖĐ¼ÓÈë |
|
SO2ÓëFe3+·´Ó¦Éú³ÉÁËSO42¡ª |
ÉÏÊö·½°¸¢ÙµĂ³öµÄ½áÂÛÊÇ·ñºÏÀí £¬Ộ̉ ¡£
Èç¹ûËûĂÇÉè¼ÆµÄ·½°¸¢ÚÓë·½°¸¢Û¾ùºÏÀí²¢Ç̉µĂµ½ÏàÓ¦½áÂÛ£¬ÇëÄă½«ÉÏĂæ±í¸ñ²¹³äÍêƠû¡£
£¨4£©×°ÖĂBÖĐÄܱíĂ÷Br¡ªµÄ»¹ÔĐÔÈơÓÚSO2µÄÏÖÏóÊÇ ¡£
Ạ́¼°Æ仯ºÏÎïÓĐ¹ă·ºµÄÓ¦ÓĂ£¬¶ÔSO2ĐÔÖʵÄÑĐ¾¿ÊǸßÖĐ»¯Ñ§½̀ѧµÄ̉»ÏîÖØ̉ªÄÚÈƯ¡£
I£®¶Ô±ÈÑĐ¾¿ÊÇ̉»ÖÖÖØ̉ªµÄÑĐ¾¿·½·¨¡£Èô½«Ạ́µÄµ¥Öʼ°²¿·Ö»¯ºÏÎï°´ÈçϱíËùʾ·Ö³É3 ×飬ỘµÚ2×éÖĐÎïÖÊMµÄ»¯Ñ§Ê½ÊÇ ¡£
| µÚ1×é | µÚ2×é | µÚ3×é |
| S (µ¥ÖÊ) | SO2¡¢H2SO3¡¢M¡¢NaHSO3 | SO3¡¢H2SO4¡¢Na2SO4¡¢ NaHSO4 |
| n(SO32¡ª)£ºn(HSO3¡ª) | 91£º9 | 1£º1 | 9£º91 |
| pH | 8.2 | 7.2 | 6.2 |
| Đ̣ºÅ | ʵÑé·½°¸ | ʵÑéÏÖÏó | ½áÂÛ |
| ·½°¸¢Ù | ÍùµÚ̉»·ƯÊỔºÖĐ¼ÓÈëKMnO4ÈÜ̉ºÈÜ̉º | ×Ϻ́É«ÍÊÈ¥ | SO2ÓëFe3+·´Ó¦Éú³ÉÁËFe2+ |
| ·½°¸¢Ú | ÍùµÚ¶₫·ƯÊỔºÖĐ¼ÓÈë | | SO2ÓëFe3+·´Ó¦Éú³ÉÁËFe2+ |
| ·½°¸¢Û | ÍùµÚ¶₫·ƯÊỔºÖĐ¼ÓÈë | | SO2ÓëFe3+·´Ó¦Éú³ÉÁËSO42¡ª |
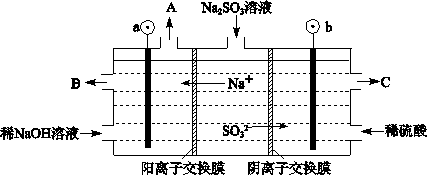
£¨14·Ö£©¹¤̉µ·ÏÆø¡¢Æû³µÎ²ÆøÅŷųöµÄSO2¡¢NOxµÈ£¬ÊÇĐγÉÎíö²µÄÖØ̉ª̣̉ËØ¡£ö²ÊÇÓÉ¿ƠÆøÖеĻ̉³¾¡¢Ạ́Ëá¡¢ÏơËá¡¢ÓĐ»ú̀¼Ç⻯ºÏÎïµÈÁ£×ÓĐγɵÄÑ̀Îí¡£
£¨1£©´óÆøÖеÄSO2ÔÚÑ̀³¾µÄ´ß»¯ÏÂĐγÉẠ́ËáµÄ·´Ó¦·½³̀ʽÊÇ____________________¡£
£¨2£©̉ÑÖª2SO2 (g)+ O2 (g) 2SO3(g) ¡÷H£½£196kJ/mol£¬̀á¸ß·´Ó¦ÖĐSO2µÄת»¯ÂÊ£¬ÊǼơÉÙSO2ÅŷŵÄÓĐЧ´ëÊ©¡£
2SO3(g) ¡÷H£½£196kJ/mol£¬̀á¸ß·´Ó¦ÖĐSO2µÄת»¯ÂÊ£¬ÊǼơÉÙSO2ÅŷŵÄÓĐЧ´ëÊ©¡£
¢ÙTζÈʱ£¬ÔÚ2LÈƯ»ư¹̀¶¨²»±äµÄĂܱƠÈƯÆ÷ÖĐ¼ÓÈë2.0 mol SO2ºÍ1.0 mol O2£¬5 minºó·´Ó¦´ïµ½Æ½ºâ£¬¶₫Ñơ»¯Ạ́µÄת»¯ÂÊΪ50%£¬Ộ¦Ô(O2)£½____________¡£
¢ÚÔÚ¢ÙµÄ̀ơ¼₫Ï£¬ÅĐ¶Ï¸Ă·´Ó¦´ïµ½Æ½ºâ×´̀¬µÄ±êÖ¾ÊÇ_______(̀î×Öĸ)¡£
| A£®SO2¡¢O2¡¢SO3ÈưƠßµÄŨ¶ÈÖ®±ÈΪ2¡Ă1¡Ă2 | B£®ÈƯÆ÷ÄÚÆø̀åµÄѹǿ²»±ä |
| C£®ÈƯÆ÷ÄÚ»́ºÏÆø̀åµÄĂܶȱ£³Ö²»±ä | D£®SO3µÄÎïÖʵÄÁ¿²»Ôٱ仯 |
 2SO3(g) ¡÷H£½£196kJ/mol£¬̀á¸ß·´Ó¦ÖĐSO2µÄת»¯ÂÊ£¬ÊǼơÉÙSO2ÅŷŵÄÓĐЧ´ëÊ©¡£
2SO3(g) ¡÷H£½£196kJ/mol£¬̀á¸ß·´Ó¦ÖĐSO2µÄת»¯ÂÊ£¬ÊǼơÉÙSO2ÅŷŵÄÓĐЧ´ëÊ©¡£| A£®SO2¡¢O2¡¢SO3ÈưƠßµÄŨ¶ÈÖ®±ÈΪ2¡Ă1¡Ă2 | B£®ÈƯÆ÷ÄÚÆø̀åµÄѹǿ²»±ä |
| C£®ÈƯÆ÷ÄÚ»́ºÏÆø̀åµÄĂܶȱ£³Ö²»±ä | D£®SO3µÄÎïÖʵÄÁ¿²»Ôٱ仯 |
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com