
题目列表(包括答案和解析)
28.(8分)某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
 ① 称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
① 称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
② 将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③ 将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,
研细备用;
④ 按下表中的质量混合好固体后,在相同条件下加热,并与
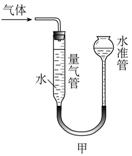
MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略。
|
编号 |
KClO3质量(g) |
其他物质质量(g) |
待测数据 |
|
1 |
2.0 |
∕ |
|
|
2 |
2.0 |
CuO 0.5 |
|
|
3 |
2.0 |
MnO2 0.5 |
|
回答下列问题:
(1)步骤①中的x应至少称取 g(结果保留1位小数),上述实验步骤中需要使用玻璃棒的是 (填序号)。
(2)表格中的“待测数据”是指 。
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意 (填字母编号)。
a.视线与凹液面最低处相平
 b.读数前不能移动量气管和水准管
b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
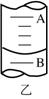
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为 。
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验。(提示:可从催化剂的概念完成实验。)
|
实验步骤 |
设计这一步骤的目的 |
|
实验表明,加入CuO后产生O2的速率比未加入时快得多 |
CuO能加快KClO3的分解 |
|
|
|
|
|
|
27.(5分)小海、小林、小明三同学一起测定双氧水溶液中溶质的质量分数。
查阅资料:2H2O2  2H2O+
O2↑;常温下氧气密度为1.42g/L。
2H2O+
O2↑;常温下氧气密度为1.42g/L。
设计原理:将一定质量的双氧水样品与二氧化锰混合,测定反应产生的氧气的质量,计算出H2O2的质量,继而得双氧水溶液中溶质的质量分数。
过程方法:
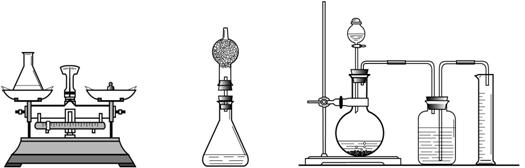
(1)小海首先设计(如左图):向装有样品溶液(20 g)的锥形瓶(75 g)中投入0.5g二氧化锰,待双氧水反应完毕后测得锥形瓶和反应后混合物的总质量为95.1 g,则产生氧气的质量是 g,双氧水溶液中溶质的质量分数为 。
(2)小林对小海的设计提出质疑后,设计如中图的方案(只在上述方案中的锥形瓶上加一干燥管),请你说明小林质疑的理由是 。
(3)小明通过思考后,觉得他们的方案误差都较大,于是小明设计如右图的方案(试剂用量不变)。请你说明小明认为他们误差较大的原因:
。如果要满足小明的要求,该实验需用 mL的量筒。
26.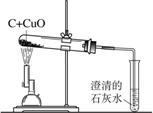 (3分) 某同学为了探究木炭还原氧化铜所生成的气体产物是什么,提出了猜想:a.可能是二氧化碳;b.可能是一氧化碳。并设计如右图所示装置进行实验,预期的实验现象及结论如下:
(3分) 某同学为了探究木炭还原氧化铜所生成的气体产物是什么,提出了猜想:a.可能是二氧化碳;b.可能是一氧化碳。并设计如右图所示装置进行实验,预期的实验现象及结论如下:
① 若澄清的石灰水变浑浊,则气体为二氧化碳;
② 若澄清的石灰水不变浑浊,则气体为一氧化碳。
请你回答:
(1)该同学的猜想是否严谨?若不严谨,请作补充。
(2)请你对该实验装置予以评价。
25.(4分)A、B是实验室二种常见的玻璃仪器。
(1)下表内已绘制其中2种仪器上部约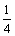 的局部特征,请你分别根据其用途补绘剩余部分。
的局部特征,请你分别根据其用途补绘剩余部分。
|
仪器 |
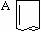 |
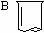 |
|
主要用途 |
用作少量试剂的反应容器,收集少量气体,装配小型气体发生器。 |
用作反应物较多、加热时间较长的反应器,如制取气体等。 |
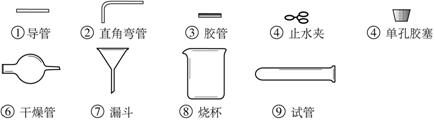
(2)下列仪器可装配一套“随开随用、随关随停”的气体发生装置。请填写所用仪器的序号: (夹持、固定的仪器不考虑)。能用该套装置制取的气体有 (任填两种)。
24.(8分)按表中要求收集四瓶氢气和空气混合气,并点火实验,结果列于表中。
|
V(H2): V(空气) |
2 : 8 |
4 : 6 |
6 : 4 |
8 : 2 |
|
点火处理 |
炸 |
炸 |
炸 |
不炸 |
(1)如何收集混合气[ 以V(H2): V(空气) = 2 : 8 为例]?
(2)由点火实验的结果可知,氢气在空气混合气中爆炸范围的上限在 %(体积,下同)到 %之间。
(3)为进一步精确探究爆炸范围的上限,请再收集三瓶混合气并点火实验。写出具体的方案、结论:
23.(7分)地球是一颗蓝色的星球,表面大部分被海洋覆盖,海水中蕴含的元素多达80多种。通过海水晒制可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。以下是一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):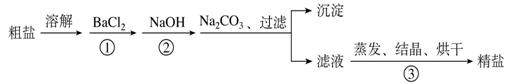
回答下列问题:
(1)操作①能否改用硝酸钡溶液?说明原因。 。
(2)进行操作①后,判断BaCl2过量的方法是
。
(3)加入Na2CO3的目的是 。为什么不先过滤而后加Na2CO3溶液,其理由是 。
(4)滤液的主要成分有 。此实验方案尚需完善,具体步骤是
。
(5)请再写一种实验方案,添加沉淀试剂的步骤为: 。
22.(5分)(1)CaCl2溶液和NaHCO3溶液反应生成CaCO3沉淀。为表示这个反应写出了下列两个反应方程式: CaCl2 + NaHCO3 == CaCO3↓+ NaCl + HCl
CaCl2 + 2 NaHCO3 == CaCO3↓+ 2 NaCl + CO 2↑+ H2O
你认为哪一个反应的化学方程式不合理,并简述理由。
(2)已知难溶的物质在一定条件下可转化成更难溶的物质。将白色Mg(OH)2加到FeCl3溶液中有红棕色沉淀生成。请写出反应的化学方程式并简述理由。
21.(3分)有一种技术可将糖[通式为Ca(H2O)b]发酵进行无氧分解,生成两种化合物,其中一种物质是沼气的主要成分。写出糖发酵进行无氧分解的化学方程式:
,指出a、b之间的关系 。
20.(5分)下列有关的物质及相互转化,都与人类生活有密切关系,其中A、B、M、E均为常见单质,F为难溶于水的白色沉淀。
① 一定量的A在B中点燃可生成C和D的混合物,且C、D均为无色气体,C是常见的还原剂,可与B进一步反应生成D。
② M+B→G(此反应是人类获取能量的最佳反应)
③ D+L→F+G
④ C+K→D+E
(1)写出D和F的化学式:D ,F 。
(2)转化④在金属冶炼中常用来炼 。
(3)A在B中燃烧可能发生反应的化学方程式(写两个):
、 。
19.(4分)二氧化碳是导致温室效应的主要气体,同时,它也是一种宝贵的碳氧资源,在地球上它的含量比天然气、石油和煤的总和还多数倍。
(1)以CO2和NH3合成尿素CO(NH2)2是固定和利用CO2的成功范例,写出经以上途径合成尿素的化学方程式 。若按上述方法生产1000万吨尿素,可固定的CO2将达 万吨。
(2)英国Nature,2005,437:681报道,目前海洋表层海水中溶解的CaCO3 [ 20℃ S(CaCO3) = 0.0013 g/100gH2O ] 处于饱和状态,海洋吸收大气中的CO2可以减弱温室效应,但却使海水中碳酸钙浓度降低,该变化的化学方程式为 CaCO3 + H2O + CO2 == Ca(HCO3)2。海水中CaCO3浓度降低会造成 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com