
题目列表(包括答案和解析)
5.(3分)在我市经济大开发的进程中,要坚持开发与环保并重。某化学课外活动小组在调查一化工厂时发现该厂有甲、乙两个车间,排出的废水澄清透明,经分析分别含有三种不同的离子,共有K+、Ba2+、Cu2+、OH-、NO3-、CO32- 六种离子,经查部分物质的溶解性见下表:
(1)将甲、乙两车间的废水按适当的比例混合,可以变废为宝,既能使废水中的Ba2+、
Cu2+、OH-、CO32- 等离子转化为沉淀除去,又可以用上层清液来浇灌农田。清液中含有的溶质主要是 (填写物质的化学式)。
|
|
OH- |
NO3- |
CO32- |
|
K+ |
溶 |
溶 |
溶 |
|
Ba2+ |
溶 |
溶 |
不 |
|
Cu2+ |
不 |
溶 |
不 |
(2)已知甲车间废水明显呈碱性,则乙车间废水中含有的阴离子是 。
(3)根据以上溶解性表判断,Cu(NO3)2和 Ba(OH)2溶液能发生复分解反应。写出化学方程式
。
Ba(OH)2溶液能发生复分解反应。写出化学方程式
。
4.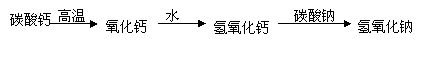 (3分)如果以碳酸钙、碳酸钠、水为原料制取氢氧化钠,可设计如下反应过程:
(3分)如果以碳酸钙、碳酸钠、水为原料制取氢氧化钠,可设计如下反应过程:
如果以锌、稀硫酸和氧化铜为原料制取单质铜,可有两种设计方案,请你按照上面的设计格式,完成以下设计方案。
 方案一:Zn
方案一:Zn
 方案二:CuO
方案二:CuO
在以上两个设计方案中,你认为方案__操作更合理、更简单。
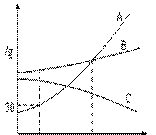
3.(3分)右图是A.B.C三种物质的溶解度曲线,据图回答:
(1)t1℃时A.B.C三种物质的溶解度由大到
小的顺序是______(填写序号,下同)。
(2)t1℃时30gA物质加入到50g水中不断搅拌形成的溶
液质量是______g。 t1 t2
(3)将t1℃时A.B.C三种物质的饱和溶液升温到t2℃时,三种溶液的溶质质量分数由大小关系是 ______。
2.(4分)按要求用化学符号表示下列内容:
①2个铁离子_____②正二价的锰元素_____
 ③一种有机物______④一种金属氧化物_____
③一种有机物______④一种金属氧化物_____
1.(4分)用下列物质填空(填写字母):
a.干冰 b.活性炭 c.天然气 d.纯碱 e.烧碱 f.胆矾
①可除去水中异味的物质是_____;②可用于人工降雨的物质是 ; ③标有"CNG"标志的汽车使用的燃料是 ;④侯氏联合制碱法所生产的“碱”是___________。
30.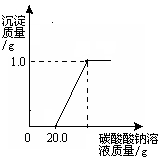 某班同学在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质)。为了对废液进行处理,某同学做了如下实验:取废液缸上层清液20.0g于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液至过量,滴入碳酸钠溶液质量(/g)与生成沉淀的质量
(/g)的变化关系如图所示。(计算结果精确到0.1%)
某班同学在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质)。为了对废液进行处理,某同学做了如下实验:取废液缸上层清液20.0g于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液至过量,滴入碳酸钠溶液质量(/g)与生成沉淀的质量
(/g)的变化关系如图所示。(计算结果精确到0.1%)
求:(1) 当废液中盐酸完全反应时,生成的二氧化碳的质量。
(2) 实验过程中实际参加反应的碳酸钠溶液的质量为多少?
2009年中考如皋市实验初中第二次模拟考试
29.为防止汶川地震灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒, “漂白粉”的有效成分为次氯酸钙[化学式为:Ca(ClO)2]。请回答:
(1)次氯酸钙中钙、氯、氧三种元素的质量比为 ▲ 。
(2)次氯酸钙中氯元素的质量分数是 ▲ (精确到0.1%)。
(3)若灾区饮用水需要5%漂白粉溶液250g来消毒,则需要20%的漂白粉溶液 ▲ g。
28.废旧干电池中许多物质应该是可以回收利用的。某种型号干电池的剖面如下图
所示。请回答下列问题:
 (1)提取干电池内填充物中的MnO2:取填充物溶于水、过滤、洗涤,得到黑色不溶物。再经过 ▲ 的处理,即得到MnO2。
(1)提取干电池内填充物中的MnO2:取填充物溶于水、过滤、洗涤,得到黑色不溶物。再经过 ▲ 的处理,即得到MnO2。
(2)取(1)中过滤得到的滤液,分为两份,一份加入烧碱溶液,加热产生一种刺激性气味的气体,该气体的水溶液pH>7,且常用作化肥,则该气体的化学式为 ▲ ;另一份加入AgNO3溶液,产生白色沉淀,滴加稀HNO3沉淀不溶解,则可推知A物质的化学式为 ▲ 。
(3)提到化肥,小明联想到暑假期间在农田施肥时,发现撒落在地上的碳酸氢铵在阳光的照射下很快消失了,同时有浓烈的刺激性气味。他很好奇,返校后和同学们进行探究,请你一同参与:
[提出问题]温度较高时,碳酸氢铵能分解吗?产物是什么?
[猜想假设]碳酸氢铵受热易分解,产物可能为水、二氧化碳、氨气。
[资料查阅]红色石蕊试纸遇碱溶液变蓝,蓝色石蕊试纸遇酸溶液变红。
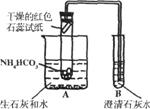 [实验设计]小明设计了如图所示的装置进行实验(夹持装置省略)。
[实验设计]小明设计了如图所示的装置进行实验(夹持装置省略)。
①根据现象: ▲ ,证明实验后生成了水和氨气。
②装置B中澄清石灰水 ▲ ,证明产物中有二氧化碳生成。
③小红同学认为若将装置B中澄清石灰水改为NaOH溶液,再通过实验验证B中产物,也可以证明碳酸氢铵分解后有二氧化碳生成。请你帮她设计并完成验证B中产物的实验:
|
实验步骤 |
实验现象 |
反应的化学方程式 |
|
▲ |
▲ |
▲ |
[实验结论]碳酸氢铵受热易分解,其反应的化学方程式为 ▲ 。
[实验反思]根据以上实验,你认为碳酸氢铵化肥在存放时应注意的问题是 ▲ 。
27.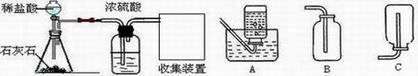 为探究CO2的化学性质,需要制取并收集干燥的CO2,以下是老师提供的一些实验装置。
为探究CO2的化学性质,需要制取并收集干燥的CO2,以下是老师提供的一些实验装置。
⑴ 实验室制取CO2的化学方程式为 ▲ ,收集装置为 ▲ (填字母),检验二氧化碳是否收集满的方法是 ▲ ,观察火焰是否熄灭。
⑵ 化学课上,李芹同学将燃烧的钠迅速伸入盛有CO2的集气瓶中,钠在瓶中继续燃
烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
[提出问题]黑色颗粒和白色物质可能是什么呢?
[进行猜想]你认为黑色颗粒是 ▲ ,小明认为白色物质是氧化钠,小艺认为是碳
酸钠,小亮认为是氧化钠和碳酸钠的混合物,小华认为是氢氧化钠。
你认为 ▲ 的猜想是错误的,其理由是 ▲ 。
[查阅资料]CaCl2+Na2CO3=CaCO3↓+2NaCl,氧化钠为白色粉末,溶于水生成氢氧化钠。
[实验探究]李芹同学对白色物质进行实验探究。
实验方案1:取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,向其
中加入无色酚酞试液,观察到溶液变成红色,结论:白色物质为氧化钠。
实验方案2:取该样品少量于试管里,加入适量的水,振荡,样品全部溶于水,向其
中加入过量的CaCl2溶液,出现白色沉淀,然后过滤,再向溶液里滴加无色酚酞试液,无明显现象出现。结论:白色物质为 ▲ 。
[反思评价]小娟同学认为实验方案1得出的结论不正确,其理由是 ▲ 。
[得出结论] 钠在二氧化碳中燃烧的化学方程式为 ▲ 。
26.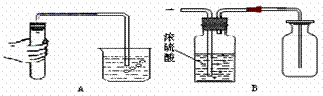 请你根据下图回答有关问题:
请你根据下图回答有关问题:
⑴ 图A实验操作的目的是检验装置的气密性,从该图观察到的实验现象中,你能得出的结论是 ▲ ;
⑵ 能用图B所示装置来干燥并收集的气体应具备的性质是: ▲ , ▲ 。(写两条)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com