
题目列表(包括答案和解析)
22. 下列各组溶液,不另加试剂只用相互混合的方法就能鉴别的是( )
(A) K2SO4、 K2CO3、 BaCl2、 KCl
(B) Na2SO4、 BaCl2、 KCl、 KNO3
(C) AgNO3、 HCl、 KCl、 KNO3
(D) KOH、 K2SO4、 Fe2(SO4)3、 MgSO4
21. 已知c1、c2、a1、a2、pH1、pH2分别表示2种一元弱酸的摩尔浓度、电离度和溶液的
pH值。若pH1<pH2,且a1>a2,则c1和c2的关系为( )
(A) c1>c2 (B) c1=c2
(C) c1<c2 (D) 无法确定
20. 由下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是( )
(A) 6和8 (B) 11和8
(C) 11和16 (D) 12和17
19. 下列说法中不正确的是( )
(A) 任何酸都不能与二氧化硅发生氧化-还原反应
(B) 二氧化硅是制造水泥的主要原料,它在高温下可与石灰石发生反应
(C) 二氧化硅属于原子晶体,具有四面体的空间网状结构
(D) 烟水晶的主要成分为二氧化硅
18. 某有机物的结构为:CH2=CH-C6H5(-OH)-OCH3它不可能具有的性质是( )
① 易溶于水; ② 可以燃烧; ③ 能使酸性KMnO4溶液褪色;
④ 能跟KOH溶液反应; ⑤ 能跟NaHCO3溶液反应; ⑥ 能发生聚合反应
(A) ①、④ (B) ①、②、⑥
(C) ①、⑤ (D) ③、⑤、⑥
17. 把等质量的金属镁分别放在①纯氧气中、②空气中、③二氧化碳气体中,充分燃烧。
得到固体物质的总质量依次分别是W1、W2、W3,三者的大小关系是( )
①、 无法判断 ②、 W1一定小于W2
③、 W3一定大于W2 ④、 W1等于W3
(A) ①、② (B) ②、④
(C) ②、③ (D) ③、④
16. 用Pt电极电解一定浓度的下列物质的水溶液,在电解后的剩余电解液中加入适量水时,
能使溶液浓度恢复到电解前浓度的是( )
①、 AgNO3 ③、 NaOH ②、 Na2SO4 ④、 CuCl2
(A) ①、② (B) ②、④
(C) ②、③ (D) ③、④
15. 蓄电池是一种直流电源,它的用途很广。已知蓄电池在放电时是起原电池作用,在充电
时是起电解作用。其中铅蓄电池是最常用的蓄电池之一,它的两极材料是Pb和PbO2,
电解质是稀H2SO4,放电时电极反应为:Pb - 2e + SO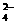 = PbSO4↓
= PbSO4↓
PbO2 + 2e + 4H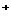 + SO
+ SO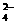 = PbSO4↓+ 2H2O
= PbSO4↓+ 2H2O
铅蓄电池充电时,PbO2极上的电极反应是( )
(A) PbSO4
+ 2e = Pb + SO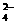
(B) PbO2
+ 2e + 4H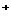 + SO
+ SO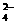 = PbSO4↓+ 2H2O
= PbSO4↓+ 2H2O
(C) Pb - 2e + SO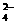 = PbSO4 ↓
= PbSO4 ↓
(D) PbSO4
+ 2H2O - 2e = PbO2 + 4H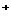 + SO
+ SO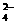
13. 将0.2摩/升NH4Cl溶液与0.1摩/升NaOH溶液等体积混合后,溶液中下列微粒的物质
的量浓度的关系正确的是( )
(A) [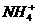 ]=[
]=[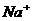 ]=[
]=[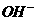 ]>[
]>[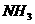 ·
·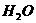 ]
]
(B) [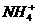 ]=[
]=[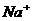 ]>[
]>[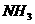 ·
·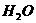 ]>[
]>[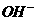 ]
]
(C) [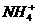 ]>[
]>[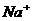 ]>[
]>[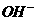 ]>[
]>[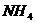 ·
·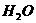 ]
]
(D) [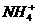 ]>[
]>[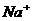 ]>[
]>[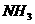 ·
·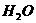 ]>[
]>[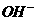 ]
]
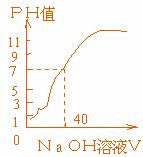 14. 用1.0摩/升NaOH溶液中和某浓度
14. 用1.0摩/升NaOH溶液中和某浓度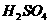 溶液其pH值和所用NaOH溶液体积(V)关系如
溶液其pH值和所用NaOH溶液体积(V)关系如
图所示,则原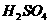 溶液的物质的量浓度和完全反应后
溶液的物质的量浓度和完全反应后
溶液的大致体积是( )
(A) 1.0 摩/升,60 毫升
(B) 0.5 摩/升,80 毫升
(C) 0.5 摩/升,40 毫升
(D) 1.0 摩/升,80 毫升
12.
已知一种[H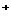 ]=1×10
]=1×10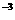 摩/升的酸溶液和一种[OH
摩/升的酸溶液和一种[OH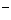 ]=1×10
]=1×10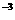 摩/升的碱溶液等体
摩/升的碱溶液等体
积混合后溶液呈现碱性,其原因可能是( )
①、 浓的强碱和稀的强酸溶液反应 ②、 浓的弱碱和稀的强酸溶液反应
③、 等浓度的强碱和弱酸溶液反应 ④、 生成了一种强碱弱酸盐
(A) ①、② (B) ②、④
(C) ②、③ (D) ③、④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com