
题目列表(包括答案和解析)
20.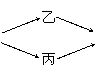 (10分)甲、乙、丙、丁四种烃的含氧衍生物,其分子中都含有一个或一个以上的官能团,通过下列转化关系可由甲制取丁:
(10分)甲、乙、丙、丁四种烃的含氧衍生物,其分子中都含有一个或一个以上的官能团,通过下列转化关系可由甲制取丁:
甲 丁
若丁的相对分子质量总为甲的两倍,乙的相对分子质量总大于丙。回答下列问题:
⑴乙的分子结构中一定含有的官能团是 (填名称);丙的分子结构中一定含有的官能团的电子式为 。
⑵乙、丙的相对分子质量之差为 (填一个数字)的整数倍。
⑶满足上述转化关系的甲、乙、丙、丁中,相对分子质量最小的甲的结构简式为 ,此时,生成丁的化学方程式为 。
19.(12分)NH4NO3在不同条件(温度)下加热分解,可能发生非氧化还原反应,也可能发生氧化还原反应
⑴若NH4NO3在通常条件下加热的分解产物不出下列范围,根据已学知识(化合价升降规律等)判断,下列反应可能的是 (有错选得“0”分)
A、NH4NO3→N2+O2+H2O B、NH4NO3→NH3+HNO3
C、NH4NO3→O2+HNO3+H2O D、NH4NO3→N2+HNO3+H2O
E、NH4NO3→N2+NH3+H2O F、NH4NO3→N2O+H2O
⑵现将NH4NO3晶体在三种不同温度下加热使其分解,若分解产物能发生如图所示的转化关系(仅反应条件及反应Ⅱ、Ⅲ两个反应中生成的水被略去)
回答下列问题
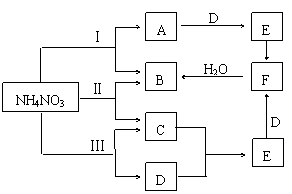
①写出下列物质的分子式
A、 E、 F、
②请写出反应Ⅲ的化学方程式
Ⅲ、
18.(12分)已知胆矾在不同温度下可以逐步失水:
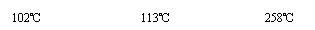
CuSO4·5H2O--→CuSO4·3H2O--→CuSO4·H2O--→CuSO4
某课外活动小组准备用浓硫酸和铜片为主要原料制取少量胆矾,其主要步骤有:①取少量铜片放在干燥的蒸发皿内,用酒精灯灼烧到其表面变黑为止;②向蒸发皿内加入一定量浓硫酸并加热,反应结束后发现有少量黑色固体及白色固体存在;③将上述冷却后的反应混合物用水稀释得蓝色溶液,白色固体消失,但仍有黑色固体存在;④向稀释后的所得溶液中加入过量碱式碳酸铜[Cu2(OH)2CO3],充分搅拌;⑤过滤,弃去不溶物;⑥将滤液转回洗净的蒸发皿内,用沸水浴缓缓加热蒸发,浓缩至表面有晶膜析出时为止,取下蒸发皿使溶液冷却,析出蓝色晶体。
⑴步骤⑤中要用到的玻璃仪器有 。
⑵步骤④中发生反应的离子方程式是 。
⑶简述步骤③的具体操作方法
。
⑷下列叙述错误的是 (有错选得“0”分)
A、将铜片灼烧,可以减少浓硫酸的消耗量。
B、用浓硫酸溶解灼烧后的铜片时,应在通风橱中进行。
C、步骤②中得到的黑色固体是CuO。
D、步骤②中得到的白色固体是CuSO4。
E、步骤⑥中为加快蒸发速度,也可用酒精灯直接给蒸发皿加热。
17.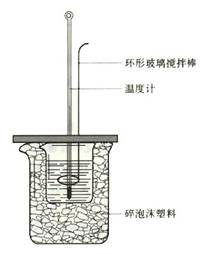 (10分)实验室用50 mL 1.0 mol·L-1盐酸跟50
mL 1.1 mol·L-1氢氧化钠溶液在下图装置中进行中和反应,并通过测定反应过程中所放
(10分)实验室用50 mL 1.0 mol·L-1盐酸跟50
mL 1.1 mol·L-1氢氧化钠溶液在下图装置中进行中和反应,并通过测定反应过程中所放
出的热量来计算中和热。试回答下列问题: ⑴大小烧杯间填满碎泡沫塑料的作用是 。
⑵ (填“能”或“不能”)将环形玻璃搅拌棒
改为环形金属(如铜)棒。其原因是 。
⑶大烧杯上如不盖硬纸板,对求得中和热数值的影响
是 (填“偏高”或“偏低”或“无影响”)。
⑷如果改用60 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1
氢氧化钠溶液进行反应,则与上述实验相比,所放热量
(“增加”、 “减少”或“不变”),理由是
;
所求中和热数值 (“增加”、 “减少”或“不变”),
理由是 。
16.将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X。将1.892gX中Cr元素全部氧化成Cr2O72-, Cr2O72-可与过量的KI发生氧化还原反应氧化出2.667g I2,反应的离子方程式是:Cr2O72-+6I-+14H+=2Cr3++3 I2+7H2O,如果取溶有1.892g X的溶液,加入过量的AgNO3,可得4.52gAgCl沉淀,则表示X组成的化学式为
A.K3Cr2Cl7 B.K3Cr2Cl5
C.K3Cr2Cl9 D.K2CrCl4
第II卷(非选择题,共62分)
15.某二元酸(化学式用H2A表示)在水中的电离方程式是: H2A == H++HA-,
HA- H++A2-;则在0.1mol.L-1的Na2A溶液中,下列微粒浓度关系式不合理的是
H++A2-;则在0.1mol.L-1的Na2A溶液中,下列微粒浓度关系式不合理的是
A.c(A2-) +c( HA-)+c( H2A) =0.1mol·L-1 B.c(OH-)=c(H+) +c( HA-)
C.c(Na+ )+ c(H+) =c(OH-)+ c( HA-)+2c(A2-) D.c(Na+ )= 2c(A2-) +2c( HA-)
14.新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式为:
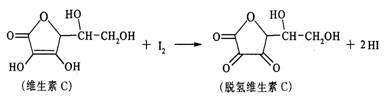
下列说法正确的是
A.上述反应为取代反应 B.滴定时可用淀粉溶液作指示剂
C.滴定时应剧烈振荡锥形瓶 D.维生素C的分子式为C6H7O6
13.将含有O2和CH4的混合气体置于盛有23.4 g Na2O2的密闭容器中,电火花点燃,反应结束后,容器内的压强为零(150℃),将残留物溶于水中,无气体产生。下列叙述正确的是
A.原混合气体中O2和CH4的体积比为2∶1 B.残留物只有Na2CO3
C.原混合气体中O2与CH4的体积比为1∶1 D.残留物只有Na2CO3和NaOH
12.在右下图的实验装置中,从实验开始过一段时间,对看到的现象叙述不正确的是
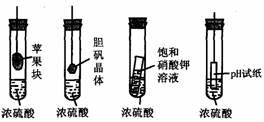
A.苹果块会干瘪 B.胆矾晶体表面有“白斑”
C.小试管内有晶体析出 D.pH试纸变红
11.某温度下,在一容积可变的容器中,反应2A(g)+B(g)  2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol,在保持温度不变的条件时下列操作不会使平衡右移的是
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol,在保持温度不变的条件时下列操作不会使平衡右移的是
A.压强不变时,A、B和C均增加lmol
B.压强不变时,充入少量不参与反应的氖气
C.容积不变时,A、B和C均增加1mol
D.容积不变时,充入物质的量之比为2∶1的A和B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com