
题目列表(包括答案和解析)
7.将SO2通入BaCl2溶液至饱和未见沉淀,继续通入另一气体仍无沉淀,通入的气体可能是( )
A.CO2 B.NH3 C.NO2 D.H2S
6.在相同状况下,将下列四种混合气体:①体积比为3∶1的NH3和N2 ②体积比为 1∶1的NO2和N2 ③体积比为1∶1的NO2和O2 ④体积比为4∶1的NO2和O2,分别置于相同的四支试管中并倒置于水槽中,充分反应后液面上升高度分别为h1、h2、h3、h4,下列关系正确的是( )
A.h1>h2>h3>h4 B.h4>h3>h2>h1
C.h4>h1>h3>h2 D.h2>h3>h1>h4
5.磷酸的结构式为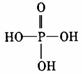 ,两个磷酸分子可脱去一分子水生成焦磷酸(H4P2O7)。含磷洗衣粉中含有三聚磷酸钠(Na5P3O10),1mol此钠盐中P-O键的物质的量为( )
,两个磷酸分子可脱去一分子水生成焦磷酸(H4P2O7)。含磷洗衣粉中含有三聚磷酸钠(Na5P3O10),1mol此钠盐中P-O键的物质的量为( )
A.7mol B.8mol C.9mol D.12mol
4.在一定条件下,RO3-与R-可发生反应:RO3-+5R+6H+=3R2+3H2O下列关于R元素的叙述中,正确的是( )
A.R位于周期表中VA族 B.R的气态氧化物的水溶液是强酸
C.RO3-中的R只能被还原 D.R2在常温常压下一定是气体
3.地壳中含量第一和第二的两元素形成的化合物,不具有的性质是( )
A.熔点很高 B.是酸酐,与水反应生成对应的酸
C.可与纯碱反应 D.与碳在高温下反应可制取两元素中一种单质
2.下列叙述中正确的是( )
A.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
B.凡质子数相同的微粒,其化学性质一定相同
C.含氧酸可作氧化剂,无氧酸只能作还原剂
D.元素的非金属性越活泼,其阴离子的还原性越弱
1.下列说法从化学角度分析,其中不正确的是( )
A.高温高压下可将石墨转变为金刚石
B.从煤焦油中可分馏出苯、甲苯、酚等有机物
C.制取镁粉时,可将镁蒸气在氮气中冷却
D.“氮的固定”是指将空气中游离的氮转变为氮的化合物的方法
5.还原法:C+H2O CO+H2,Zn+2HCl=ZnCl2+H2↑ 2C+ SiO2
CO+H2,Zn+2HCl=ZnCl2+H2↑ 2C+ SiO2 Si+2CO↑
Si+2CO↑
[思维技巧点拨]
例1
(1)氰化钾、氰化氢的制备反应式为:K2CO3+C+2NH3 2KCN+3H2O;△H=+276kJ/mol ①
2KCN+3H2O;△H=+276kJ/mol ①
CO+NH3 HCN+H2O;△H=+46kJ/mol ②
HCN+H2O;△H=+46kJ/mol ②
氰离子为负一价(CN-),其中碳氮元素的化合价分别为________。以上两个反应是否均为氧化还原反应?(2)制备纯净无水HCN(沸点299K)的另一种方法是 :混合磨细的KCN和KHS粉末适度加热①试写出这个反应式。②为什么要磨细和用粉末?③为什么要强调适度加热?
解析 据共价键理论,一般当碳同非金属性比它强的元素结合时,碳显正价,氮为负价,为-3价,所以(CN-)中碳为+2价,氮为-3价。故①为氧化还原反应,②为非氧化还原反应。第二种方法制备HCN是固体与固体之间的反应,故磨细和用粉末的目的是增大表面积,加快反应速率,据题意知,第二种方法制备HCN如温度太低,反应速率较小,温度太高,则酸式盐易分解发生副反应:2KHS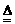 K2S+H2S↑。该反应的化学方程式为KCN+KHS
K2S+H2S↑。该反应的化学方程式为KCN+KHS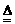 HCN↑+K2S。
HCN↑+K2S。
例2 金属M可以在不同条件下发生下列五个反应:M+A→I, M+B→H, M+C→H+F, M+D→H+A, M+E→I+G。 其中(1)A、B、C、D、E在通常情况下都是气体,并且C是CO 2。(2)上述反应的产物,在不同条件下,还可和有关反应物发生下列反应:F+B→C A +G→E,(3)I是一种离子化合物,它可以水解产生一种白色沉淀和E。该白色沉淀加热可分解为H和H2O。而E则是分子晶体,其分子中共有10个电子,根据以上条件,判断并写出 有关物质的化学式:A________,B________,C________,D________,E________,F________,G________,H________,I________,M________。
解析 本题的突破口是M+C→H+F,而C为CO2。一般同CO2能发生反应的金属就现有知识来讲,只能是Mg。F、H中有一为碳,根据F+B→C,则C为CO2,B为气体,F肯定为碳,H为MgO。扫描全题,得知E是分子晶体,且其分子中共有10个电子。分子中有10个电子的有:HF、H2O、NH3、CH4等。而E又通过一种离子化合物水解而得到,E可能为 HF或NH3。如E为HF,根据M+E→I+G,HF同Mg作用,但事实HF同Mg不反应。如为NH3同样根据A+G→E,A为N2或H2。因为Mg可跟A作用,显然A为N2,I为Mg3N2。再根据M+D→H+A,M为Mg,H为MgO,A为N2,则D只能为NO2。
A:N2,B:O2,C:CO2,D:NO2,E:NH3,F:C,G:H2,H:MgO,I:Mg 3N2,M:Mg。

[能力突破练习]
4.氧化法:如MnO2+4HCl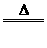 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
4NaBr+3H2SO4+MnO2=2Na2SO4+MnSO4+2Br2+3H2O
2H2S+SO2=3S+2H2O
3.置换法:如Cl2+2NaBr=2NaCl+Br2 2H2S+O2(不足) 2H2O+2S
2H2O+2S
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com