
题目列表(包括答案和解析)
16.(05江苏3.)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3 + N2 + 3 C 高温 2 AlN + 3 CO 下列叙述正确的是
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为-3
D.氮化铝晶体属于分子晶体
第I卷答题表 班考号 姓名
第Ⅱ卷(非选择题共60分)
15.(05江苏7.)已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2氧化性依次减弱。下列反应在水溶液中不可能发生的是
A.3 Cl2 + 6 FeI2 = 2FeCl3 + 4 FeI3 B.Cl2 + FeI2 = FeCl2 + I2
C.Co2O3 + 6 HCl = 2CoCl2 + Cl2↑+ 3H2O D.2Fe3+ + 2I- = 2Fe2+ + I2
14.(05广东21.)从海水中可以提取溴,主要反应为:2Br-+Cl2=2Cl-+Br2,下列说法正确的是
A.溴离子具有氧化性 B.氯气是还原剂C.该反应属于复分解反应 D.氯气的氧化性比溴单质强
13.(05江苏8.)在下列生成二氧化硫的反应中,反应物中的含硫物质被氧化的是
A 硫在空气中燃烧 B 铜片与浓硫酸共热
C 红热的木炭与浓硫酸反应 D 亚硫酸钠与稀硫酸反应
12.(05江苏11.)能用离子方程式H++OH-=H2O表示的反应是(b)
A 稀醋酸和稀氨水反应 B 稀硫酸和烧碱溶液反应
C 稀盐酸和氢氧化铜反应 D 稀硫酸和氢氧化钡溶液反应
11.(05全国卷Ⅲ11.)已知KH和H2O反应生成H2和KOH,反应中1 mol KH
A.失去1 mol电子 B.得到1 mol电子 C.失去2 mol电子 D.没有电子得失
10.(05江苏9.)下列离子方程式正确的是
A.碳酸氢钠溶液与少量石灰水反应 HCO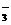 + Ca2+ + OH- = CaCO3↓ + H2O
+ Ca2+ + OH- = CaCO3↓ + H2O
B.氯化铵与氢氧化钠两种浓溶液混合加热OH- + NH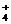 △
H2O
+ NH3↑
△
H2O
+ NH3↑
C.氢氧化镁与稀硫酸反应 H+ + OH- = H2O
D.单质铜与稀硝酸反应 Cu + 2 H++ 2NO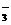 = Cu2+ + 2NO↑+H2O
= Cu2+ + 2NO↑+H2O
9.(05广东22.)下列反应的现象描述与离子方程式都正确的是
A.金属镁与稀盐酸反应,有氢气产生:Mg + 2H++ 2Cl- == MgCl2 + H2↑
B.氯化钡溶液与硫酸反应,有白色沉淀产生;Ba2+ + SO42- == BaSO4↓
C.碳酸钠溶液与盐酸反应,有气泡逸出;Na2CO3 +2H+ == 2Na+ + H2O + CO2↑
D.过量铁粉与氯化铁溶液反应,溶液变浅绿色;Fe + Fe3+ == 2Fe2+
8.(05全国卷Ⅲ13.)能正确表示下列反应的离子方程式是
A.甲酸钠溶液和盐酸反应:HCOO-+H+=HCOOH
B.硫化钠的第一步水解:S2-+2H2O H2S+2OH-
H2S+2OH-
C.醋酸钡溶液和硫酸反应:Ba2++SO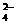 =BaSO4↓
=BaSO4↓
D.氢氧化钙溶液和碳酸氢镁反应: Ca2++OH-+HCO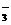 =CaCO3↓+H2O
=CaCO3↓+H2O
7. (05江苏4.)氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2(g) + 1/2O2(g) = H2O(l);△H= -285.8 kJ/mol
CO(g) + 1/2O2(g) = CO2(g);△H= -283.0 kJ/mol
C8H18(l) + 25/2O2(g) = 8CO2(g) + 9 H2O(l);△H= -5518 kJ/mol
CH4(g) + 2 O2(g) = CO2(g) + 2 H2O(l);△H= -890.3 kJ/mol
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是
A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com