
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
4£®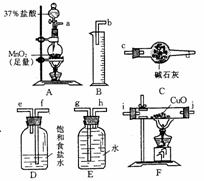 ʵÑéỂ¿ÉÓĂ2Cl2+2CuO=2CuCl2+O2µÄ·´Ó¦À´²â¶¨ÍµÄ½üËÆÏà¶ÔÔ×ÓÖÊÁ¿¡£ÊԻشđ£º
ʵÑéỂ¿ÉÓĂ2Cl2+2CuO=2CuCl2+O2µÄ·´Ó¦À´²â¶¨ÍµÄ½üËÆÏà¶ÔÔ×ÓÖÊÁ¿¡£ÊԻشđ£º
(1)Ϊ²â¶¨·´Ó¦ÎïCuOµÄÖÊÁ¿[¼Ç×÷m(CuO)g]ºÍÉú³ÉÎïO2µÄ̀å»ư(±ê×¼×´¿öÏÂ)[¼Ç×÷V(O2)mL]£¬ÇëÓĂͼËùÁĐ̉ÇÆ÷Éè¼Æ̉»¸ö¼̣µ¥µÄʵÑé·½°¸£º
¢Ù°´Æø̀åÁ÷Ị̈´Ó×óµ½Ó̉£¬ÓĂÈ齺¹Ü(ͼÖĐδ»³ö)Á¬½ÓÉÏÊö̉ÇÆ÷£¬×éºÏ³É̉»̀×ʵÑé×°ÖĂ£¬ƠưÈ·µÄÁ¬½Ó˳Đ̣ÊÇ¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡(Óõ¼¹Ü¿ÚĐ̣ºÅ̀îĐ´)£¬×°ÖĂCµÄ×÷ÓĂÊÇ¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡ ¡¡¡£ÊµÑéÍê±ÏʱÔÚFµÄ·´Ó¦¹ÜÖĐ¹Û²́µ½µÄÏÖÏóÊÇ¡¡¡¡ ¡¡¡¡¡¡¡¡ ¡£
¢Ú¼ÆËăCuµÄÏà¶ÔÔ×ÓÖÊÁ¿µÄ±í´ïʽÊÇ¡¡¡¡¡¡¡¡¡£(̉ÑÖªÑơµÄÏà¶ÔÔ×ÓÖÊÁ¿Îª16)
(2)ÏÂÁĐÇé¿öÖĐ»áʹ²â¶¨½á¹ûÆ«´óµÄÊÇ¡¡¡¡¡¡¡£
A£®CuOδȫ²¿×ª»¯ÎªCuCl2¡¡ B£®CuOÊܳ±
C£®CuOÖĐ»́ÓĐCu¡¡¡¡¡¡¡¡D£®Î´Ê¹ÓĂC×°ÖĂ¡¡¡¡¡¡¡¡ E£®Î´Ê¹ÓĂD×°ÖĂ
(3)Èç¹ûÈÔ²ÉÓĂÉÏÊö̉ÇÆ÷Éè¼ÆÁíÍâµÄʵÑé·½°¸£¬»¹¿É̉ԲⶨÆäËûÎïÀíÁ¿À´Çó³öCuµÄÏà¶ÔÔ×ÓÖÊÁ¿£¬ƠâĐ©ÎïÀíÁ¿ÊÇ¡¡¡¡¡¡¡£
A£®m(CuO)¡¢m(CuCl2)¡¡¡¡B£®m(Cl2)¡¢V(O2)
C£®m(CuCl2)¡¢V(O2)¡¡¡¡¡¡D£®V(HCl)¡¢V(O2)
(±¾̀⿼²éÁËÆø̀åµÄÖƱ¸ÔÀí¡¢¾»»¯·½·¨¡¢Êư¾ƯµÄ²É¼¯ºÍ´¦Àí£¬ÀûÓĂ³£ÓõĻ¯Ñ§̉ÇÆ÷×÷¶¨Á¿ÊµÑéµÈÉè¼ÆʵÑé·½°¸µÄÄÜÁ¦¡£´đ̀âʱ̉À¾ƯÎïÖÊÖƱ¸µÄ̉»°ă˼·£¬Àä¾²µØÉó̀â¡¢ÁªÏµËùѧ¹ưµÄʵÑé֪ʶºÍʵÑé¼¼ÄÜ£¬½øĐĐ֪ʶÀà±È¡¢Ç¨̉Æ¡¢ÖØ×飬ȫĂæ¶øϸÖµÄ˼¿¼¿É»Ø´đÎỀâ¡£)
3£®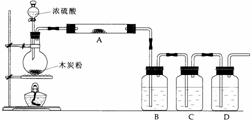 ¸ù¾ƯÏÂͼ»Ø´đÎỀ⣺
¸ù¾ƯÏÂͼ»Ø´đÎỀ⣺
(1)ÉÏÊö×°ÖĂÖĐ£¬ÔÚ·´Ó¦Ç°ÓĂÊÖƠƽồùÉƠÆ¿Íâ±Ú¼́²é×°ÖõÄÆøĂÜĐÔ£¬Èç¹Û²́²»µ½Ă÷ÏÔµÄÏÖÏ󣬻¹¿É̉ÔÓĂÊ²Ă´¼̣µ¥µÄ·½·¨Ö¤Ă÷¸Ă×°ÖĂ²»Â©Æø¡£
´đ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£»
(2)Đ´³öŨẠ́ËáºÍľ̀¿·ÛÔÚ¼ÓÈÈ̀ơ¼₫Ï·¢Éú·´Ó¦µÄ»¯Ñ§·½³̀ʽ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(3)Èç¹ûÓĂͼÖеÄ×°ÖĂ¼́ÑéÉÏÊö·´Ó¦µÄÈ«²¿²úÎï£¬Đ´³öÏÂĂæ±êºÅËù±íʾµÄ̉ÇÆ÷ÖĐÓ¦¼ÓÈëµÄÊÔ¼ÁµÄĂû³Æ¼°Æä×÷ÓĂ£º
AÖĐ¼ÓÈëµÄÊÔ¼ÁÊÇ¡¡¡¡¡¡¡¡¡¡ £¬×÷ÓĂÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
BÖĐ¼ÓÈëµÄÊÔ¼ÁÊÇ¡¡¡¡¡¡¡¡¡¡ £¬×÷ÓĂÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
CÖĐ¼ÓÈëµÄÊÔ¼ÁÊÇ¡¡¡¡¡¡¡¡¡¡ £¬×÷ÓĂÊdzư¾¡¡¡¡¡ Æø̀å¡£
DÖĐ¼ÓÈëµÄÊÔ¼ÁÊÇ¡¡¡¡¡¡¡¡¡¡ £¬×÷ÓĂÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(4)ʵÑéʱ£¬CÖĐÓ¦¹Û²́µ½µÄÏÖÏóÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(¸Ằ⿼²éѧÉú¶Ô½Ï¸´ÔÓ×°ÖĂÆøĂÜĐԵļ́²éÇé¿ö£¬Å¨Ạ́ËáÓëľ̀¿·Û·´Ó¦²úÎï¼́Ñé·½°¸µÄÉè¼ÆÓëÆÀ¼ÛÄÜÁ¦¡£´đ̀âʱ̉ª×¢̉âÈưÖÖ²úÎï¼́ÑéµÄÏȺó˳Đ̣£¬Åųư¿ÉÄܲúÉúµÄ¸ÉÈÅ¡£)
2£®ÇëÉè¼Æ¼̣µ¥µÄ·½°¸Ö¤Ă÷KMnO4ÈÜ̉ºµÄÑƠÉ«ÊÇÓÉÓÚMnO4-µÄ´æÔÚ¶ø̉ưÆđµÄ£¿(ÓöàÖÖ·½·¨)
(´Ë̀⿼²éѧÉú¶ÔÎïÖʵļ́ÑéʵÑé·½°¸Éè¼ÆµÄÄÜÁ¦¡£
´đ̀âʱÀûÓĂÎïÖʵÄĐÔÖÊ£¬Í¨¹ư¶Ô±È½â¾öÎỀâ¡£)
1£®Ä³Ñ§ÉúÀûÓĂ³ø·¿ÖеÄÓĂÆ·½øĐĐĐ¡ÊµÑéÑĐ¾¿£¬ÏÖÓĐ£º¼¦µ°¿Ç¡¢Ê³´×¡¢´¿¾»Ë®¡¢Ê³ÑΡ¢¸Éµç³Ø¡¢Ê¯Ä«µç¼«¼°µ¼Ïߣ¬ÄăÈÏΪËû²»ÄÜÍê³ÉµÄ¼̉Í¥Đ¡ÊµÑéÓĐ(¡¡ )
A£®³ưÈ¥¼¦µ°°×ÈÜ̉ºÖеÄÉÙÁ¿Ê³ÑΡ¡¡¡ B£®×ÔÖƼ̉ÓĂº¬´ÎÂÈËáÄÆÈÜ̉ºµÄÏû¶¾¼Á
C£®¼́ÑéµâÑÎÖĐÊÇ·ñ¼ÓÓеâËá¼Ø¡¡¡¡¡¡ D£®³ưÈ¥ÈÈˮƿµ¨ÄÚµÄË®¹¸
(±¾̀âÊÇ»¯Ñ§ÁªÏµÉú»îʵ¼ÊµÄÎỀ⣬¿¼²éѧÉú¶ÔËù̀ṩÓĂÆ·µÄ×é³É¡¢ĐÔÖÊẾϤµÄÇé¿ö̉Ô¼°Áé»îÔËÓĂÄÜÁ¦¡£´đ̀âʱע̉âÍê³ÉƠâĐ©ÊµÑéµÄ̀ơ¼₫¡£)
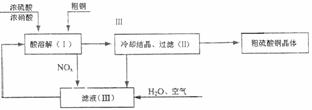
2£®(2003ÄêÄϾ©ÊиßÈư»¯Ñ§Ä£Äầâ)̉ÔŨẠ́ËᡢŨÏơËá¡¢´ÖÍ¡¢Ë®ºÍ¿ƠÆøΪÔÁÏ¿ÉÖƵĂẠ́ËáÍ(CuSO4¡¤5H2O)¡£ÖÆÈ¡Ạ́Ëá;§̀åµÄ¹ư³̀ÈçÏÂͼËùʾ¡£
 ¡¡
¡¡
(1)Đ´³öÖÆÈ¡Ạ́Ëá͵Ä×Ü·´Ó¦·½³̀ʽ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)ÔÚÉÏÊöÉú²ú¹ư³̀ÖĐ£¬±»Ñ»·Ê¹ÓõÄÎïÊÇ¡¡¡¡¡¡¡¡ ¡£
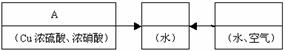
(3)ÇëÄăÑ¡ÓĂÏÂÁĐÊỂ˵Ä×°ÖĂÀ´Ä£ÄâÉÏÊöÉú²ú¹ư³̀¡£½«ËüĂǵıàºÅ̀îÈë·½¿̣¡£

 ¡¡
¡¡
(±¾̀⿼²éÁËѧÉú¶Ô¼¸ÖÖ³£¼ûÎïÖÊĐÔÖʵÄƠÆÎƠÇé¿ö¼°·ÖÎöÆÀ¼ÛÄÜÁ¦¡£´đ̀âʱÓÉ̀â¸ø̀ơ¼₫È·¶¨·´Ó¦ÔÀí£¬¿´¶®Á÷³̀ͼ£¬Ă÷È·¸÷²½µÄʵÑéÄ¿µÄ£¬Í¨¹ư·ÖÎö¡¢±È½ÏÈ·¶¨·½°¸¡£)
Đ»î̀âÍøƠ¾
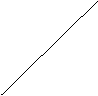
1£®(2000ÄêÉϺ£¸ß¿¼̀â)ij¿ÎÍâ»î¶¯Đ¡×é¼ÓÈÈ̀¿·Û(¹ưÁ¿)ºÍÑơ»¯ÍµÄ»́ºÏÎÔÙÓĂÏÂͼװÖĂ£¬¶Ô»ñµĂµÄÍ·Û(º¬̀¿)ÑùÆ·½øĐĐʵÑ顣ͼÖĐ̀ú¼Ǜ¨µÈ×°ÖẲÑÂÔÈ¥¡£ÇëÄă°ïÖúËûĂÇÍê³ÉÏÂÁĐʵÑ鱨¸æ¡£
|
ʵÑé¹ư³̀ |
ʵÑéÏÖÏó |
ÓĐ¹Ø»¯Ñ§·½³̀ʽ |
 ÔÚCÖĐ¼ÓÈëÑùÆ·±ê±¾W¿Ë£¬DÖĐ×°Èë̉©Æ·ºó²¢³ÆÁ¿Îªm1g¡£Á¬½ÓºẲÇÆ÷ºó£¬¼́²éÆøĂÜĐÔ ÔÚCÖĐ¼ÓÈëÑùÆ·±ê±¾W¿Ë£¬DÖĐ×°Èë̉©Æ·ºó²¢³ÆÁ¿Îªm1g¡£Á¬½ÓºẲÇÆ÷ºó£¬¼́²éÆøĂÜĐÔ |
 |
¡¡ |
|
´̣¿ªAµÄ»îÈû£¬ÂưÂưµÎ¼ÓÈÜ̉º¡£ |
¡¡ |
¡¡ |
|
¶ÔC½øĐĐ¼ÓÈÈ¡£µ±CÖĐ̉©Æ·³ä·Ö·´Ó¦ºó¡£¹Ø±ƠAµÄ»îÈû¡£Í£Ö¹¼ÓÈÈ£º |
¡¡ |
¡¡ |
 ÀäÈ´ºó£¬³ÆÁ¿DµÄÖÊÁ¿Îªm2¿Ë¡£ ÀäÈ´ºó£¬³ÆÁ¿DµÄÖÊÁ¿Îªm2¿Ë¡£ |
 |
¡¡ |
(1)ʵÑéÄ¿µÄ£º¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡£
¡¡¡¡ (2)ʵÑéÓĂÆ·£º̉ÇÆ÷£º̀́ƽ¡¢·Ö̉ºÂ©¶·¡¢×¶ĐÎÆ¿¡¢Ó²Öʲ£Á§¹Ü¡¢¸ÉÔï¹Ü¡¢¾Æ¾«µÆ¡¢Ï´ÆøÆ¿µÈ£¬̉©Æ·£ºº́ºÖÉ«Í·Û(º¬̀¿)ÑùÆ·¡¢¹ưÑơ»¯ÇâÈÜ̉º¡¢¶₫Ñơ»¯Ằ¡¢¼îʯ»̉¡¢Å¨Ạ́ËáµÈ¡£
¡¡¡¡ (3)ʵÑéÄÚÈƯ(¼û±í1)¡£
±í1¡¡ ʵÑé²½Öè¡¢ÏÖÏó¼°»¯Ñ§·½³̀ʽ£º
(4)¼ÆËă£ºÑùÆ·ÖĐ͵ÄÖÊÁ¿·ÖÊư£½_________¡£(ÓĂº¬W¡¢m1¡¢m2µÄ´úÊưʽ±íʾ¡£)
¡¡¡¡ (5)ÎỀâºÍ̀ÖÂÛ£º
ʵÑéÍê³Éºó£¬ÀÏʦÆÀ̉é˵£º°´ÉÏÊöʵÑéÉè¼Æ£¬¼´Ê¹CÖĐ·´Ó¦ÍêÈ«¡¢DÖĐÎüÊƠÍêÈ«£¬̉²²»»áµĂ³öƠưÈ·µÄ½á¹û¡£¾̀ÖÂÛ£¬ÓĐѧÉú̀á³öÔÚBÓëCÖ®¼ä¼ÓÈë̉»¸ö×°ÖĂ£¬ÔÙ´ÎʵÑéºó£¬µĂµ½Á˽ÏƠưÈ·µÄ½á¹û¡£ÄÇĂ´£¬ÔÀ´ÊµÑéËù²âµĂµÄ͵ÄÖÊÁ¿·ÖÊưÆ«Đ¡µÄỘ̉¿ÉÄÜÊÇ__________¡£ÔÚBÓëCÖ®¼ä¼ÓÈëµÄ×°ÖĂ¿É̉ÔÊÇ_____________£¬ÆäÖĐÊ¢·ÅµÄ̉©Æ·ÊÇ____________¡£
(¸ẰâÊǶỔ»¸öÏà¶ÔÍêƠûµÄʵÑé·½°¸¼Ó̉Ô·ÖÎö¡¢ÍÆÀí¡¢ÆÀ¼ÛµÄ×ÛºÏĐÔʵÑé¼̣´đ̀⣬̉âÔÚ¿¼²éѧÉúµÄ¹Û²́ÄÜÁ¦¡¢ÊµÑéÄÜÁ¦ºÍ˼άÄÜÁ¦¡£½â´đ´Ë̀âµÄ¹Ø¼üÔÚʵÑ鱨¸æµÄ̉ÇÆ÷ºÍ̉©Æ·̉»ÏÓÉ´Ë¿ÉÈ·¶¨·´Ó¦µÄ×°ÖĂºÍ·´Ó¦ÔÀí¡£)
2£®»¯Ñ§ÊµÑé·½°¸Éè¼ÆµÄ̉»°ă·½·¨
(1)Ă÷È·Ä¿µÄÔÀí
Ê×ÏȱØĐëÈÏƠæÉó̀â(Èç̉ªÇó²ÉÓĂ×î¼̣µ¥»̣×î¼ÑµÄ·½°¸£¬ÖÆÈ¡´¿¾»µÄijÎïÖʵÈ)£¬Ă÷ȷʵÑéµÄÄ¿µÄ̉ªÇó¡£ÅªÇå̀âÄ¿ÓĐÄÄЩеÄĐÅÏ¢£¬×ÛºÏ̉Ñѧ¹ưµÄ֪ʶ£¬Í¨¹ưÀà±È¡¢Ç¨̉Æ¡¢·ÖÎö£¬´Ó¶øĂ÷ȷʵÑéÔÀí¡£
(2)Ñ¡Ôñ̉ÇÆ÷̉©Æ·
¸ù¾ƯʵÑéµÄÄ¿µÄºÍÔÀí£¬̉Ô¼°·´Ó¦ÎïºÍÉú³ÉÎïµÄĐÔÖÊ¡¢·´Ó¦̀ơ¼₫£¬Èç·´Ó¦ÎïºÍÉú³ÉÎïµÄ×´̀¬¡¢ÄÜ·ñ¸¯Ê´̉ÇÆ÷ºÍÏđƤ£¬·´Ó¦ÊÇ·ñ¼ÓÈȼ°Î¶ÈÊÇ·ñ¿ØÖÆÔÚ̉»¶¨·¶Î§£¬¸ø³öµÄ̉©Æ·¡¢̉ÇÆ÷»̣×°ÖĂÊÇ·ñ×ă¹»£¬Đè̉ª²¹³ä»¹ÊÇɸѡ£¬̉ÇÆ÷̉©Æ·µÄ¹æ¸ñµÈ¡£´Ó¶øÑ¡ÔñºÏÀíµÄ»¯Ñ§̉ÇÆ÷ºÍ̉©Æ·¡£
(3)Éè¼Æ×°ÖĂ²½Öè
¸ù¾ƯÉÏÊöʵÑéÄ¿µÄºÍÔÀí£¬̉Ô¼°ËùÑ¡ÓõÄʵÑé̉ÇÆ÷ºÍ̉©Æ·£¬Éè¼Æ³öºÏÀíµÄʵÑé²Ù×÷²½Ö衢ʵÑé×°ÖĂ¡£Ñ§ÉúÓ¦¾ß±¸Ê¶±đºÍ»æÖƵäĐ͵ÄʵÑé×°ÖĂͼµÄÄÜÁ¦£¬ÊµÑé²½ÖèÓ¦ÍêƠû¶øÓÖ¼̣Ă÷¡£
(4)¼Ç¼ÏÖÏóÊư¾Ư
¸ù¾Ư¹Û²́£¬È«Ăæ׼ȷµØ¼Ç¼ʵÑé¹ư³̀ÖеÄÏÖÏóºÍÊư¾Ư¡£
(5)·ÖÎöµĂ³ö½áÂÛ
¸ù¾ƯʵÑé¹Û²́µÄÏÖÏóºÍ¼Ç¼µÄÊư¾Ư£¬Í¨¹ư·ÖÎö¡¢¼ÆËă¡¢Í¼±í¡¢ÍÆÀíµÈ´¦Àí£¬µĂ³öƠưÈ·µÄ½áÂÛ¡£
µäĐÍ̀âµă»÷
1£®»¯Ñ§ÊµÑé·½°¸Éè¼ÆµÄ»ù±¾̉ªÇó
»¯Ñ§ÊµÑé·½°¸µÄÉè¼Æ»ù±¾̉ªÇóÊÇ·½·¨¼̣±ă¡¢ÔÁÏ»̣̉©Æ·̉×µĂ¡¢ÏÖÏóĂ÷ÏÔ¡¢²Ù×÷̉×ĐĐ¡¢»·±£·ÀÎÛ¡£
6£®(1)¢Ù¢̣ ABC¡¡ ¢Ú¡¡ ̉ø°±ÈÜ̉º£»ÊÔ¹ÜÄÚ±Ú²úÉú̉ø¾µ
 CH3CHO + 2[Ag(NH3)2]+
+ 2OH-¡¡¡¡¡¡ CH3COO- + NH4+
+2Ag¡ư+ 3NH3
+2H2O
CH3CHO + 2[Ag(NH3)2]+
+ 2OH-¡¡¡¡¡¡ CH3COO- + NH4+
+2Ag¡ư+ 3NH3
+2H2O
¢Û¡¡¡¡¡¡ ˮԡ¼ÓÈÈ£¬Î¶ȼƿØÎÂ78¡æ»̣ÂÔ´óÓÚ78¡æ
(2)¢Ù¡¡ F¡¢G¡¢E·ÀÖ¹¿ƠÆøÖĐH2OºÍCO2½øÈëE£¬̉ưÆđ²â¶¨Îó²î¡¡ ¢Ú¡¡ ·ÀÖ¹¼ÓÈÈʱ²úÉúµÄË®ƠôÆøÔÚÊԹܿڲ¿·ÖÀäÄư»ØÁ÷Ö§ÊԹܵײ¿£¬̉ưÆđƠ¨ÁÑ
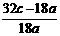
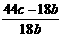 (3)¡¡¡¡¡¡¡¡
»̣
(3)¡¡¡¡¡¡¡¡
»̣
5£®(1)D(2)¼ÓÈëµÄ̉ºäåÑƠÉ«»ù±¾²»ÍÊ(3)³ưÈ¥¹ưÁ¿µÄäå(4)ËÄÇ⻯ƯÁ¡¢̀ú·Û(5)1.3
½²Îö£º±¾̀âÖ÷̉ª¿¼²é¿¼Éú¶ÔʵÑéÄ¿µÄ¡¢ÔÀíÊÇ·ñÀí½â£¬Í¬Ê±¿¼²é¿¼ÉúÄÜ·ñ×ĐϸÉó̀âºÍÀûÓẰâÄ¿ÖĐ̀ṩµÄĐÅÏ¢À´½â´đÎỀâ¡£
¡¡¡¡ °´ƠƠ²½Öè¢Ù£¬±¾ÊµÑéÊÇ°ÑËÄÇ⻯ƯÁ¡¢Ë®ºÍ̀ú·Û¼ÓÈëͬ̉»ÈƯÆ÷ÖĐ½øĐĐ·´Ó¦£¬Ëù̉ÔB²»ÊÇƠưÈ·Ñ¡Ïî¡£ÈôÓĂAÖеÄ×°ÖĂ½øĐĐ·´Ó¦£¬äåƠôÆøºÍ´̀¼¤ĐÔÆøζµÄËÄÇ⻯ƯÁ¶¼»áÎÛȾ»·¾³£¬Í¬ÑùC×°ÖĂÔÚ²½Öè¢Ú·´Ó¦Ê±£¬̉²»áỐ³É»·¾³ÎÛȾ£¬Ëù̉ÔAºÍC¶¼²»ÊÇƠưÈ·Ñ¡Ïî¡£ƠưÈ·Ñ¡ÏîÊÇD¡£¸ù¾ỪâÖĐËù̀ṩµÄĐÅÏ¢£¬ËÄä廯ƯÁÊDz»ÈÜË®µÄ¹̀̀壬ËÄÇ⻯ƯÁºÍÇâäåËáÈÜ̉º¶¼ÊÇÎ̃É«µÄ£¬·´Ó¦Íêȫʱ£¬ËÄÇ⻯ƯÁ̉Ñ»ù±¾ÏûºÄÍ꣬¼ÓÈëµÄäåÈÜÓÚË®ÖĐʹÈÜ̉º³Ê×Ø»ÆÉ«¡£ÔÚ²½Öè¢ÛÖĐ²¹³äÉÙÁ¿ËÄÇ⻯ƯÁỘÊÇΪÁ˳ưÈ¥ÈÜ̉ºÖĐ¹ưÁ¿µÄäå¡£´Ó̀âÖĐ¿ÉÖª¹ưÂ˺óµĂµ½µÄ¹̀̀åÎïÖÊÖ»ÄÜÊÇËÄä廯ƯÁºÍ×÷Ϊ´ß»¯¼ÁµÄ̀ú·Û¡£ÓÉ·´Ó¦·½³̀ʽ¿ÉÖª£¬1 molC10Hl2(132 g/mol)Óëäå·´Ó¦ºó²úÉú4molHBr(81 g/mol)£¬ÓÖÖª·´Ó¦̀ơ¼₫ϵõ½µÄÇâäåËá±¥ºÍÈÜ̉ºÖĐHBrµÄÖÊÁ¿·ÖÊưÊÇ66%£¬Ëù̉Ôº¬4molHBrµÄ±¥ºÍÈÜ̉ºÖĐË®µÄÖÊÁ¿ÊÇ(81¡Á4)¡Á34%¡Â66%£¬Ëù̉Ô²½Öè¢ÙÖĐËÄÇ⻯ƯÁºÍË®µÄÖÊÁ¿±ÈÓ¦ÊÇ£º 132£º[(81¡Á4)¡Á34%¡Â66%]=1£º1.3
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com