
题目列表(包括答案和解析)
7. (山东省聊城一中08-09高三期末综合)密度为1.45 g/cm3的硫酸中,逐渐滴入BaCl2溶液直到沉淀完全为止,测得沉淀质量与原硫酸溶液质量相等,则原硫酸溶液物质的量浓度为
( )
(山东省聊城一中08-09高三期末综合)密度为1.45 g/cm3的硫酸中,逐渐滴入BaCl2溶液直到沉淀完全为止,测得沉淀质量与原硫酸溶液质量相等,则原硫酸溶液物质的量浓度为
( )
A.6.22 mol/L B.12.22 mol/L
C.15.8 mol/L D.16.8 mol/L
6.(山东省泰安英雄山中学2009届高三年级第一次复习检测化学卷)设NA为阿伏加德罗常数,下列关于0.2mol·L-1的Ba(NO3)2溶液正确的说法是( )
A.2L溶液中有阴、阳离子总数为0.8NA
B.500mL溶液中NO3-离子浓度为0.2mol·L-1
C.500mL溶液中Ba2+离子浓度为0.2mol·L-1
D.500mL溶液中含NO3-离子总数为0.4NA
5.(常州一中2009学年度第二学期高三化学期初试卷)设NA表示阿伏加德罗常数,下列说法正确的是
A. 在含有NA个CH3COO-的醋酸溶液中, H+ 数目略大于NA
B. N60结构如右图,28gN60单质中含有的N-N键个数为NA
C. 2.9g 熟石膏(2 CaSO4·H2O)含有的结晶水分子数为0.02NA
D. 在标准状况下,2.24L的CCl4中含有C-Cl键的数目约为0.4NA
4. (山东省临沭一中2009届高三上学期期中考试)用NA表示阿伏加德罗常数,下列说法中正确的是
( )
(山东省临沭一中2009届高三上学期期中考试)用NA表示阿伏加德罗常数,下列说法中正确的是
( )
①18g D2O含有的电子数为10NA ②同温、同压下,相同体积的氟气和氩气所含的原子数相等 ③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA ④在标准状况下,22.4LSO3的物质的量为1mol ⑤4℃时5.4mL的水所含的原子总数为0.9NA ⑥0.1molOH-含0.1NA个电子 ⑦1mol Na2O2与水完全反应时转移电子数为2NA
A.③⑤⑥⑦ B.③⑤ C.①②④⑦ D.③④⑤⑥
3.(山东省宁阳二中2009届高三一轮复习月考)实验室配制1mol·L-1盐酸250mL,下列不需用的仪器是 ( )
A.250 mL容量瓶 B.托盘天平 C.胶头滴管 D.烧杯
2.(山东省宁阳二中2009届高三一轮复习月考)下列叙述正确的是 ( )
A.一定温度、压强下,气体体积由其分子的大小决定
B.一定温度、压强下,气体体积由其物质的量的多少决定
C.气体摩尔体积是指1 mol任何气体所占的体积为22.4 L
D.不同的气体,若体积不等,则它们所含的分子数一定不等
1.( 山东省实验中学2009届高三第一次诊断性测试)用NA代表阿伏加德罗常数的值,下列有关说法正确的是 ( )
A.78g过氧化钠晶体中,含2NA个阴离子
 B.常温常压下,22.4L氦气含有NA个氦原子
B.常温常压下,22.4L氦气含有NA个氦原子
C.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA
D.常温下16g O2与O3的混合气体中含氧原子数为NA
22.(福建08-09学年福州三中高三理科综合试卷)某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。
(1)该反应的离子方程式为(提示:H2C2O4的一级电离常数为5.4×10-2)
__________________________________________________________________。
(2)实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01 mol·L-1、0.001 mol·L-1,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液(0.1 mol·L-1)的用量均为2mL。如果要探究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成_______个实验进行对比即可得出结论。
(3)在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
|
KMnO4酸性溶液 的浓度 / mol·L-1 |
溶液褪色所需时间
t / min |
||
|
第1次 |
第2次 |
第3次 |
|
|
0.01 |
14 |
13 |
11 |
|
0.001 |
6 |
 7 7 |
7 |
① 计算用0.001 mol·L-1
KMnO4酸性溶液进行实验时KMnO4的平均反应速率(忽略混合前后溶液的体积变化,写出计算过程)

② 若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?____________。若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案:_________________________________________________________
[答案](1)2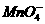 + 5H2C2O4 + 6H+
= 2Mn2+ + 10CO2↑+ 8H2O (2)4
+ 5H2C2O4 + 6H+
= 2Mn2+ + 10CO2↑+ 8H2O (2)4
(3)①
反应开始时:c(KMnO4)=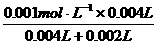 =0.00067
mol·L-1
=0.00067
mol·L-1
反应时间: =
=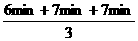 =6.7min
=6.7min
KMnO4的平均反应速率:
ν(KMnO4)=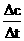 =
=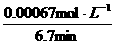 =1×10-4
mol·L-1·min-1
=1×10-4
mol·L-1·min-1
② 否(或:不可行) 取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应 高
高
21. (福建厦门双十中学09届高三第二学期开学考)某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
(福建厦门双十中学09届高三第二学期开学考)某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:


 请根据上面流程,回答以下问题:
请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 ,(填仪器名称)操作II必须用到的仪器是 。(填编号)
A.50mL烧杯 B.50mL量筒 C.100mL量筒 D.25mL滴定管
(2)请写出加入溴水发生的离子反应方程式 ,加入氨水要过量的原因是 。
(3)洗涤沉淀的操作是 ;检验沉淀是否已经洗涤干净的操作是 。
(4)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是 。
(5)若蒸发皿质量是W1 g,蒸发皿与加热后固体总质量是W2 g,则样品中铁元素的质量分数是 (列出原始算式,不需化简);若称量准确,最终测量的结果偏大,则造成误差的原因可能是 。
[答案](1)250mL容量瓶、胶头滴管 D
(2)2Fe 2+ + Br2 = 2Fe 3+ + 2Br- 使Fe3+充分沉淀
(3)往过滤器中加入蒸馏水使之稍浸没沉淀,让水自然滤下,反复操作2~3次。
取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净(合理的答案均可得分) (4)再次加热冷却并称量,直至两次质量差小于0.1g
(5)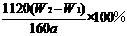 固体加热时未充分反应变为 Fe2O3
固体加热时未充分反应变为 Fe2O3
20.(漳州市芗城中学2009年5月份月模拟)
Ⅰ.短周期元素X、Y、Z、W在元素周期表中的位置如右图所示,其中X、Y、Z三种元素的质子数之和为21。
(1)氢元素与Z形成原子个数比为1∶1的化合物,其结构式为 。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是 (用离子方程式表示) ;该溶液中各种离子浓度由大到小的顺序为 。
(3)写出Y的最高价氧化物对应水化物的浓溶液与X在加热条件下反应的化学方程式
,反应中每转移8mol 电子,消耗的还原剂质量为 g
Ⅱ.为了减少CO对大气的污染,某研究性学习小组拟研究CO和H2O反应转化为绿色能源H2。已知:2CO(g)+O2(g)===2CO2(g);ΔH=-566kJ·moL-1
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6KJ·moL-1
H2O (g)===H2O(l);ΔH=-44.0KJ·moL-1
写出CO和H2O(g)作用生成CO2和H2的热化学方程式 。
Ⅲ.往1L体积不变的容器中加入0.200mol CO和1.00mol H2O(g),在t℃时反应:
CO+ H2O(g)=== CO2+ H2达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为 。
Ⅳ.H2是一种理想的绿色能源,可作燃料电池;若该氢氧燃料电池以KOH为电解质溶液,其负极的电极反应式是 。
[答案]Ⅰ.(1)H-O-O-H
(2)NH4+
+ H2O 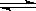 NH3·H2O + H+
NH3·H2O + H+
c (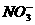 )> c (
)> c (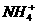 ) > c (H+) > c (
) > c (H+) > c (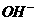 )
)
(3)C + 4HNO3(浓)△ CO2↑ + 4NO2↑ + 2H2O 24
Ⅱ.CO(g)+H2O(g)===CO2(g)+H2(g);ΔH=-41.2KJ·moL-1 (其它合理答案也可给分)
Ⅲ.83.3%
Ⅳ.H2+2OH--2e-===2H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com