
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
11°¢MnO2∫ÕZn «÷∆‘Ï∏…µÁ≥ÿµƒ÷ÿ“™‘≠¡œ£¨π§“µ…œ”√»Ì√ÃøÛ∫Õ…¡–øøÛ¡™∫œ…˙≤˙MnO2∫ÕZnµƒª˘±æ≤Ω÷ËŒ™£∫
¢≈ »Ì√ÃøÛ°¢…¡–øø۔ΡÚÀ·π≤»»£∫ MnO2+ZnS+2H2SO4£ΩMnSO4+ZnSO4+S+2H2O°£
 ¢∆ ≥˝»•∑¥”¶ªÏ∫œŒÔ÷–µƒ≤ª»ÐŒÔ
¢∆ ≥˝»•∑¥”¶ªÏ∫œŒÔ÷–µƒ≤ª»ÐŒÔ
¢« µÁΩ‚ªÏ∫œ“∫MnSO4+ZnSO4+2H2O°° MnO2+Zn+2H2SO4
œ¬¡–Àµ∑®≤ª’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
A£Æ≤Ω÷Ë¢≈÷–MnO2∫ÕH2SO4∂º «—ıªØº¡
B£Æ≤Ω÷Ë¢≈÷–√øŒˆ≥ˆ12.8g S≥¡µÌπ≤◊™“∆0.8molµÁ◊”
C£ÆµÁΩ‚ ±MnO2‘⁄—Ùº´¥¶≤˙…˙
D£Æ¡ÚÀ·‘⁄…˙≤˙÷–ø…—≠ª∑ π”√
10°¢ «‚ªØ—«Õ≠(CuH) «“ª÷÷ƒ—»ÐŒÔ÷ £¨ø…”√CuSO4»Ð“∫∫Õ°∞¡Ì“ª÷÷∑¥”¶ŒÔ°±‘⁄40°Ê-50°Ê ±∑¥”¶¿¥÷∆±∏°£CuH≤ªŒ»∂®£¨À¸º»ƒÐ”ΗŒÀ·∑¥”¶≤˙…˙∆¯Ã£¨”÷ƒÐ‘⁄¬»∆¯÷–»º…’°£“‘œ¬”–πÿÕ∆∂œ¥ÌŒÛµƒ «(°°°° )
«‚ªØ—«Õ≠(CuH) «“ª÷÷ƒ—»ÐŒÔ÷ £¨ø…”√CuSO4»Ð“∫∫Õ°∞¡Ì“ª÷÷∑¥”¶ŒÔ°±‘⁄40°Ê-50°Ê ±∑¥”¶¿¥÷∆±∏°£CuH≤ªŒ»∂®£¨À¸º»ƒÐ”ΗŒÀ·∑¥”¶≤˙…˙∆¯Ã£¨”÷ƒÐ‘⁄¬»∆¯÷–»º…’°£“‘œ¬”–πÿÕ∆∂œ¥ÌŒÛµƒ «(°°°° )
A°¢CuH‘⁄¬»∆¯÷–»º…’µƒªØ—ß∑Ω≥Ã ΩŒ™CuH+Cl2°°°°°°°° CuCl+HCl
B°¢CuHº»ø…◊ˆ—ıªØº¡“≤ø…◊ˆªπ‘≠º¡
C°¢’‚°∞¡Ì“ª÷÷∑¥”¶ŒÔ°±“ª∂®æþ”–ªπ‘≠–‘
D°¢CuH∏˙—ŒÀ·∑¥”¶ªØ—ß∑Ω≥Ã ΩŒ™2CuH+2HCl=CuCl2+2H2°¸+Cu
9°¢∑¥”¶(1)°¢(2)∑÷± «¥”∫£‘ª“∫Õ÷«¿˚œı Ø÷–÷»°µ‚µƒ÷˜“™∑¥”¶£∫
2NaI+MnO2+3H2SO4®T2NaHSO4+MnSO4+2H2O+I2°°°°°°°°°°°°°°°°°°°°°°°° (1)
2NaIO3+5NaHSO3®T2Na2SO4+3NaHSO4+H2O+I2°°°°°°°°°°°°°°°° (2)
œ¬¡–Àµ∑®’˝»∑µƒ «
A£Æ¡Ω∏ˆ∑¥”¶÷–NaHSO4æ˘Œ™—ıªØ≤˙ŒÔ
B£ÆI2‘⁄∑¥”¶(1) «ªπ‘≠≤˙ŒÔ£¨‘⁄∑¥”¶(2)÷– «—ıªØ≤˙ŒÔ
C£Æ—ıªØ–‘£∫MnO2>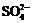 >
> >I2
>I2
D£Æ∑¥”¶(1)°¢(2)÷–…˙≥…µ»¡øµƒI2 ±◊™“∆µÁ◊” ˝±»Œ™1°√5
8°¢Ω ÙÕ≠µƒÃ·¡∂∂ý¥”ª∆Õ≠øÛø™ º°£ª∆Õ≠øÛ±∫…’π˝≥Ã÷–÷˜“™∑¥”¶÷Æ“ªµƒªØ—ß∑Ω≥Ã ΩŒ™
°°°°
 °ı
°ı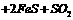 £¨œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
£¨œ¬¡–Àµ∑®≤ª’˝»∑µƒ «
°°°° A£Æ∑ΩøÚ÷–µƒŒÔ÷ ”¶Œ™Cu2S
°°°° B£ÆO2÷ª◊˜—ıªØº¡
°°°° C£ÆSO2º» «—ıªØ≤˙ŒÔ”÷ «ªπ‘≠≤˙ŒÔ
°°°° D.»Ù”–1molSO2…˙≥…£¨‘Ú∑¥”¶÷–”–4molµÁ◊”◊™“∆
7°¢¬»À· «“ª÷÷«øÀ·£¨≈®∂»≥¨π˝40% ±ª·∑¢…˙∑÷Ω‚£¨∑¥”¶ø…±Ì 挙£∫aHClO3 =bO2°¸+cCl2°¸+d HClO4 + e H2O£¨”√ ™»ÛµƒµÌ∑€µ‚ªØºÿ ‘÷ΩºÏ—È∆¯ÃÂ≤˙ŒÔ ±£¨ ‘÷Ωœ»±‰¿∂∫ÛÕ …´°£œ¬¡–Àµ∑®’˝»∑µƒ «(°°°° )
A£ÆŒÔ÷ HClO4µƒ—ıªØ–‘¥Û”⁄HClO3µƒ—ıªØ–‘
B£Æ±‰¿∂µƒµÌ∑€µ‚ªØºÿ ‘÷ΩÕ …´ø…ƒÐ «∑¢…˙£∫4C12 + I2 + 6H2O = 12H+ +8Cl£≠+2IO3£≠
C£Æ»ÙªØ—ߺ∆¡ø ˝a=8£¨b=3£¨‘Ú∏√∑¥”¶◊™“∆µÁ◊” ˝Œ™20e-
D£Æ¬»À·∑÷Ω‚À˘µ√O2∫ÕC12µƒŒÔ÷ µƒ¡ø÷Ʊ» «»∑∂®≤ª±‰µƒ
6°¢œÚ1mol≥„»»µƒCu2SÕ®»Î◊„¡øµƒÀÆ’Ù∆¯£¨≥‰∑÷∑¥”¶∫Û…˙≥…2mol H2£¨‘ÚCu2S”¶◊™ªØŒ™(°°°° )
°°°° A£ÆCu∫ÕSO2°°°°°°°°°° B£ÆCu∫ÕS°°°°°° C£ÆCuO∫ÕSO2°°°°°°°° D£ÆCu2O∫ÕS
5°¢—«¬»À·ƒ∆(NaClO2)ø…”√◊˜∆Ø∞◊º¡£¨‘⁄À·–‘»Ð“∫÷–…˙≥…HClO2∂¯∑¢…˙∑÷Ω‚£¨∑÷Ω‚µƒªØ—ß∑Ω≥Ã ΩŒ™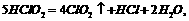
 «π„∆◊–Õœ˚∂溡°£œ¬¡–Àµ∑®’˝»∑µƒ «
«π„∆◊–Õœ˚∂溡°£œ¬¡–Àµ∑®’˝»∑µƒ «
°°°° A£ÆHClO2 «”–ª˙À·
°°°° B£Æ…œ ˆ∑¥”¶÷–£¨ClO2 «ªπ‘≠≤˙ŒÔ
°°°° C£Æ…œ ˆ∑¥”¶÷–£¨1 mol HClO2∑÷Ω‚◊™“∆2 molµÁ◊”
D£Æ…œ ˆ∑¥”¶÷–£¨—ıªØº¡”Ϊπ‘≠º¡ŒÔ÷ µƒ¡ø÷Ʊ»1°√4
4°¢Ω´SO2Õ®»ÎCuSO4∫ÕNaClµƒ≈®»Ð“∫÷–£¨»Ð“∫—’…´±‰«≥£¨Œˆ≥ˆ∞◊…´≥¡µÌ£¨»°∏√≥¡µÌ∑÷Œˆ£¨÷™∆‰÷–∫¨Cl£∫35.7%£¨Cu£∫64.3%£¨SO2‘⁄…œ ˆ∑¥”¶÷–◊˜”√ «°°°°
A£ÆÀ·°°°°°°°°°°°°°°°° B£Æ∆Ø∞◊º¡°°°°°°°°°°°°°°°° C£Æ—ıªØº¡°°°°°°°°°°°°°°°° D£Æ ªπ‘≠º¡
3°¢ƒ≥Œ¬∂»œ¬£¨Ω´C12Õ®»ÎNaOH»Ð“∫÷–£¨∑¥”¶µ√µΩNaCl°¢NaClO°¢NaC1O3µƒªÏ∫œ“∫£¨æ≠≤‚∂®C1O-”ÎC1O3-µƒŒÔ÷ µƒ¡ø≈®∂»÷Ʊ»Œ™1£∫3£¨‘ÚC12”ÎNaOH»Ð“∫∑¥”¶ ±±ªªπ‘≠µƒ¬»‘™Àÿ”αª—ıªØµƒ¬»‘™ÀÿµƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™ °°°° (°°°° )
°°°° A£Æ21£∫5°°°°°°°° B£Æ11£∫3°°°°°°°° C£Æ3£∫1°°°°°°°° D£Æ4£∫1
2°¢ƒ≥ªı≥µ”…”⁄÷∆∂Ø ß¡È≥»Î∏þÀŸπ´¬∑±þµƒ–°∫”πµƒ⁄£¨≥µ…œ◊∞‘ÿµƒªØπ§‘≠¡œ”ˆÀÆ◊≈ª»º…’£¨∏√ªØπ§‘≠¡œø…ƒÐ «
A£ÆNH4NO3°° °°°°°°°°°°°°B£ÆKClO3°°°°°°°° C£ÆCaC2°°°° °°°°°°D£ÆCaO
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com