
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
0.05 mol/LΓΓ 0.20 mol/L
ΗυΨί»ή“Κ÷–ΒΡΒγΚ… ΊΚψ
3c(Al3+)+c(K+)ΘΫ2c(SO)
c(K+)ΘΫ2ΓΝ0.20 mol/LΘ≠3ΓΝ0.05 mol/LΘΫ0.25 mol/LΓΘ
¥πΑΗΓΓB
11Θ°(2010ΓΛ¬ΠΒΉΝΣΩΦ)ΝρΥαΦ”NaOH»ή“ΚΓΔΝρΥαΦΊΓΔΟςΖ·»ΐ÷÷Έο÷ Ήι≥…ΒΡΜλΚœΈο÷–Θ§Β±SOΒΡ≈®Ε»ΈΣ0.20 mol/L ±Θ§Φ”»κΒ»ΧεΜΐΒΡ0.20 mol/LΒΡKOH»ή“Κ(ΜλΚœ»ή“ΚΧεΜΐ±δΜ·Κω¬‘≤ΜΦΤ)Θ§ Ι…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ«ΓΚΟ»ήΫβΘ§Ρ«Ο¥Ζ¥”ΠΚσ»ή“Κ÷–K+ΒΡ≈®Ε»ΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ°0.20 mol/L ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓBΘ°0.25 mol/L
CΘ°0.225 mol/L ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓDΘ°0.45 mol/L
ΫβΈωΓΓAl3+ΓΓ+ΓΓ4OHΘ≠===AlO+2H2O
ΓΓ ΓΓΓΓΓΓ1ΓΓΓΓΓΓΓΓ ΓΓ4
10Θ°(2009ΓΛΤΫΕΞ…ΫΡΘΡβ)œ¬Ν–≤ΌΉςΥυΒΟΈο÷ ΈΣ¥ΩΨΜΈοΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ°ΫΪ“ΜΩι¥χ”–―θΜ·ΡΛΒΡΦ”NaOH»ή“ΚΤ§”κΙΐΝΩΒΡ≈®NaOH»ή“ΚΆξ»ΪΖ¥”ΠΚσΘ§»Γ≥Έ«ε»ή“ΚΫΪΤδ’τΗ…Θ§ΒΟ¥ΩΨΜΒΡNaAlO2ΙΧΧε
BΘ°œρNaAlO2»ή“Κ÷–Φ”»κΙΐΝΩΒΡAlCl3»ή“ΚΘ§ΫΪΥυΒΟ≥ΝΒμΙΐ¬Υœ¥Β”Θ§Φ”»»ΉΤ…’»ΞΒτΥ°Ζ÷Θ§Ω…ΒΟ¥ΩΨΜΒΡAl(OH)3ΙΧΧε
CΘ°Α―Φ”NaOH»ή“ΚΩι”κ ΝΩΒΡœΓ―ΈΥαΆξ»ΪΖ¥”ΠΘ§ΫΪΥυΒΟ»ή“Κ’τΗ…Θ§Ω…ΒΟAlCl3ΙΧΧε
DΘ°Α―AlCl3»ή“Κ”κΉψΝΩΑ±Υ°Ζ¥”ΠΘ§ΫΪ≥ΝΒμΙΐ¬ΥΓΔœ¥Β”ΓΔΉΤ…’»ΞΒτΥ°Ζ÷Ω…ΒΟAl2O3ΙΧΧε
¥πΑΗΓΓD
9Θ°(2010ΓΛ―ο÷ίΡΘΡβ)»τ‘ΎΦ”»κΦ”NaOH»ή“ΚΖέΡήΖ≈≥ω«βΤχΒΡ»ή“Κ÷–Θ§Ζ÷±πΦ”»κœ¬Ν–ΗςΉιάκΉ”Θ§Ω…ΡήΙ≤¥φΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ°NHΓΓNOΓΓCOΓΓNa+
BΘ°Na+ΓΓBa2+ΓΓMg2+ΓΓHCO
CΘ°NOΓΓCa2+ΓΓK+ΓΓClΘ≠
DΘ°NOΓΓK+ΓΓAlOΓΓH+
¥πΑΗΓΓC
8Θ°(2010ΓΛΚΘΩΎΒς―–)œ¬Ν–”–ΙΊΫπ τΦ”NaOH»ή“ΚΦΑΤδΜ·ΚœΈοΒΡ–π ω’ΐ»ΖΒΡ «ΓΓΓΓ (ΓΓ)
AΘ°Φ”NaOH»ή“Κ‘Ύ≥ΘΈ¬œ¬≤ΜΡή”κ―θΤχΖ¥”Π
BΘ°Φ”NaOH»ή“Κ≤ΜΡޔꬻΤχΖ¥”Π
CΘ°Φ”NaOH»ή“ΚΦ»Ρή»ή”ΎΥαΘ§”÷Ρή»ή”ΎΦν
DΘ°―θΜ·Φ”NaOH»ή“Κ÷ΜΡή”κΥαΖ¥”ΠΘ§≤ΜΡή”κΦνΖ¥”Π
ΫβΈωΓΓΦ”NaOH»ή“Κ‘Ύ≥ΘΈ¬œ¬Ω…ΚΆO2Ζ¥”ΠΘ§A¥μΘΜΦ”NaOH»ή“ΚΡޔꬻΤχΖ¥”ΠΘ§B¥μΘΜ―θΜ·Φ”NaOH»ή“Κ «ΝΫ–‘―θΜ·ΈοΘ§Φ»Ρή”κΥαΖ¥”Π”÷Ρή”κΦνΖ¥”ΠΘ§D¥μΓΘ
¥πΑΗΓΓC
7Θ°(2010ΓΛΈΪΖΜΡΘΡβ)œ¬Ν–ΗςΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ÷–Θ§¥μΈσΒΡ «(ΓΓ)
AΘ°ΝρΥαΦ”NaOH»ή“Κ»ή“Κ÷–Φ”»κΙΐΝΩΒΡΑ±Υ°ΘΚAl3++3NH3ΓΛH2O===Al(OH)3Γΐ+3NH
BΘ°ΧζΤ§Ζ≈»κΙΐΝΩΒΡœΓœθΥα÷–ΘΚ3Fe+8H++2NO===3Fe2++2NO2Γϋ+4H2O
CΘ°ΫΪΦ”NaOH»ή“ΚΤ§Ζ≈»κΙΐΝΩNaOH»ή“Κ÷–ΘΚ2Al+2OHΘ≠+2H2O===2AlO+3H2Γϋ
DΘ°ΤΪΦ”NaOH»ή“ΚΥαΡΤ”κΙΐΝΩ―ΈΥαΖ¥”ΠΘΚAlO+4H+===Al3++2H2O
¥πΑΗΓΓB
6Θ°(2008ΓΛΙψΕΪΘ§6)œύΆ§÷ ΝΩΒΡœ¬Ν–Έο÷ Ζ÷±π”κΒ»≈®Ε»ΒΡNaOH»ή“ΚΖ¥”ΠΘ§÷ΝΧεœΒ÷–ΨυΈόΙΧΧεΈο÷ Θ§œϊΚΡΦνΝΩΉνΕύΒΡ «ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ°AlΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ BΘ°Al(OH)3
CΘ°AlCl3 ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓ DΘ°Al2O3
ΫβΈωΓΓΗυΨίΜ·―ßΖ¥”ΠΈο÷ ΒΡΝΩΙΊœΒΘΚAΘΚ1 mol Al-1 mol NaOHΘ§BΘΚ1 mol Al(OH)3-1 mol NaOHΘ§CΘΚ1 mol AlCl3-4 mol NaOHΘ§DΘΚ1 mol Al2O3-2 mol NaOHΓΘ»τœϊΚΡ4 mol NaOHΘ§–η“Σm(Al)ΘΫ4 molΓΝ27 g/molΘΫ108 gΘ§–η“Σm[Al(OH)3]ΘΫ78 g/molΓΝ4 molΘΫ312 gΘ§–η“Σm(AlCl3)ΘΫ1 molΓΝ133.5 g/molΘΫ133.5 gΘ§–η“Σm(Al2O3)ΘΫ2 molΓΝ102 g/molΘΫ204 gΓΘ”…“‘…œ≈–ΕœΩ…÷ΣΘ§œύΆ§÷ ΝΩ ±AlœϊΚΡNaOHΉνΕύΓΘ
¥πΑΗΓΓA
5Θ°(2009ΓΛΥΡ¥®άμΉέΘ§11)œρm gΟΨΚΆΦ”NaOH»ή“ΚΒΡΜλΚœΈο÷–Φ”»κ ΝΩΒΡœΓΝρΥαΘ§«ΓΚΟΆξ»ΪΖ¥”Π…ζ≥…±ξΉΦΉ¥Ωωœ¬ΒΡΤχΧεb LΓΘœρΖ¥”ΠΚσΒΡ»ή“Κ÷–Φ”»κc mol/L«β―θΜ·ΦΊ»ή“ΚV mLΘ§ ΙΫπ τάκΉ”Η’ΚΟ≥ΝΒμΆξ»ΪΘ§ΒΟΒΫΒΡ≥ΝΒμ÷ ΝΩΈΣn gΓΘ‘ΌΫΪΒΟΒΫΒΡ≥ΝΒμΉΤ…’÷Ν÷ ΝΩ≤Μ‘ΌΗΡ±δΈΣ÷ΙΘ§ΒΟΒΫΙΧΧεp gΓΘ‘ρœ¬Ν–ΙΊœΒ≤Μ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
AΘ°cΘΫ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓBΘ°pΘΫm+
CΘ°nΘΫm+17Vc ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓD.m<p<m
ΫβΈωΓΓœρm g MgΓΔAlΒΡΜλΚœΈο÷–Φ”»κ ΝΩΒΡœΓH2SO4Θ§«ΓΚΟΆξ»ΪΖ¥”ΠΘ§»ή“Κ÷–÷Μ”–MgSO4ΓΔAl2(SO4)3ΝΫ÷÷Έο÷ Θ§«“Mg2+”κAl3+ΒΡ÷ ΝΩΚΆΈΣm gΘΜœρΖ¥”ΠΚσΒΡ»ή“Κ÷–Φ”»κc mol/L KOH»ή“ΚV mLΘ§ ΙΫπ τάκΉ”«ΓΚΟΆξ»Ϊ≥ΝΒμΘ§ΖΔ…ζΒΡΖ¥”Π «ΘΚMg2++2OHΘ≠===Mg(OH)2ΓΐΘ§Al3++3OHΘ≠===Al(OH)3ΓΐΘ§‘ρΒΟΒΫ≥ΝΒμΒΡ÷ ΝΩ «Mg2+ΓΔAl3+ΒΡ÷ ΝΩ”κNaOH»ή“Κ÷–OHΘ≠÷ ΝΩΒΡ÷ ΝΩΚΆΘ§Υυ“‘nΘΫm+VΓΝ10Θ≠3ΓΝcΓΝ17ΘΫm+1.7ΓΝ10Θ≠2 VcΘ§Cœν¥μΈσΓΘ
¥πΑΗΓΓC
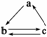
4.(2009ΓΛΫ≠Υ’Θ§3) œ¬Ν–ΥυΝ–ΗςΉιΈο÷ ÷–Θ§Έο÷ ÷°ΦδΆ®Ιΐ“Μ≤ΫΖ¥”ΠΨΆΡή Βœ÷»γΆΦΥυ ΨΉΣΜ·ΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (ΓΓ)
|
ΓΓΈο÷ ―ΓœνΓΓ |
a |
b |
c |
|
A |
Al |
AlCl3 |
Al(OH)3 |
|
B |
HNO3 |
NO |
NO2 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
CH2===CH2 |
CH3CH2OH |
CH3CHO |
 ΫβΈωΓΓA÷–ΒΡAl(OH)3ΈόΖ®Ά®Ιΐ“Μ≤ΫΖ¥”Π÷ΤΒΟAlΘ§A¥μΈσΘΜHNO3(œΓ)NOΘ§NOO2H2OΓΓ NO2Θ§NO2HNO3Θ§B’ΐ»ΖΘΜSiO2≤Μ»ή”ΎΥ°Θ§ΈόΖ®Ά®Ιΐ“Μ≤ΫΖ¥”Π÷ΤΒΟH2SiO3Θ§C¥μΈσΘΜCH3CHOΈόΖ®Ά®Ιΐ“Μ≤ΫΖ¥”Π÷ΤΒΟ““œ©Θ§D¥μΈσΓΘ
ΫβΈωΓΓA÷–ΒΡAl(OH)3ΈόΖ®Ά®Ιΐ“Μ≤ΫΖ¥”Π÷ΤΒΟAlΘ§A¥μΈσΘΜHNO3(œΓ)NOΘ§NOO2H2OΓΓ NO2Θ§NO2HNO3Θ§B’ΐ»ΖΘΜSiO2≤Μ»ή”ΎΥ°Θ§ΈόΖ®Ά®Ιΐ“Μ≤ΫΖ¥”Π÷ΤΒΟH2SiO3Θ§C¥μΈσΘΜCH3CHOΈόΖ®Ά®Ιΐ“Μ≤ΫΖ¥”Π÷ΤΒΟ““œ©Θ§D¥μΈσΓΘ
¥πΑΗΓΓB
3Θ°(2009ΓΛ…œΚΘΘ§22ΗΡ±ύ) Β―ι “ΫΪ9 gΦ”NaOH»ή“ΚΖέΗζ“ΜΕ®ΝΩΒΡΫπ τ―θΜ·ΈοΖέΡ©ΜλΚœ–Έ≥…Φ”NaOH»ή“Κ»»ΦΝΓΘΖΔ…ζΦ”NaOH»ή“Κ»»Ζ¥”Π÷°ΚσΘ§ΥυΒΟΙΧΧε÷–Κ§Ϋπ τΒΞ÷ ΈΣ18 gΘ§‘ρΗΟ―θΜ·ΈοΖέΡ©Ω…Ρή «(ΓΓ)
ΔΌFe2O3ΚΆMnO2ΓΓΓΓ ΓΓΓΓΓΓΔΎMnO2ΚΆV2O5
ΔέCr2O3ΚΆV2O5 ΓΓΓΓΓΓΓΓΔήFe3O4ΚΆFeO
AΘ°ΔΌΔήΓΓ BΘ°ΔΎΔέΓΓ CΘ°ΔΌΔέΓΓ DΘ°ΔΎΔή
ΫβΈωΓΓn(Al)ΘΫΘΫmolΘ§AlΆξ»ΪΖ¥”Π ±ΉΣ“ΤΒγΉ”ΒΡΈο÷ ΒΡΝΩΈΣmolΓΝ3ΘΫ1 molΘ§‘ρ…ζ≥…Ϋπ τΒΡΡΠΕϊΒγΉ”÷ ΝΩ(ΉΣ“Τ1 mol eΘ≠…ζ≥…Ϋπ τΒΡ÷ ΝΩ)ΈΣ18 g/molΓΘ
ΔΌœν…ζ≥…FeΒΡΡΠΕϊΒγΉ”÷ ΝΩΈΣΘΫ18.67 g/molΘ§…ζ≥…MnΒΡΡΠΕϊΒγΉ”÷ ΝΩΈΣΘΫ13.75 g/molΘ§ΗυΨίΤΫΨυ÷ΒΙφ¬…Θ§ΔΌœν’ΐ»ΖΘΜΔΎœν…ζ≥…MnΒΡΡΠΕϊΒγΉ”÷ ΝΩΈΣ13.75 g/molΘ§…ζ≥…VΒΡΡΠΕϊΒγΉ”÷ ΝΩΈΣΘΫ10.2 g/molΘ§ΗυΨίΤΫΨυ÷ΒΙφ¬…Θ§ΔΎœν≤ΜΩ…Ρή…ζ≥…ΒΞ÷ 18 gΘΜΆ§άμΘ§Δέœν“≤≤ΜΩ…Ρή…ζ≥…ΒΞ÷ 18 gΘΜΔήœνAlΆξ≥…Ζ¥”Π ±…ζ≥…FeΒΡ÷ ΝΩ¥σ”Ύ18 gΘ§Β±―θΜ·ΈοΖέΡ©≤ΜΉψΝΩ ±Θ§…ζ≥…ΒΡΫπ τΩ…ΡήΈΣ18 gΘ§Δήœν’ΐ»ΖΓΘ
¥πΑΗΓΓA
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com