
题目列表(包括答案和解析)
7.某同学实验报告中有以下数据,其中数据合理的是 ( )
A.用托盘天平称取11.7 g食盐
B.用量筒量取12.30 mL盐酸
C.用广泛pH试纸测得某溶液的pH值为3.6
D.用标准NaOH溶液滴定未知浓度的盐酸,用去21.20 mL NaOH溶液。
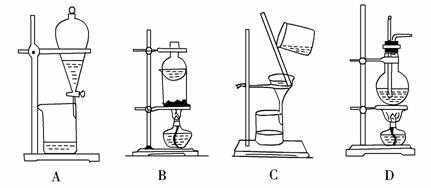
6.(2009年上海卷)下列实验装置不适用于物质分离的是 ( )
5.玻璃棒在实验中一般有如下三种用途:搅拌、引流和蘸取溶液,下列实验中至少用到其中两个作用的是( )
①配制一定物质的量浓度的溶液 ②硫酸铜晶体结晶水含量的测定 ③用硫酸铜和氢氧化钠制取氧化铜 ④从KClO3和MnO2加热制取氧气的剩余固体中提取KCl ⑤测定溶液的pH ⑥浓盐酸与浓氨水相遇发烟
A.①③④ B.②④ C.只有④ D.全部错误
4.下列试剂中需要用棕色瓶保存的是 ( )
①氨水 ②氯水 ③硝酸银 ④浓硝酸 ⑤浓硫酸
⑥磷酸
A.①②⑤ B.②③④ C.③④⑥ D.④⑤⑥
2.(2009年山东模拟)下列实验所用的试纸不能预先用蒸馏水润湿的是 ( )
A.用品红试纸检验SO2
B.用淀粉碘化钾试纸检验Cl2
C.用红色石蕊试纸检验NH3
D.用pH试纸测定某溶液的pH3.给50 mL某液体加热的操作中,所需的仪器是 ( )
①试管 ②烧杯 ③酒精灯 ④试管夹 ⑤石棉网 ?⑥泥?三角 ⑦坩埚 ⑧铁三角架
A.②③⑤⑧ B.①④⑥ C.①③⑤⑧ D.②③⑤⑥
1.下列仪器:①集气瓶 ②量筒 ③烧杯 ④表面皿 ⑤蒸发皿 ⑥容量瓶 ⑦烧瓶,能用酒精灯加热的是 ( )
A.②③⑤ B.③⑥⑦ C.①③④ D.③⑤⑦
12.(2009年文昌质检)在一定体积的0.005 mol·-1L的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的pH=11。
(1)写出所发生反应的离子方程式。
(2)若反应后溶液中由水电离产生的OH-浓度为a mol·-1L,而相同pH的Na2CO3溶液中由水电离出的OH-为b mol·-1L,则a与b的关系为:____________(填序号)。
A.a>b B.a=10-8b
C.b=10-8a D.a=b
(3)若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,求Ba(OH)2溶液与NaHSO4溶液的体积之比。
11.(2009年启东质检)在温度T ℃下,某Ba(OH)2y的稀溶液中c(H+)=10-a mol·-1L,c(OH-)=10-b mol·-1L,已知a+b=12,向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
|
序号 |
氢氧化钡的体积/mL |
盐酸的体积/mL |
溶液的pH |
|
① |
22.00 |
0.00 |
8 |
|
② |
22.00 |
18.00 |
7 |
|
③ |
22.00 |
22.00 |
6 |
(1)依据题意判断,T ℃____________25 ℃(填“大于”、“小于”或“等于”),该温度下水的离子积KW=____________。
(2)b=____________,原Ba(OH)2的稀溶液的物质的量浓度为____________。
(3)该温度下,向1 L硫酸与硫酸钠的混合溶液中加入3 L该Ba(OH)2的稀溶液时,沉淀正好达最大量,从所得溶液中取出4 mL并加水稀释至20 mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为____________,以及其中Na2SO4的物质的量浓度为____________。
10.随着溶液酸碱性的变化,酚酞分子结构发生转化而显示不同颜色:无色酚酞结构A=红色酚酞结构B。在化学实验课上,细心的某同学发现:当无色的酚酞溶液滴入到氢氧化钠溶液中时,溶液立刻变成红色,但是随后红色溶液又逐渐变成无色。对此,许多同学纷纷发表看法,主要有三种推测:
①红色酚酞结构被空气中的氧气氧化;②溶液吸收了空气中的二氧化碳,pH减小,红色褪去;③红色酚酞结构自动转化为另外一种无色酚酞结构C。为此在老师的指导下,同学们做了如下实验。分别取4 mL不同浓度的NaOH溶液于试管中,滴加2滴酚酞溶液,实验现象与数据如下表:
|
编号 |
/静置方式 |
NaOH溶液浓度 |
滴入2 滴酚酞溶液 |
加热至沸腾 |
冷却 |
再加热至沸腾 |
冷却 |
滴入适量稀盐酸 |
|
① |
敞口 |
1% |
变红, 30 min 后褪色 |
变红 |
褪色 |
变红 |
褪色/ |
变红 |
|
② |
密闭 |
1% |
变红, 29 min 后褪色 |
变红 |
褪色 |
变红 |
褪色/ |
变红 |
|
③ |
敞口 |
5% |
变红, 29 min 后褪色 |
变红 |
褪色 |
变红 |
褪色/ |
变红 |
|
④ |
密闭 |
5% |
变红, 29 min 后褪色 |
变红 |
褪色 |
变红 |
褪色/ |
变红 |
|
⑤ |
敞口 |
10% |
变红, 29 min 后褪色 |
变红 |
褪色 |
变红 |
褪色/ |
变红 |
|
⑥ |
密闭 |
10% |
变红, 29 min 后褪色 |
变红 |
褪色 |
变红 |
褪色/ |
变红 |
请回答下列问题:
(1)通过分析表中数据及现象,该组同学认为第①种推测不合理。理由是:_________ 。
(2)第②种推测也不合理。理由是____________ 。
(3)红色酚酞结构B转化为无色酚酞结构C是否为可逆反应:____________(填“是”或“否”),在各个滴入适量稀盐酸又变红的试管中加入足量稀盐酸产生的现象是____________ ____________
(4)红色酚酞结构B的热稳定性比无色酚酞结构C的热稳定性要____________(填“强”或“弱”),红色酚酞结构B转化为无色酚酞结构C是一个____________(填“吸”或“放”)热的过程。
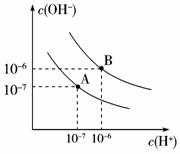
9.已知水在25 ℃和95 ℃时,其电离平衡曲线如右图所示:(1)则25 ℃时水的电离平衡曲线应为____________(填“A”或“B”),请说明理由____________
____________ 。
(2)25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,
则NaOH溶液与H2SO4溶液的体积比为______________。
(3)95 ℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是____________ 。
(4)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,
混合溶液的pH=5。请分析其原因:____________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com