
题目列表(包括答案和解析)
8.NA代表阿伏加德罗常数,下列叙述错误的是 ( )
A.一定温度下,1L 0.5mol/L NH4Cl溶液与2L 0.25mol/L NH4Cl溶液含NH4+物质的量不同
B.在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移2NA个电子
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g
D.10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8%
7、右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量
随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是
A.MgSO4 B.KAl(SO4)2 C.Al2(SO4)3 D.NaAlO2
6.某有机物结构简式为CH3CH2CH(CH3)CH2CH(CH2CH3)CH3北京四中网校下列说法不正确的是
A.该有机物属于烷烃,是甲烷的同系物
B.该烃的名称是3,5-二甲基庚烷
C.该烃与2-甲基-3-乙基己烷互为同分异构体
D.它的一氯代物只有四种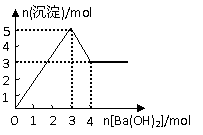
5.下列化学用语或模型图表示正确的是
A.甲烷的球棍模型: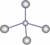 B.S2-的结构示意图为:
B.S2-的结构示意图为: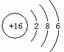
C.乙炔的最简式CH≡CH D.羟基的电子式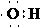
4、下列离子在强酸性溶液中能大量共存的是
A.Fe3+、Ca2+、NO3-、SCN- B.Na+、Fe2+、SO42-、Cl-
C.K+、Mg2+、Cl-、HCO3-、 D.Na+、NH4+、Cl-、SiO32-
3.下列反应中生成物总能量高于反应物总能量的是 ( )
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
2、下列各组中,两种气体的分子数一定相等的是:
A. 0.4 mol氧气和5.6 L二氧化碳 B. 体积相同、密度相同的N2和C2H4 C. 16g N2和16g O2 D. 温度相同、体积相同的O2和N2
1、下列叙述正确的是:
A.用焰色反应可以检验钠的化合物跟钾的化合物
B.钾、钠等碱金属着火时,立即用水或泡沫灭火器来灭火
C.过氧化钠与水反应生成氢氧化钠,则过氧化钠是碱性氧化物
D.钠是一种还原性很强的金属,能把铜从硫酸铜溶液中置换出来
21.(8分)将一定量的SO2和含0.7 mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550 ℃时,在催化剂作用下发生反应:2SO2+O2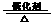 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28
L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28
L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6 L(以上气体体积均为标准状况下的体积)。(计算结果保留一位小数)
请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________。(填字母)
a.SO2和SO3浓度相等 b.SO2体积分数保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是________。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(3)求该反应达到平衡时SO3的转化率(用百分数表示)。
(4)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀多少克?
20.(10分)
已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
(1)T ℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如下表:
T ℃时物质的浓度( mol/L)变化
|
时间 / min |
CO |
H2O(g) |
CO2 |
H2 |
|
0 |
0.2 |
0.3 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
0.1 |
0.2 |
0.1 |
0.1 |
|
4 |
0.1 |
0.2 |
0.1 |
0.1 |
|
5 |
0.116 |
0.216 |
0.084 |
C1 |
|
6 |
0.096 |
0.266 |
0.104 |
C2 |
第5、6min时的数据是保持温度和体积不变时,改变某一条件后测得的。第4-5min之间,改变的条件是___________________,第5-6min之间,改变的条件是____________。T ℃时该化 学反应的平衡常数是_________________。
(2)已知420 ℃时,该化学反应的平衡常数为9。如果反应开始时,CO和H2O(g)的浓度都是0.01 mol/L,则CO在此条件下的转化率为______________。
(3)397 ℃时该反应的平衡常数为12,请判断该反应的H______0(填“>”、“=”、“<”).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com