
题目列表(包括答案和解析)
1.化学工业在经济发展中的作用举足轻重,下列有关工业生产的叙述中正确的是( )
A.硫酸生产中常采用高压条件提高SO2的转化率
B.合成氨中常采用及时分离氨气提高反应速率
C.电解精炼铜时,溶液中c(Cu2+)基本保持不变
D.铝热反应常用于冶炼某些熔点较低的金属
9、有机反应中的定量关系:
(1)烃和氯气的取代反应,被取代的H原子和被消耗的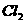 分子之间的数值关系为1:1。
分子之间的数值关系为1:1。
(2)不饱和烃分子与 、
、 、
、 等分子加成反应中,
等分子加成反应中, 、
、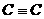 键与无机物分子的个数比关系分别为1;1、1:2。
键与无机物分子的个数比关系分别为1;1、1:2。
(3)含 的有机物与
的有机物与 的反应中,
的反应中, 与
与 分子的个数比关系为2:1。
分子的个数比关系为2:1。
(4) 与
与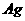 或
或 的物质的量比关系为1:2、1:1。
的物质的量比关系为1:2、1:1。
(5)醇被氧化成醛或酮的反应中,被氧化的 和消耗的
和消耗的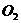 的个数比关系为2:1。
的个数比关系为2:1。
(6)酯化反应或形成肽中酯基或肽键与生成的水分子的个数比关系为1:1。
(7)1mol一元醇与足量乙酸反应生成1mol酯时,其相对分子质量将增加42,1mol二元醇与足量乙酸反应生成酯时,其相对分子质量将增加84。 (8)1mol某酯A发生水解反应生成B和乙酸时,若A与B的相对分子质量相差42,则生成1mol乙酸,若A与B的相对分子质量相差84时,则生成2mol乙酸。
[高&考%资(源#网]


8.深刻理解醇的催化氧化,卤代烃及醇的消去反应,酯化反应等重要反应类型的实质。
能够举一反三、触类旁通、联想发散。
 ⑴由乙醇的催化氧化,可推测:
⑴由乙醇的催化氧化,可推测:
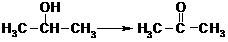
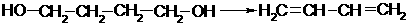 ⑵由乙醇的消去反应,可推测:
⑵由乙醇的消去反应,可推测:
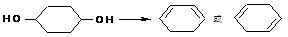
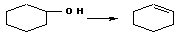
(3)由乙醇的脱水生成乙醚,可推测:略
⑷由酯化反应原理,可推测:(肽键同)

7.重要有机物间的相互转变关系。
(1) 烃的重要性质
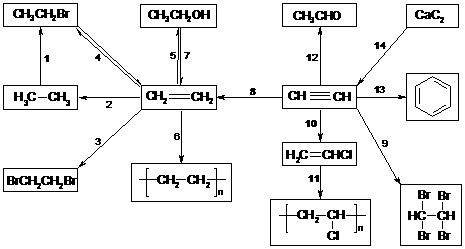
|
序号 |
反应试剂 |
反应条件 |
反应类型 |
|
1 |
Br2 |
光 |
取代 |
|
2 |
H2 |
Ni,加热 |
加成 |
|
3 |
Br2水 |
|
加成 |
|
4 |
HBr |
|
加成 |
|
5 |
H2O |
加热、加压、催化剂 |
加成 |
|
6 |
乙烯 |
催化剂 |
加聚 |
|
7 |
|
浓硫酸,170℃ |
消去 |
|
8 |
H2 |
Ni,加热 |
加成 |
|
9 |
Br2水 |
|
加成 |
|
10 |
HCl |
催化剂,加热 |
加成 |
|
11 |
|
催化剂 |
加聚 |
|
12 |
H2O |
催化剂 |
加成 |
|
13 |
|
催化剂 |
聚合 |
|
14 |
H2O(饱和食盐水) |
|
水解 |
(2) 烃的衍生物重要性质

|
序号 |
反应试剂 |
反应条件 |
反应类型 |
|
1 |
NaOH/H2O |
加热 |
水解 |
|
2 |
NaOH/醇 |
加热 |
消去 |
|
3 |
Na |
|
置换 |
|
4 |
HBr |
加热 |
取代 |
|
5 |
|
浓硫酸,170℃ |
消去 |
|
6 |
|
浓硫酸,140℃ |
取代 |
|
7 |
O2 |
Cu或Ag,加热 |
氧化 |
|
8 |
H2 |
Ni,加热 |
加成 |
|
9 |
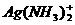 ,OH- ,OH-新制Cu(OH)2 O2 溴水或KMnO4/H+ |
水浴加热 加热 催化剂,加热 |
氧化 |
|
10 |
乙醇或乙酸 |
浓硫酸,加热 |
酯化 |
|
11 |
H2O/H+ H2O/OH- |
水浴加热 |
水解 |
(3) 芳香族化合物的重要性质
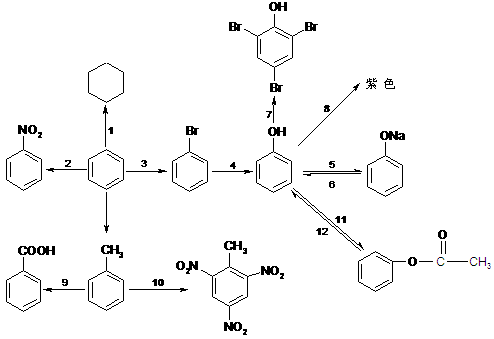
|
序号 |
反应试剂 |
反应条件 |
反应类型 |
|
1 |
H2 |
Ni,加热 |
加成 |
|
2 |
浓硝酸 |
浓硫酸,55-60℃ |
取代 |
|
3 |
液溴 |
Fe |
取代 |
|
4 |
NaOH/H2O |
催化剂,加热 |
取代 |
|
5 |
NaOH |
|
中和 |
|
6 |
CO2+H2O |
|
复分解 |
|
7 |
溴水 |
|
取代 |
|
8 |
FeCl3 |
|
显色 |
|
9 |
KMnO4/H+ |
|
氧化 |
|
10 |
浓硝酸 |
浓硫酸,加热 |
取代 |
|
11 |
(CH3CO)2O |
|
取代 |
|
12 |
H2O |
H+或OH- |
水解 |
(4) 有机反应类型
|
反应类型 |
特点 |
常见形式 |
实例 |
|
取代 |
有机分子中某些原子或原子团被其它原子或原子团所代替的反应。 |
酯化 |
羧酸与醇;酚与酸酐;无机含氧酸与醇 |
|
水解 |
卤代烃;酯;二糖与多糖;多肽与蛋白质 |
||
|
卤代 |
烷烃;芳香烃 |
||
|
硝化 |
苯及其同系物;苯酚 |
||
|
缩聚 |
酚与醛;多元羧酸与多元醇;氨基酸 |
||
|
分子间脱水 |
醇分子之间脱水形成醚 |
||
|
磺化 |
苯与浓硫酸 |
||
|
加成 |
不饱和碳原子跟其它原子或原子团直接结合。 |
加氢 |
烯烃;炔烃;苯环;醛与酮的羰基;油脂 |
|
加卤素单质 |
烯烃;炔烃; |
||
|
加卤化氢 |
烯烃;炔烃;醛与酮的羰基 |
||
|
加水 |
烯烃;炔烃 |
||
|
加聚 |
烯烃;炔烃 |
||
|
消去 |
从一个分子脱去一个小分子(如水、HX)等而生成不饱和化合物。 |
|
醇的消去 |
|
|
卤代烃消去 |
||
|
氧化 |
加氧 |
催化氧化;使酸性KMnO4褪色;银镜反应等 |
不饱和有机物;苯的同系物;醇,苯酚,含醛基有机物(醛,甲酸,甲酸某酯,葡萄糖,麦芽糖) |
|
还原 |
加氢 |
|
不饱和有机物,醛或酮,含苯环有机物 |
|
显色 |
|
|
苯酚与氯化铁:紫色;淀粉与碘水:蓝色 蛋白质与浓硝酸:黄色 |
(5) 有机物的重要性质
|
试剂 |
Na |
NaOH |
Na2CO3 |
NaHCO3 |
Br2水(Br2) |
KMnO4/H+ |
|
烷烃 |
|
×(√) |
× |
|||
|
烯烃 |
√ |
√ |
||||
|
炔烃 |
√ |
√ |
||||
 |
×(√) |
× |
||||
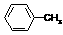 |
×(√) |
√ |
||||
|
R-Cl |
× |
√ |
× |
× |
× |
× |
|
R-OH |
√ |
× |
× |
× |
|
√ |
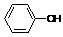 |
√ |
√ |
√ |
× |
√ |
√ |
|
R-CHO |
× |
× |
× |
× |
√ |
√ |
|
R-COOH |
√ |
√ |
√ |
√ |
× |
× |
|
RCOOR’ |
× |
√ |
× |
× |
× |
× |
(6)其它变化
① 官能团的变化;
② “碳架” 的变化(碳原子数增多、减少,成环、破环)。
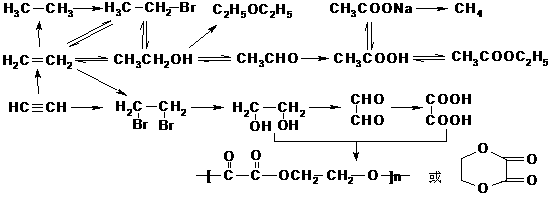

6.关注外界条件对有机反应的影响。
反应物相同,但反应条件(温度、浓度、用量、催化剂、反应介质和操作顺序)不同而导致生成物不同。
⑴温度的影响
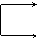 R-OH与浓H2SO4-
R-OH与浓H2SO4-
HCOOH+Cu(OH\s\do0(――→
⑵催化剂的影响


 与Br2―
(C6H10O5)n-
与Br2―
(C6H10O5)n-
⑶反应介质的影响
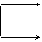 R-X与NaOH-
R-X与NaOH-
5、有机合成中的成环反应规律
a、有机成环方式一种是通过加成、聚合反应来实现的,另一种是至少含有两个相同或不同官能团的有机分子,如多元醇、羟基酸、氨基酸通过分子内或分子间脱去小分子的成环。
b 成环反应生成的环上应至少含有3个原子,其中以形五员环或六员环比较稳定。
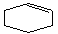 类型: <1> 加成成环
类型: <1> 加成成环
如:CH2=CHCH= CH2+CH2=CH2→
 <2> 醇分子间脱水成环
<2> 醇分子间脱水成环
CH2(OH) CH2OH→ +2H2O
 <3> 醇分子内脱水成环
<3> 醇分子内脱水成环
如:HOCH2CH2CH2CH2OH→ + H2O
<4> 醇与酸酯化成环(氨基和羧基同):
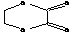 如:
如:
HOCH2CH2OH+HOOCCOOH→+2H2O
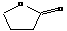 又如:
又如:
HOCH2CH2CH2CH2COOH→+H2O
4.缩短碳链:酯水解、裂化或裂解、烯催化氧化、脱羧
3.增长碳链:酯化,炔、烯加HCN,聚合等
2.消除官能团:
①消除双键方法:加成反应
②消除羟基方法:消去、氧化、酯化
③消除醛基方法:还原和氧化
2.消除官能团
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com