
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
12Θ°(2010ΓΛœεΖ° –Βς―–)ΫΪ“ΜΕ®ΝΩΒΡΟΨΚΆΆ≠Ήι≥…ΒΡΜλΚœΈοΦ”»κΒΫœΓœθΥα÷–Θ§Ϋπ τΆξ»Ϊ»ήΫβ(ΦΌ…ηΖ¥”Π÷–ΜΙ‘≠≤ζΈο÷Μ”–NO)ΓΘœρΖ¥”ΠΚσΒΡ»ή“Κ÷–Φ”»κ3 mol/L NaOH»ή“Κ÷Ν≥ΝΒμΆξ»ΪΘ§≤βΒΟ…ζ≥…≥ΝΒμΒΡ÷ ΝΩ±»‘≠ΚœΫπΒΡ÷ ΝΩ‘ωΦ”5.1 gΓΘ‘ρœ¬Ν––π ω÷–≤Μ’ΐ»ΖΒΡ «(ΓΓ)
AΘ°Β±…ζ≥…ΒΡ≥ΝΒμΝΩ¥οΒΫΉν¥σ ±Θ§œϊΚΡNaOH»ή“ΚΒΡΧεΜΐVΓί100 mL
BΘ°Β±Ϋπ τ»Ϊ≤Ω»ήΫβ ± ’Φ·ΒΫNOΤχΧεΒΡΧεΜΐ“ΜΕ®ΈΣ2.24 L
CΘ°≤ΈΦ”Ζ¥”ΠΒΡΫπ τΒΡΉή÷ ΝΩΈΣ9.6 g>m>3.6 g
DΘ°Β±Ϋπ τ»Ϊ≤Ω»ήΫβ ±Θ§≤ΈΦ”Ζ¥”ΠΒΡœθΥαΒΡΈο÷ ΒΡΝΩ“ΜΕ® «0.4 mol
ΫβΈωΘΚ≥ΝΒμ‘ωΦ”ΒΡ÷ ΝΩΈΣOHΘ≠ΒΡ÷ ΝΩΘ§‘ρn(OHΘ≠)ΘΫΘΫ0.3 molΘ§“ρ¥ΥΒ±≥ΝΒμΝΩ¥οΒΫΉν¥σ ±Θ§œϊΚΡNaOH»ή“ΚΒΡΧεΜΐΉν…ΌΈΣΘΫ0.1 LΘ§AΕ‘ΘΜΗυΨίCu(OH)2ΓΔMg(OH)2Θ§‘ρn(Cu)+n(Mg)ΘΫn(OHΘ≠)ΘΫ0.15 molΘ§ΗυΨίΒΟ ßΒγΉ” ΊΚψΘ§”–2n(Cu)+2n(Mg)ΘΫ3n(NO)Θ§‘ρn(NO)ΘΫ0.15 molΓΝ2ΓΝΘΫ0.1 molΘ§‘ρ ’Φ·ΒΫNOΒΡΧεΜΐ‘Ύ±ξΉΦΉ¥Ωωœ¬ΈΣ2.24 LΘ§B¥μΘΜΦΌ…ηΜλΚœΈο»Ϊ≤ΩΈΣMgΘ§‘ρΫπ τΉή÷ ΝΩΈΣ0.15 molΓΝ24 gΓΛmolΘ≠1ΘΫ3.6 gΘ§ΦΌ…ηΜλΚœΈο»Ϊ≤ΩΈΣCuΘ§‘ρΫπ τΉή÷ ΝΩΈΣ0.15 molΓΝ64 gΓΛmolΘ≠1ΘΫ9.6 gΘ§Ι ≤ΈΦ”Ζ¥”ΠΒΡΫπ τΒΡΉή÷ ΝΩΈΣ9.6 g>m>3.6 gΘ§CΕ‘ΘΜMgΚΆCu”κœΓœθΥαΒΡΖ¥”ΠΩ…“‘–¥ΈΣ3M+8HNO3===3M(NO3)2+2NOΓϋ+4H2OΘ§≤ΈΦ”Ζ¥”ΠΒΡn(HNO3)ΘΫ4n(NO)ΘΫ0.4 molΘ§DΕ‘ΓΘ
¥πΑΗΘΚB
11Θ°(2010ΓΛΈδΚΚ –Έδ≤ΐ«χΒς―–)ΫΪ“ΜΕ®ΝΩΒΡΆ≠ΖέΦ”»κΒΫ100 mLΡ≥≈®Ε»ΒΡœΓœθΥα÷–Θ§≥δΖ÷Ζ¥”ΠΚσΘ§»ίΤς÷– Θ”–m1gΒΡΆ≠ΖέΘ§¥Υ ±Ι≤ ’Φ·ΒΫNOΤχΧε448 mL(±ξΉΦΉ¥Ωω)ΓΘ»ΜΚσœρ…œ ωΜλΚœΈο÷–Φ”»κΉψΝΩœΓΝρΥα÷Ν≤Μ‘ΌΖ¥”ΠΈΣ÷ΙΘ§»ίΤς Θ”–Ά≠Ζέm2gΘ§‘ρ(m1Θ≠m2)ΈΣ(ΓΓ)
AΘ°5.76ΓΓ BΘ°2.88
CΘ°1.92ΓΓ DΘ°0
ΫβΈωΘΚΗυΨί3Cu+8HNO3(œΓ)ΘΫ3Cu(NO3)2+2NOΓϋ+4H2OΘ§≥δΖ÷Ζ¥”ΠΚσ»ή“Κ÷–n(NO)ΘΫ3n(NO)ΘΫΓΝ3ΘΫ0.06 molΓΘ‘ΌΦ”»κΉψΝΩœΓΝρΥαΘ§ΗυΨί3Cu+8H++2NO===3Cu2++2NOΓϋ+4H2OΘ§»ήΫβΒΡn(Cu)ΘΫn(NO)ΘΫΓΝ0.06 molΘΫ0.09 molΘ§Ι m1Θ≠m2ΘΫ64ΓΝ0.09ΘΫ5.76ΓΘ
¥πΑΗΘΚA
10Θ°(2010ΓΛΈδΚΚ –Έδ≤ΐ«χΒς―–)”“ΆΦ÷–ΚαΉχ±ξΈΣΦ”»κΖ¥”ΠΈοΒΡΈο÷ ΒΡΝΩΘ§ΉίΉχ±ξΈΣ≤ζ…ζ≥ΝΒμΒΡΈο÷ ΒΡΝΩΓΘœ¬Ν–―Γœν±ύΚ≈Ε‘”ΠΒΡ«ζœΏ±ύΚ≈¥μΈσΒΡ «(ΓΓ)
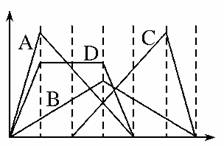
AΘ°œρNaAlO2»ή“Κ÷–÷πΒΈΦ”»κ―ΈΥα÷ΝΙΐΝΩ
BΘ°œρ≥Έ«ε ·Μ“Υ°÷–Ά®»κCO2÷ΝΙΐΝΩ
CΘ°œρΚ§”–―ΈΥαΒΡAlCl3»ή“Κ÷–ΒΈ»κNaOH»ή“Κ÷ΝΙΐΝΩ
DΘ°œρΚ§”–Β»Έο÷ ΒΡΝΩΒΡCa(OH)2ΓΔKOHΒΡΜλΚœ»ή“Κ÷–Ά®»κCO2÷ΝΙΐΝΩ
ΫβΈωΘΚΗυΨίAlO+H++H2O===Al(OH)3ΓΐΓΔAl(OH)3+3H+===Al3++3H2OΘ§AΕ‘ΘΜΗυΨίCa(OH)2+CO2===CaCO3Γΐ+H2OΓΔCaCO3+CO2+H2O===Ca(HCO3)2Θ§BΕ‘ΘΜΗυΨίH++OHΘ≠===H2OΓΔAl3++3OHΘ≠===Al(OH)3ΓΐΓΔAl(OH)3+OHΘ≠===AlO+2H2OΘ§CΕ‘ΘΜDœν÷–≤ζ…ζ≥ΝΒμΚΆ≥ΝΒμΒΡΝΩ≤Μ±δ ±œϊΚΡΒΡCO2œύΒ»Θ§D¥μΓΘ
¥πΑΗΘΚD
9Θ°(2010ΓΛΫ≠Ές ΓΝΣΩΦ)ΫΪ15.6 g Na2O2ΚΆ5.4 g AlΆ§ ±Ζ≈»κ“ΜΕ®ΝΩΒΡΥ°÷–Θ§≥δΖ÷Ζ¥”ΠΚσΒΟΒΫ200 mL»ή“ΚΘ§‘ΌœρΗΟ»ή“Κ÷–ΜΚ¬ΐΆ®»κ±ξΉΦΉ¥Ωωœ¬ΒΡHClΤχΧε6.72 LΘ§»τΖ¥”ΠΙΐ≥Χ÷–»ή“ΚΒΡΧεΜΐ±Θ≥÷≤Μ±δΘ§‘ρœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «(ΓΓ)
AΘ°Ζ¥”ΠΙΐ≥Χ÷–ΡήΒΟΒΫ6.72 LΒΡΤχΧε(±ξΉΦΉ¥Ωωœ¬)
BΘ°Ήν÷’ΒΟΒΫΒΡ»ή“Κ÷–c(Na+)ΘΫc(ClΘ≠)+c(OHΘ≠)
CΘ°Ήν÷’ΒΟΒΫ15.6 gΒΡ≥ΝΒμ
DΘ°Ήν÷’ΒΟΒΫΒΡ»ή“Κ÷–c(NaCl)ΘΫ1.5 mol/L
ΫβΈωΘΚ”…Χβ“βΩ…÷Σn(Na2O2)ΘΫ0.2 molΘ§n(Al)ΘΫ0.2 molΘ§ΖΔ…ζΖ¥”ΠΘΚ2Na2O2+2H2O===4NaOH+O2ΓϋΘ§2Al+2NaOH+2H2O===2NaAlO2+3H2ΓϋΘ§Ω…÷Σ…ζ≥…ΤχΧε0.4 molΘ§±ξΉΦΉ¥Ωωœ¬ΧεΜΐΈΣ8.96 LΘΜΆ®»κΒΡHClΤχΧεœ»ΚΆΙΐΝΩΒΡNaOHΖ¥”ΠΘ§ Θ”ύ0.1 mol HClΚΆNaAlO2Ζ¥”Π…ζ≥…0.1 mol Al(OH)3ΘΚNaAlO2+HCl+H2O===NaCl+Al(OH)3ΓΐΘ§ΒΟΒΫ≥ΝΒμΒΡ÷ ΝΩΈΣ7.8 gΘ§Ήν÷’»ή“Κ÷–Κ§”–0.3 mol NaClΓΔ0.1 mol NaAlO2Θ§Ι AΓΔBΓΔC¥μΈσΓΘ
¥πΑΗΘΚD
8Θ°(2010ΓΛ ·Φ“Ή·÷ Φλ(“Μ))œ¬Ν–ΆΦœσ±μ ΨAl3+”κAlOΈο÷ ΒΡΝΩ±δΜ·ΒΡ«ζœΏΘ§ ΒœΏ±μ ΨAl3+Θ§–ιœΏ±μ ΨAlOΘ§Τδ÷–’ΐ»ΖΒΡ «(ΓΓ)

ΫβΈωΘΚΗυΨίΖ¥”ΠAl3++3OHΘ≠===Al(OH)3ΓΐΚΆAl(OH)3+OHΘ≠===AlO+2H2O÷–œϊΚΡOHΘ≠ΒΡΙΊœΒΩ…÷ΣΆΦœσB’ΐ»ΖΘΜ”…AlO+H++H2O===Al(OH)3ΚΆAl(OH)3+3H+===Al3++3H2O÷ΣCΓΔD¥μΓΘ
¥πΑΗΘΚB
7Θ°(2010ΓΛΥΡ¥® ΓΦλ≤β)ΫΪ4 molΫπ τAl»Ϊ≤ΩΉΣΜ·ΈΣAl(OH)3Θ§Ι≤ΦΤœϊΚΡHCl a molΘ§NaOH b molΘ§‘ρ(a+b)ΒΡΉν–Γ÷ΒΈΣ(ΓΓ)
AΘ°4ΓΓ BΘ°6
CΘ°8ΓΓ DΘ°16
ΫβΈωΘΚ”…¬Ν÷Τ«β―θΜ·¬Ν ±Ήν Γ‘≠ΝœΒΡΖΫΑΗ «άϊ”ΟΥΪΥ°ΫβΘΚAlCl3+3NaAlO2+6H2O===3NaCl+4Al(OH)3ΓΐΘ§”…‘≠Ή” ΊΚψ÷ΣΘ§άϊ”Ο¬Ν÷Τ±Η4 mol Al(OH)3–η“Σ3 mol HClΚΆ3 mol NaOHΓΘ
¥πΑΗΘΚB
6Θ°(2010ΓΛ±±Ψ© –ΕΪ≥««χΦλ≤β)–Ω”κ100 mL 18.5 molΓΛLΘ≠1ΒΡ≈®ΝρΥα≥δΖ÷Ζ¥”ΠΚσΘ§–ΩΆξ»Ϊ»ήΫβΘ§Ά§ ±…ζ≥…ΤχΧεΦΉ33.6 L(±ξΉΦΉ¥Ωω)ΓΘΫΪΖ¥”ΠΚσΒΡ»ή“ΚœΓ Ά÷Ν1 LΘ§≤βΒΟ»ή“ΚΒΡpHΘΫ1Θ§œ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «(ΓΓ)
AΘ°Ζ¥”Π÷–Ι≤œϊΚΡ1.8 mol H2SO4
BΘ°ΤχΧεΦΉ÷–SO2”κH2ΒΡΧεΜΐ±»ΈΣ4?1
CΘ°Ζ¥”Π÷–Ι≤œϊΚΡ97.5 g Zn
DΘ°Ζ¥”Π÷–Ι≤ΉΣ“Τ3 molΒγΉ”
ΫβΈωΘΚΖ¥”Π«Αn(H2SO4)ΘΫ1.85 molΘ§Ζ¥”ΠΚσ Θ”ύH2SO4ΈΣ0.05 molΘ§ΆΤ÷ΣΤχΧεΦΉ”ΠΗΟ «Zn”κ≈®H2SO4Ζ¥”Π≤ζ…ζΒΡSO2ΦΑZn”κœΓH2SO4Ζ¥”Π≤ζ…ζΒΡH2ΒΡΜλΚœΤχΧεΓΘ…η…ζ≥…SO2ΓΔH2ΒΡΈο÷ ΒΡΝΩΖ÷±πΈΣx molΓΔy molΘ§‘ρ”–ΘΚx+yΘΫ1.5Θ§ΗυΨίΖ¥”ΠΘΚZn+2H2SO4(≈®)===ZnSO4+SO2Γϋ+2H2OΘ§Zn+H2SO4(œΓ)===ZnSO4+H2ΓϋΘ§ΒΟ2x+yΘΫ1.8Θ§ΫβΒΟxΘΫ0.3Θ§yΘΫ1.2ΓΘn(SO2)/n(H2)ΘΫ0.3 mol/1.2 molΘΫ1/4ΓΘΖ¥”Π÷–œϊΚΡZnΒΡ÷ ΝΩΘΫ1.5 molΓΝ65 g/molΘΫ97.5 gΓΘΖ¥”Π÷–ΉΣ“ΤΒγΉ”ΒΡΈο÷ ΒΡΝΩΘΫ2ΓΝ1.5 molΘΫ3 molΓΘΉέΚœ…œ ω÷Σ―ΓœνB¥μΈσΓΘ
¥πΑΗΘΚB
5Θ°(2010ΓΛΚΰ±± ΓΑΥ–ΘΝΣΩΦ)CO2”κH2ΒΡΜλΚœΤχΧε5 gΘ§‘Ύ150Γφ ±ΚΆΉψΝΩΒΡ―θΤχΜλΚœΘ§”ΟΒγΜπΜ®≥δΖ÷“ΐ»ΦΘ§‘ΎœύΆ§Ή¥Ωωœ¬‘ΌΫΪΖ¥”ΠΚσΥυΒΟΜλΚœΤχΧεΆ®»κΒΫΉψΝΩΒΡNa2O2÷–Θ§≤βΒΟNa2O2ΙΧΧε‘ω÷ΊΒΡ÷ ΝΩΈΣ3.4 gΘ§‘ρ‘≠ΜλΚœΤχΧε÷–CO2ΒΡΈο÷ ΒΡΝΩΖ÷ ΐΈΣ(ΓΓ)
AΘ°25%ΓΓ BΘ°75%
CΘ°88%ΓΓ DΘ°32%
ΫβΈωΘΚΗυΨίΖ¥”ΠΘΚ2CO2+2Na2O2===2Na2CO3+O2ΔΌΘΜ2H2+O22H2OΔΎΘΜ2H2O+2Na2O2===4NaOH+O2ΔέΘ§”…ΔΎ+Δέ‘ρ”–ΘΚ2Na2O2+2H2===4NaOHΔήΓΘ…ηCO2ΈΣx molΘ§‘ρΤδ÷ ΝΩΈΣ44x gΘ§H2ΒΡ÷ ΝΩΘΫ(5Θ≠44x)gΘ§ΗυΨί≤ν÷ΒΖ®Θ§Ζ¥”ΠΔΌ‘ω÷Ί28x gΘ§Ζ¥”ΠΔή‘ω÷Ί(5Θ≠44x)gΘ§‘ρ”–ΘΚ5Θ≠44x+28xΘΫ3.4Θ§ΫβΒΟxΘΫ0.1Θ§Ι CO2÷ ΝΩΈΣ4.4 gΘ§ΤδΈο÷ ΒΡΝΩΖ÷ ΐΘΫΓΝ100%ΘΫ25%ΓΘ
¥πΑΗΘΚA
4Θ°(2010ΓΛΗ”÷ί –÷ Φλ)œ¬Ν–ΗςΉι÷–ΝΫ÷÷≈®»ή“ΚœύΜλΚœ ±Φ»Έό≥ΝΒμΈω≥ω”÷ΈόΤχΧεΖ≈≥ωΒΡ «(ΓΓ)
AΘ°Ba(HCO3)2ΓΔNaHSO4ΓΓ BΘ°NaHCO3ΓΔAl2(SO4)3
CΘ°Mg(HCO3)2ΓΔCaCl2ΓΓ DΘ°Na2SiO3ΓΔHCl
ΫβΈωΘΚAœν÷–Ζ¥”ΠΈΣBa(HCO3)2+2NaHSO4===Na2SO4+BaSO4Γΐ+2H2O+2CO2ΓϋΘ§Φ»”–≥ΝΒμ≤ζ…ζΘ§”÷”–ΤχΧεΖ≈≥ωΘΜBœν÷–Ζ¥”ΠΈΣAl3++3HCO===Al(OH)3Γΐ+3CO2ΓϋΘ§Φ»”–≥ΝΒμ≤ζ…ζΘ§”÷”–ΤχΧεΖ≈≥ωΘΜDœν÷–SiO+2H+===H2SiO3ΓΐΘ§”–≥ΝΒμ≤ζ…ζΓΘ
¥πΑΗΘΚC
3Θ°(2010ΓΛΫ≠Ές ΓΝΣΩΦ)ΫΪΒ»ΧεΜΐΓΔΒ»pHΒΡNaOH»ή“ΚΚΆΑ±Υ°Θ§Ζ÷±π»Ϊ≤ΩΦ”»κΒΫΦΉΓΔ““…’±≠÷–ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «(ΓΓ)
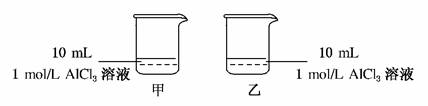
AΘ°ΦΉ÷–≥ΝΒμ“ΜΕ®±»““Εύ
BΘ°““÷–≥ΝΒμ“ΜΕ®±»ΦΉΕύ
CΘ°ΦΉ÷–≥ΝΒμΩ…Ρή±»““Εύ
DΘ°ΦΉΚΆ““÷–≥ΝΒμΩ…Ρή“Μ―υΕύ
ΫβΈωΘΚNaOH»ή“ΚΩ…“‘»ήΫβAl(OH)3Θ§ΕχNH3ΓΛH2O≤ΜΡή»ήΫβAl(OH)3ΓΘΒ»ΧεΜΐΓΔΒ»pHΒΡNaOH»ή“ΚΚΆΑ±Υ°Θ§œ‘»Μn(NH3ΓΛH2O)>n(NaOH)Θ§Β±n(NaOH)Γή3n(Al3+) ±Θ§ΦΉΚΆ““÷–≥ΝΒμ“Μ―υΕύΘΜΒ±n(NaOH)>3n(Al3+) ±Θ§ΦΉ÷–≥ΝΒμ±»““…ΌΘΜ≤ΜΩ…Ρή≥ωœ÷ΦΉ÷–≥ΝΒμ±»““ΕύΒΡ«ιΩωΓΘ
¥πΑΗΘΚD
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com