
请回答:
20.(10分)有三种常见短周期元素 ,它们的原子序数依次增大。
,它们的原子序数依次增大。 元素原子最外层电子数比
元素原子最外层电子数比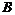 元素原子最外层电子数多1个,
元素原子最外层电子数多1个,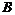 元素原子最外层电子数是
元素原子最外层电子数是 元素原子最外层电子数的一半。甲是
元素原子最外层电子数的一半。甲是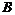 元素含氧酸的钠盐;乙是
元素含氧酸的钠盐;乙是 元素最高价含氧酸的酸式钠盐;丙是
元素最高价含氧酸的酸式钠盐;丙是 元素含氧酸的钠盐(正盐)。甲.丙溶液
元素含氧酸的钠盐(正盐)。甲.丙溶液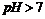 ,乙溶液
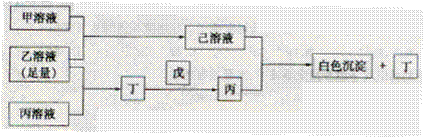
,乙溶液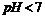 。丁为无色.无味的气体,戊为淡黄色固体,丁与戊的反应是呼吸面具中发生的主要反应。甲.乙.丙.丁.戊.已六种物质之间相互反应关系如下(与变化无关的产物已略去);
。丁为无色.无味的气体,戊为淡黄色固体,丁与戊的反应是呼吸面具中发生的主要反应。甲.乙.丙.丁.戊.已六种物质之间相互反应关系如下(与变化无关的产物已略去);
(5) 以原子数比4 : 2 : 3所形成的化合物,晶体类型为_____________。
以原子数比4 : 2 : 3所形成的化合物,晶体类型为_____________。
(4)已知0.5mol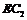 被
被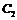 氧化成气态
氧化成气态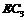 ,放出49.15KJ热量,其热化学方程式为____________。
,放出49.15KJ热量,其热化学方程式为____________。
(3) 形成的化合物分子中,各原子达8电子结构,则该分子的电子式为___________。
形成的化合物分子中,各原子达8电子结构,则该分子的电子式为___________。
(2)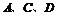 三种元素可组成一种常见化合物,该化合物的化学式为________________,生产该化合物和单质
三种元素可组成一种常见化合物,该化合物的化学式为________________,生产该化合物和单质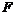 的的工业称为_____________工业。
的的工业称为_____________工业。
(1)元素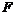 在周期表中位置________________。
在周期表中位置________________。
19.(8分)现有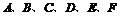 六种短周期元素,原子序数依次增大,已知
六种短周期元素,原子序数依次增大,已知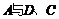 与
与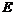 分别同主族,
分别同主族,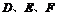 同周期;
同周期;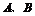 的最外层电子数之和与
的最外层电子数之和与 的最外层电子数相等,
的最外层电子数相等,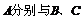 形成电子总数相等的分子甲和乙,且
形成电子总数相等的分子甲和乙,且 形成的化合物常温下均为液态,
形成的化合物常温下均为液态, 分别与
分别与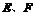 形成电子数相等的气体分子丙和丁。
形成电子数相等的气体分子丙和丁。
请回答下列问题:
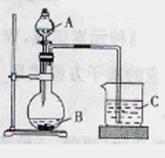
(1)甲同学设计实验的目的是_______________________,反应最剧烈的烧杯是_______(填序号)。
(2)乙同学设计的实验可证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状 固体;打开分液漏斗的活塞后,C中可观察到白色沉淀生成。
①写出所选用物质的化学式:
A_______,B______,C_________.
②写出烧杯中发生反应的离子方程式:____________________________。
Ⅰ.甲同学在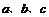 三只烧杯里分别加入50mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂.钠.钾块,观察现象。
三只烧杯里分别加入50mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂.钠.钾块,观察现象。
Ⅱ.乙同学设计实验验证:非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。他设计了下图装置:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com