
23£®(14·Ö)
I£®Ä³Í¬Ñ§Óû²â¶¨Ạ́Ëá;§̀åÖĐ½á¾§Ë®µÄº¬Á¿¡£ËûÁĐ³öµÄʵÑéÓĂƷΪ£ºẠ́Ëá;§̀åÊÔÑù¡¢ÑĐ²§¡¢ÛáÛö¡¢ÛáÛöǯ¡¢¾Æ¾«µÆ¡¢Èư½Å¼Ü¡¢²£Á§°ô¡¢̉©³×¡¢ÍĐÅ̀̀́ƽ¡£¡¡ »Ø´đÏÂĂæÎỀ⣺
(1)Íê³É±¾ÊµÑ黹Đè̉ªµÄʵÑéÓĂÆ·ÓĐ¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)ÏÂĂæµÄÇé¿öÓĐ¿ÉÄÜỐ³É²â¶¨½á¹ûÆ«µÍµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡(̀îĐ̣ºÅ)¡£
¡¡¡¡ A£®ÊÔÑùÖĐº¬ÓĐ̉×»Ó·¢µÄÔÓÖÊ¡¡¡¡ B£®¼ÓÈÈʱÓĐ¾§̀彦³ö¡¡¡¡ ¡¯
¡¡¡¡ C£®¾§̀å¼ÓÈÈÍÑË®²»ÍêÈ«¡¡¡¡ D£®ÊµÑéÇ°ÛáÛöδÍêÈ«¸ÉÔï¡¡ E£®Ạ́ËáÍÊÜÈÈ·Ö½â
¢̣£®¸Ăͬѧ·¢ÏÖẠ́Ëá;§̀å¼ÓÈȺó±äºÚ£¬²éÔÄ×ÊÁϵĂÖª£ºẠ́ËáÍÔÚ¼ÓÈÈ̀ơ¼₫ÏÂÉú³ÉCuO¡¢SO2¡¢O2¡¢SO3¡£ÏÖÓĂÏÂͼËùʾµÄ×°ÖĂÑéÖ¤Ạ́ËáÍÔÚ¼ÓÈÈ·Ö½âʱÓĐSO2²úÉú£¬²¢²âÁ¿²úÉúµÄ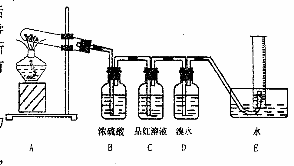 O2µÄ̀å»ư¡£
O2µÄ̀å»ư¡£
¡¡ÊỒîĐ´ÏÂÁĐ¿Ơ°×£º
(1)Ạ́ËáÍÊÜÈÈ·Ö½âµÄ»¯Ñ§·½³̀ʽ¡¡¡¡ Ϊ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡£
(2)×°ÖĂBµÄ×÷ÓĂÊÇ¡¡¡¡¡¡¡¡ £¬
¡¡(3)Í£Ö¹¼ÓÈÈʱ£¬²âÁ¿ÊƠ¼¯µ½µÄÆø̀å̀å»ư±ØĐë°üÀ¨̉Ôϼ¸²½£º
¢Ù¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»¡¡¡¡ ¢Úµ÷ƠûÁ¿Í²ÄÚÍẩºĂæ¸ß¶Èʹ֮Ïàͬ£»
¢Û¶ÁÈ¡Á¿Í²ÄÚÆø̀åµÄ̀å»ư¡£
¡¡(4)YΪ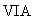 ×åÔªËع¹³ÉµÄÆø̀¬µ¥ÖÊ£¬½«YºÍSO2·Ö±đͨÈËÆ·º́ÈÜ̉º£¬¶¼ÄÜʹƷº́ÈÜ̉ºÍÊÉ«¡£ỘYµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡
£»¼̣ÊöÇø±đ¶₫ƠßµÄʵÑé·½·¨¡¡¡¡¡¡¡¡¡¡¡¡
¡£
×åÔªËع¹³ÉµÄÆø̀¬µ¥ÖÊ£¬½«YºÍSO2·Ö±đͨÈËÆ·º́ÈÜ̉º£¬¶¼ÄÜʹƷº́ÈÜ̉ºÍÊÉ«¡£ỘYµÄ»¯Ñ§Ê½Îª¡¡¡¡¡¡¡¡¡¡¡¡
£»¼̣ÊöÇø±đ¶₫ƠßµÄʵÑé·½·¨¡¡¡¡¡¡¡¡¡¡¡¡
¡£
22¡¢(12·Ö)̉ÑÖªÎïÖÊMÓÉͬ̉»¶̀ÖÜÆÚµÄX¡¢YÁ½ÖÖÔªËØ×é³É£¬XÔ×ÓµÄ×îÍâ²ăµç×ÓÊưÊÇ×îÄÚ²ăµç×ÓÊưµÄ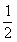 £¬YÔªËØ×î¸ßƠư¼ÛÓëËüµÄ¸º¼Û´úÊưºÍΪ6¡£MÓëÆäËüÎïÖʵÄת»¯¹ØϵÈçÏÂ(²¿·Ö²úÎï̉ÑÂÔÈ¥)£º
£¬YÔªËØ×î¸ßƠư¼ÛÓëËüµÄ¸º¼Û´úÊưºÍΪ6¡£MÓëÆäËüÎïÖʵÄת»¯¹ØϵÈçÏÂ(²¿·Ö²úÎï̉ÑÂÔÈ¥)£º
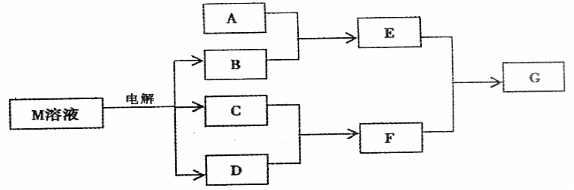 ¡¡ (1)ÈôAÊÇÓëX¡¢YͬÖÜÆÚµÄ̉»ÖÖ³£¼û½đÊôµ¥ÖÊ£¬ỘAÓëBÈÜ̉º·´Ó¦µÄ»¯Ñ§·½³̀ʽÊÇ£º¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£»
¡¡ (1)ÈôAÊÇÓëX¡¢YͬÖÜÆÚµÄ̉»ÖÖ³£¼û½đÊôµ¥ÖÊ£¬ỘAÓëBÈÜ̉º·´Ó¦µÄ»¯Ñ§·½³̀ʽÊÇ£º¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£»
¡¡ (2)ÈôAÊÇ̉»ÖÖ³£¼ûËáĐÔÑơ»¯ÎÇ̉¿ÉÓĂÓÚÖÆỐ²£Á§£¬ỘEÓëF·´Ó¦µÄÀë×Ó·½³̀ʽÊÇ£º¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ £»
(3)ÈôAÊÇ̉»ÖÖ³£¼ûµÄ»¯·Ê£¬Ê½Á¿Îª79£¬Ç̉EºÍFÉú³ÉGʱÓĐ°×Ñ̀Éú³É£¬ỘAºÍ×ăÁ¿B·´Ó¦µÄÀë×Ó·½³̀ʽ___________________________£¬GµÄµç×Óʽ_______
21£®(14·Ö)ÔªËØÖÜÆÚ±í½̉ʾÁËĐí¶àÔªËصÄÏàËÆĐԺ͵Ư±ä¹æÂÉ¡£Í¬̉»ÖÜÆÚ¹¹³ÉµÄÄ³Đ©Î¢Á£ÍùÍù¾ßÓĐÏàͬµÄµç×ÓÊư£¬ÈçÖÜÆÚ±íÖĐÖ÷×åÔªËØ¿É̉Ô¹¹³ÉĐí¶àµç×ÓÊưΪ10»̣18µÄ΢Á£¡£ÏÂÁĐÖÜÆÚ±íÖĐÁĐ³ö̉»Đ©¾ùÓë¶ÔÓ¦ÔªËØÓĐ¹ØµÄ18µç×Ó΢Á£¡£
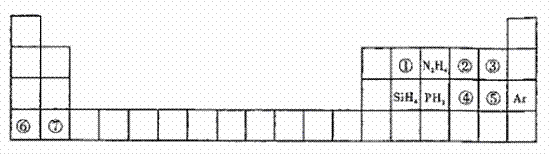
(1)¢ÙΪ8ºË΢Á££¬ÆäĂû³ÆΪ_________£»¢ÚµÄµç×Óʽ____________£¬PH3µÄ¿Ơ¼ä¹¹ĐÍΪ______¡¡
(2)¢Ü¢Ư¢̃¢ß¶ÔÓ¦ÔªËØĐγɵļ̣µ¥Àë×Ӱ뾶´ÓĐ¡µ½´óµÄ˳Đ̣Ϊ__________________(ÓĂÀë×Ó·ûºÅ±íʾ)¡£
(3)Đ´³ö¢Û²Î¼ÓµÄÖĂ»»·´Ó¦µÄ»¯Ñ§·½³̀ʽ___________________¡£
(4)¢Ü¶ÔÓ¦µÄijÖÖ18µç×ÓµÄÀë×ÓÓë ºÍ
ºÍ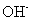 ¾ù¿É·¢Éú·´Ó¦£¬Đ´³öÆäÓëOH-·´Ó¦µÄÀë×Ó·½³̀ʽ:_____________________________
¾ù¿É·¢Éú·´Ó¦£¬Đ´³öÆäÓëOH-·´Ó¦µÄÀë×Ó·½³̀ʽ:_____________________________
(5)ÔÚ»đ¼ưÍƽøÆ÷ÖĐ×°ÓĐ̉º̀¬N2H4ºÍ̉º̀¬¢Ú£¬̉ÑÖª0.4mol̉º̀¬N2H4ºÍ×ăÁ¿̉º̀¬¢Ú·´Ó¦£¬Éú³É̉»ÖÖÆø̀¬µ¥ÖʺÍÆø̀¬Ç⻯Î·Å³ö256.6kJµÄÈÈÁ¿£¬Ộ¸Ă·´Ó¦µÄÈÈ»¯Ñ§·½³̀ʽΪ________________________________________¡£
20£®ÏơËáÓë½đÊô·´Ó¦Ê±£¬»¹Ô²úÎï¿ÉÄÜÊÇNO2¡¢NO¡¢N2O¡¢N2»̣NH4+ÖеÄ̉»ÖÖ»̣¼¸ÖÖ¡£ÏÖÓĐ̉»¶¨Á¿µÄAl·ÛºÍFe·ÛµÄ»́ºÏÎïÓë100mLÏ¡ÏơËá³ä·Ö·´Ó¦£¬·´Ó¦¹ư³̀ÖĐÎ̃ÈκÎÆø̀å·Å³ö¡£ÔÚ·´Ó¦½áÊøºóµÄÈÜ̉ºÖĐÖđµÎ¼ÓÈë4mol/LµÄNaOHÈÜ̉º£¬¼ÓÈëNaOHÈÜ̉ºµÄ̀å»ưÓë²úÉú³ÁµíµÄÎïÖÊ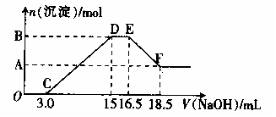 µÄÁ¿µÄ¹ØϵÈçÏÂͼ£¬ỘÏÂÁĐ˵·¨ÖĐ²»ƠưÈ·µÄÊÇ(¡¡¡¡ )
µÄÁ¿µÄ¹ØϵÈçÏÂͼ£¬ỘÏÂÁĐ˵·¨ÖĐ²»ƠưÈ·µÄÊÇ(¡¡¡¡ )
A.ÓëHNO3·´Ó¦ºó£¬FeÔªËصĻ¯ºÏ¼ÛΪ+3
B.D¡úE¶Î·´Ó¦µÄÀë×Ó·½³̀ʽΪ
NH4++OH-=NH3¡¤H2O
C.×Ư×ø±êAµăÊưֵΪ0.008
D£®×Ư×ø±êBµăÊưֵΪ0.012
µÚ¢̣¾í
19£®X¡¢Y¡¢Z¡¢WËÄÖÖÖ÷×åÔªËؾùÔÚ¶̀ÖÜÆÚ£¬Ç̉Ô×ÓĐ̣ÊửÀ´ÎÔö´ó¡£̉ÑÖªX¡¢ZÁ½ÔªËØÔ×ÓµÄ×îÍâ²ăµç×ÓÊư¾ùΪÆäµç×Ó²ăÊưµÄ2±¶£»Y¡¢WµÄ×îÍâ²ăµç×ÓÊưÏàͬ¡£ÏÂÁĐ˵·¨ÖĐƠưÈ·µÄÊÇ(¡¡¡¡ )A£®X¡¢ZÁ½ÔªËصÄÇ⻯Îï·Ö×ÓÖĐ¾ùº¬4¶Ô¹²Óõç×Ó¶Ô¡¡¡¡
B£®Y¡¢Z¡¢W¾ù¿É·Ö±đÓëXĐγɷǼ«ĐÔ·Ö×Ó
¡¡¡¡ C£®YµÄÇ⻯Îï·Đµă±ÈWµÄÇ⻯Îï·ĐµăµÍ
D£®YµÄµ¥ÖÊ¿ÉÓëÀäË®·´Ó¦²¢ÖĂ»»³ö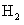
18£®ÏÂÁĐʵÑé²Ù×÷ÖĐ£¬ƠưÈ·µÄÊÇ
¢Ù׼ȷ³ÆÈ¡4.0gµÄNaOH¹̀̀åÈÜÓÚ1LË®Åä³ÉŨ¶ÈΪ1.0 mol¡¤L-1µÄÈÜ̉º¡¡¡¡¡¡¡¡¡¡¡¡
¢ÚÓĂ10 mL Á¿Í²Á¿È¡5.2mLÑÎËá
¢ÛÓĂƠô·¢Ăó¼ÓÈÈNaClÈÜ̉º¿É̉Եõ½NaCl¾§̀å
¢ÜÓĂ100 mLÈƯÁ¿Æ¿Ï¡ÊÍ18mol•L-1Ũ H2SO4ÈÜ̉º
¢ƯÓĂ´ø²£Á§ÈûµÄ×ØÉ«ÊÔ¼ÁÆ¿´æ·ÅŨHNO3
¢̃ÖĐºÍÈȲⶨµÄʵÑéÖĐʹÓĂµÄ²£Á§̉ÇÆ÷Ö»ÓĐ2ÖÖ
¢ß½«̉»Đ¡¿épHÊÔÖ½ÓĂƠôÁóË®Èóʪºó·ÅÔÚ±íĂæĂóÉÏ£¬ÓĂ²£Á§°ôƠºÈ¡ÉÙÁ¿´ư²ẩºµăÔÚÊÔÖ½
ÉÏ£¬ÔÙÓë±ê×¼±ÈÉ«¿¨¶ÔƠƠ
A£®¢Ú¢Ü¢ß¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®¢Ú¢Ư¢̃
C£®¢Ú¢Û¢Ư¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®¢Ù¢Ú¢Û
17£®.Cu2OÊÇ̉»ÖÖ°ëµ¼̀å²ÄÁÏ£¬»ùÓÚẦÉ«»¯Ñ§ÀíÄîÉè¼ÆµÄÖÆÈ¡.Cu2OµÄµç½â³Øʾ̉âͼÈçÏ£¬µă½â×Ü·´Ó¦£º2Cu+H2O==Cu2O+H2O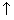 ¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A .ʯīµç¼«·¢ÉúÑơ»¯·´Ó¦
B. ʯīµç¼«ÉϲúÉúÇâÆø
C. ͵缫·¢Éú»¹Ô·´Ó¦
D.µ±ÓĐ0.1molµç×Óת̉Æʱ£¬ÓĐ0.1molCu2OÉú³É¡£
16£®
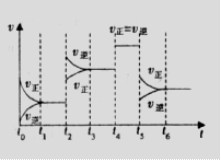 ijĂܱƠÈƯÆ÷ÖĐ·¢ÉúÈçÏ·´Ó¦£º A(g)+B(g) ¡¡¡¡¡¡¡¡2C(g)£»¡÷H<0£¬·´Ó¦ËÙ ÂÊ(
ijĂܱƠÈƯÆ÷ÖĐ·¢ÉúÈçÏ·´Ó¦£º A(g)+B(g) ¡¡¡¡¡¡¡¡2C(g)£»¡÷H<0£¬·´Ó¦ËÙ ÂÊ(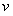 )Ëæʱ¼ä(
)Ëæʱ¼ä(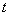 )±ä»¯µÄ¹ØϵÈçͼ£¬
)±ä»¯µÄ¹ØϵÈçͼ£¬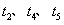 ʱ¿̀Íâ½ç̀ơ¼₫¸Ä ±ä£¬µ«¶¼Ă»Óиıä¸÷ÎïÖʼÓÈëÁ¿¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ¡¡¡¡ A£®
ʱ¿̀Íâ½ç̀ơ¼₫¸Ä ±ä£¬µ«¶¼Ă»Óиıä¸÷ÎïÖʼÓÈëÁ¿¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ¡¡¡¡ A£®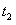 ʱÔö´óÁËѹǿ
ʱÔö´óÁËѹǿ
B£®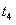 ʱ̉»¶¨Ê¹ÓĂÁË´ß»¯¼Á
ʱ̉»¶¨Ê¹ÓĂÁË´ß»¯¼Á
¡¡¡¡ C£®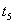 ʱ½µµÍÁËζÈ
ʱ½µµÍÁËζÈ
¡¡¡¡ D£® 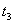 -
-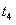 ʱ¼äÄÚAµÄ°Ù·Öº¬Á¿±È
ʱ¼äÄÚAµÄ°Ù·Öº¬Á¿±È 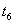 ºóµÍ
ºóµÍ
15£®Îª¼à²â¿ƠÆøÖĐ¹¯ƠôÆøÊÇ·ñ³¬±ê£¬Í¨¹ưĐü¹̉Í¿ÓĐCuI(°×É«)µÄÂËÖ½£¬¸ù¾ƯÂËÖ½ÊÇ·ñ±äÉ«(ÁÁ»ÆÉ«ÖÁ°µº́É«)¼°±äÉ«ËùĐèʱ¼äÀ´ÅĐ¶Ï¿ƠÆøÖĐµÄ¹¯º¬Á¿¡£·¢ÉúµÄ»¯Ñ§·´Ó¦Îª£º
4CuI+Hg = Cu2HgI4+2Cu ¡£ÏÂÁĐ˵·¨²»ƠưÈ·µÄÊÇ
A£®ÉÏÊö·´Ó¦ÊôÓÚÖĂ»»·´Ó¦¡¡¡¡¡¡¡¡¡¡¡¡ B£®¸Ă·´Ó¦ÖеÄÑơ»¯¼ÁΪCuI
C£®Cu2HgI4¼ÈÊÇÑơ»¯²úÎïÓÖÊÇ»¹Ô²úÎï¡¡
¡¡D£®µ±ÓĐ1 mol CuI²ÎÓ뷴Ӧʱ£¬×ª̉Ƶç×ÓµÄÎïÖʵÄÁ¿Îª0.5 mol
14£®.ÏÖÓĐŨ¶È¾ùΪ0.1 mol/L ¢Ù ´×ËáÈÜ̉º ¢Ú ÂÈ»¯ï§ÈÜ̉º ¢Û Ạ́ËáÈÜ̉º¸÷25 mL ¡£ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ¡¡¡¡
¡¡¡¡¡¡ A£®3ÖÖÈÜ̉ºpH ´óĐ¡µÄ˳Đ̣Ϊ¢Ù©ƒ¢Ú©ƒ¢Û
B£®3ÖÖÈÜ̉ºÖĐÓÉË®µçÀë²úÉúµÄÇâÀë×ÓŨ¶È´óµ½Đ¡Ë³Đ̣ÊÇ¢Ú©ƒ¢Ù©ƒ¢Û
C£®Èô½«3ÖÖÈÜ̉ºÏ¡ÊÍÏàͬ±¶Êư£¬pH ±ä»¯×î´óµÄÊÇ¢Ù
D£®Èô·Ö±đ¼ÓÈë25mL 0.1mol/LµÄÇâÑơ»¯ÄÆÈÜ̉ººó£¬pH ×î´óµÄÊÇ¢Ù
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com