
7.(07年广东理基·32)以下反应最符合绿色化学原子经济性要求的是
A.乙烯聚合为聚乙烯高分子材料 B.甲烷与氯气制备一氯甲烷
C.以铜和浓硝酸为原料生产硝酸铜 D.用SiO2制备高纯硅
答案:A
解析:绿色化学原子经济性的要求是反应中原子的利用最高,生产过程中无污染等。根据题目给出的各个选项中的反应,可以看出只有A选项中聚合反应符合。
6.(07年广东理基·27)某溶液中可能含有SO42-、CO32-、Cl-。为了检验其中是否含有SO42-,除BaCl2,除BaCl2溶液外,还需要的溶液是
A.H2SO4 B.HCl C.NaOH D.NaNO3
答案:B
解析:因为BaCO3也是一种白色沉淀,因此为了防止CO32-的干扰,还应需要用稀HCl,观察沉淀是否溶解。
5.(07年广东文基·66)下列溶液能使红色花瓣快速褪色的是
A.稀盐酸 B.新制氯水
C.氯化钙稀溶液 D.生理盐水
答案:B
解析:题目给出的选项中的物质只有B选项中的新制氯水中含有的HClO均有强氧化性,能够漂白有机色质。
4.(07年广东化学·6)下列说法正确的是
A.硅材料广泛用于光纤通讯
B.工艺师利用盐酸刻蚀石英制作艺术品
C.水晶项链和餐桌上的瓷盘都是硅酸盐制品
D.粗硅制备单晶硅不涉及氧化还原反应
答案:A
解析:硅与生活密切相关,B中刻蚀石英用氢氟酸,C中水晶成分为二氧化硅,D中粗硅与氯气反应再还原成硅是氧化还原反应。
3.(07年广东化学·5)氯气是一种重要的工业原料。工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是
A.若管道漏气遇氨就会产生白烟
B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应
D.生成1molN2有6mol电子转移
答案:C
解析:本题原理大多同学已在平时练习中接触过,06年高考题实验题21题⑵考到:将NH3通入溴水中,有N2生成,反应的化学方程式为 ,也与此题原理类似属氧化还原反应,故C错。当NH3过量时会与HCl反应生成NH4Cl白烟故A对,反应氯气为氧化剂,NH3为还原剂,氮由-3价升高至0价故生成1molN2有6mol电子转移,D对。
0.2L 0.2L
所以平衡前混合气体的体积为1L+0.2L=1.2L,因此反应后气体体积缩小率为 16.7%。
16.7%。
2.(07年宁夏理综·13)一定条件下,合成氨气反应达到平衡时,测得混合气体中氨气的体积分数为20.0% ,与反应前的体积相比,反应后体积缩小的百分率是
A.16.7% B.20.0% C.80.0% D.83.3%
答案:A
解析:设达到平衡后混合气体的体积为1L,则其中生成的氨气的体积为1L×20.0%=0.2L。则根据反应的方程式有:
N2+3H2 2NH3 △V
2NH3 △V
1 3 2 2
1.(07年山东理综·14)氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.在通入少量氯气, 减小
减小
B.通入少量SO2,溶液的漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量水,水的电离平衡向正反应方向移动
答案:D
解析:在氯水中存在如下平衡:Cl2+H2O HCl+HClO、H2O
HCl+HClO、H2O H++OH-、HClO
H++OH-、HClO H++ClO-。A中在通入少量氯气,平衡右移,生成的次氯酸和盐酸增多,氢离子浓度增大有两个方面原因,次氯酸浓度增大和盐酸完全电离,而次氯酸根的增大只受次氯酸浓度增大的影响,故该值增大,错误;B中通入二氧化硫,其与氯气反应生成无漂白性的盐酸和硫酸,漂白性减弱,错误;C中加入少量固体氢氧化钠反应后的溶液仍是电中性的,但酸碱性不为中性,应为弱酸性。溶液中阴阳离子所带正负电荷总数相等,故存在c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(ClO-),但是c(H+)应该大于c(OH-),故此等式不成立,错误;D中加水,即稀释氯水溶液的酸性减弱,即c(H+)减小,所以水的电离平衡向正向移动,正确。
H++ClO-。A中在通入少量氯气,平衡右移,生成的次氯酸和盐酸增多,氢离子浓度增大有两个方面原因,次氯酸浓度增大和盐酸完全电离,而次氯酸根的增大只受次氯酸浓度增大的影响,故该值增大,错误;B中通入二氧化硫,其与氯气反应生成无漂白性的盐酸和硫酸,漂白性减弱,错误;C中加入少量固体氢氧化钠反应后的溶液仍是电中性的,但酸碱性不为中性,应为弱酸性。溶液中阴阳离子所带正负电荷总数相等,故存在c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(ClO-),但是c(H+)应该大于c(OH-),故此等式不成立,错误;D中加水,即稀释氯水溶液的酸性减弱,即c(H+)减小,所以水的电离平衡向正向移动,正确。
1.(07年山东理综·12)下列叙述正确的是
A.16 8O2和18 8O2互为同位素,性质相似
B.常温下,pH=1的水溶液中Na+、NO3-、HCO3-、Fe2+可以大量共存
C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同
D.C(石墨,s)=C(金刚石,s) △H>0,所以石墨比金刚石稳定
答案:D
解析:A选项中同位素是指中子数不同、质子数相同的不同核素(原子)的互称,选项中给出的是分子,错误;B中PH=1的溶液为强酸性环境,解答时应在离子组Na+、NO3-、HCO3-、Fe2+ 中增加H+,分析可知碳酸氢根离子和氢离子不共存,在氢离子存在时硝酸根离子和亚铁离子不能共存,错误;C中明矾的净水原理是其溶于水电离产生的铝离子水解生成氢氧化铝能吸附水中悬浮物,而漂白粉是由其成分中的次氯酸钙和水、二氧化碳反应生成的次氯酸能杀菌消毒,作用原理不同,错误;D中此反应的△H>0,说明此反应是吸热反应,也就是金刚石的具有能量大于石墨,物质具有的能量越大,该物质越不稳定,正确。
25.(本题满分10分)已知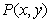 为函数
为函数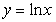 图象上一点,
图象上一点,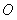 为坐标原点,记直线
为坐标原点,记直线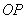
的斜率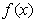 .
.
(Ⅰ)求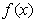 的最大值;
的最大值;
(Ⅱ)令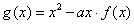 ,试讨论函数
,试讨论函数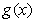 在区间
在区间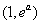 上零点的个数(
上零点的个数( 为自
为自
然对数的底数,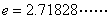 ).
).
台州市2008学年第二学期高二期末质量评估试题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com