
3.已知四种丁醇在催化剂存在下跟空气反应的情况如下:
|
|
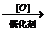 CH3CH2CH2CHO
CH3CH2CH2CHO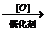 CH3CH2CH2COOH
CH3CH2CH2COOH
|
|
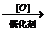 (CH3) 2CHCHO
(CH3) 2CHCHO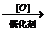 (CH3) 2CHCOOH
(CH3) 2CHCOOH
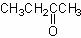
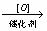
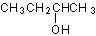
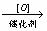
|
(CH3) 3COH 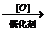 不反应
不反应
(1)各种戊醇在这样的情况下,可能得到多少种酮,请写出其结构简式。
(2)各种戊醇在这样的情况下,可能得到多少种醛,请写出其结构简式。
(3)请写出始终不反应的戊醇的结构简式。
2. A和B两种物质的分子式都是C7H8O,它们都能跟金属反应放出氢气。A不溶于NaOH溶液,而B能溶于NaOH溶液。B能使适量溴水褪色,并产生白色沉淀,A不能。B的一溴代物有两种结构。写出有A和B的结构简式和名称。
1.( )白藜芦醇 广泛存在于食物(例如桑椹、花生、尤其是
葡萄)中,它可能具有搞癌性。能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是 A、1mol 1mol B、3.5 mol 7mol C、3.5mol 6mol D、6mol 7mol
5、苯酚的用途:
重要化工原料,制酚醛树脂、染料、药品,稀溶液可用于防腐剂和消毒剂。
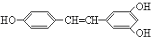 [巩固练习]
[巩固练习]
4、化学性质
⑴弱酸性: 俗名 ,加入石蕊的现象是什么?
① 酸性的验证:浊液中加入NaOH变澄清
②酸性强弱及验证:
a. 酸性 :
b. 弱酸性:
 思考:
-OH+Na2CO3
→ -ONa+NaHCO3 ?
思考:
-OH+Na2CO3
→ -ONa+NaHCO3 ?
 -OH+NaHCO3 → -ONa+CO2+H2O ?
-OH+NaHCO3 → -ONa+CO2+H2O ?
⑵取代反应:(易与Br2、HNO3发生苯环H取代,不能发生-OH取代)
①卤代(反应方程式):
注意:a常温下浓溴水即能与苯酚反应,说明苯酚的取代比苯及同系物容易,
b此反应常用于苯酚的定性检验、与定量测定,
 c ( -OH)的除杂与分离:
c ( -OH)的除杂与分离:
②硝化: 2,4,6-三硝基苯酚,俗名:苦味酸,烈性炸药
 ⑶显色反应:苯酚+Fe3+→溶液呈紫色(用于Fe3+和 -OH的相互鉴别(方程式)
⑶显色反应:苯酚+Fe3+→溶液呈紫色(用于Fe3+和 -OH的相互鉴别(方程式)
⑷其它反应:氧化反应、缩聚反应、酯化反应
3、结构特点:
⑴苯环与-OH互相影响
①苯环对-OH的影响:C-O极性减弱,O-H极性增强--酸性,显色
②-OH对苯环的影响:邻、对位H活泼性增强--取代
⑵苯酚-OH中的H原子与苯环不在同一平面内。
2、物性:
⑴色、态、味:
⑵熔沸点:43℃(保存,使用)
⑶溶解性:
⑷毒性:有毒,对皮肤有腐蚀性(不慎沾到皮肤上应立即用 洗涤)
说明:在溶液中生成的苯酚一般以水合物的形式存在,呈液态,不溶于水,ρ>1g·cm-3
1、酚类知识:
⑴代表物:苯酚
⑵苯酚的同系物:CnH2n-6O,如:CH3-C6H4-OH
 ①酚中烃基异构
①酚中烃基异构
⑷酚的同分异构体 ②与芳香醇异构
③与芳香醚
练习:写出C8H10O,分子中含有苯环的有机物的同分异构体
5、乙醇的化学性质(醇类的重要代表物)
⑴化学性质
①与活泼金属反应:
②消去反应:
[说明]
a.浓H2SO4的作用: 、
b.混合液的配制:乙醇与浓硫酸体积比1:3(如何混和?)
c.温度控制:迅速将温度升到170℃,不能过高或过低(原因)
温度计的水银球在
d.加热前加几粒碎瓷片,防止暴沸。
③与HX:
④氧化反应:
a.燃烧氧化:
b.催化氧化:
c.强氧化剂氧化:酸性KMnO4、K2Cr2O7(橙色→绿色)
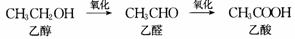
小结:有机氧化还原反应:氧化反应:加氧或去氢,还原反应:加氢或去氧,
⑤酯化反应:
⑵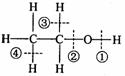 乙醇分子结构与化学性质的关系
乙醇分子结构与化学性质的关系
与活泼金属反应、酯化---断裂 取代(HX)--断裂
催化氧化--断裂
分子内脱水(消去)--断裂 分子间脱水(取代)--断裂
4、醇的物理通性:
⑴熔沸点:
⑵溶解性:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com