
【题目】下表是元素周期表的部分内容,回答下列问题。
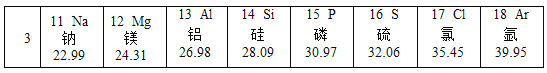
(1)1869年俄国化学家______________(填“道尔顿”“门捷列夫”“阿伏加德罗”或“居里”)列出了第一张有代表性的元素周期表;
(2)请从上表中查出硅元素的一条信息____________________。
(3)已知某微粒的结构示意图为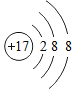 ,该微粒的符号为
,该微粒的符号为
(4)根据表中内容,可总结出的一条规律是____________________。
【答案】门捷列夫 硅元素的原子序数为14(或硅的元素符号为Si,合理即可) C1- 同一周期中元素的原子序数自左到右依次增加
【解析】
(1)1869年,俄国化学家门捷列夫发现了元素周期律并编制出元素周期表;
(2)由元素周期表中一格的信息可知,硅元素的原子序数为14(或硅的元素符号为Si,硅元素的相对原子质量为28.09等合理即可);
(3)由该微粒的结构示意图为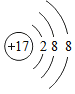 可知,该元素的质子数为17,即第17号元素(质子数=原子序数)氯元素,核外电子数为2+8+8=18质子数<电子数,故该微粒为氯离子,符号为C1-;
可知,该元素的质子数为17,即第17号元素(质子数=原子序数)氯元素,核外电子数为2+8+8=18质子数<电子数,故该微粒为氯离子,符号为C1-;
(4)由表中信息可知,第3周期中元素原子的序数从11依次增加到18。故可总结出的一条规律是:同一周期中元素的原子序数自左到右依次增加。


科目:初中化学 来源: 题型:
【题目】分析下图,回答问题。
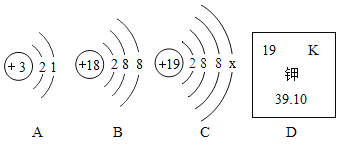
(1)图A为锂元素(Li)的原子结构示意图,锂离子的符号为_____。
(2)图B为氩元素的原子结构示意图,氩元素在周期表中位于第_____周期;
(3)图C为钾元素的原子结构示意图,图D为钾元素在周期表中的相关信息。
①x的数值为_____。
②钾元素的相对原子质量为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“宏观—微观—符号”三重表征是化学独特的表示物质及其变化的方法。某化学反应的微观示意图如图所示,下列说法不正确的是![]()
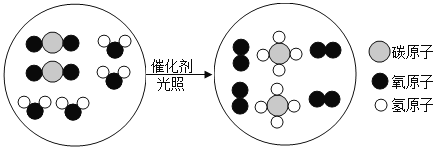
A.从微观构成看:四种物质均由分子构成
B.从物质分类看:该反应涉及到2种氧化物
C.从反应价值看:该反应能获取清洁能源
D.从表示方法看:该反应的化学方程式为2CO2+4H2O 2CH4+4O2
2CH4+4O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学活动兴趣小组的同学进行木炭还原 CuO 的探究实验,生成物是红色固体和无色气体。他们查阅资料后得知氧化亚铜(Cu2O)为红色固体,猜测反应物比例不同,产物也会不同。因此,生成物中有 CO2、CO和Cu,固体还可能有Cu2O。又知Cu2O能和常见的酸(HNO3除外)反应生成Cu2+和Cu。为此,请你和他们一起进行如下探究。
(1)探究气体中是否有CO气体。甲同学设计的方案是:先将气体通过足量的NaOH溶液,干燥后再通过灼热的CuO,未反应完的气体直接排放到空气中。
①甲同学实验后如果有______色固体生成,说明一定含有CO气体;
②上述实验方案中可选用的一种气体干燥剂是_________;
③甲同学设计的实验方案有无不足之处?若有,请你指出有何不良后果,并提出改进方案;若没有,该问不需作答。 _______。
(2)探究红色固体中是否有 Cu2O。
①在如下方法中:a 上网查询 b 实验 c 请教老师
你认为最能解决实际问题的方法是_______(填字母序号)。
②请你设计一个简便的实验方案,检验红色固体中是否有 Cu2O。
实验步骤 | _______ |
实验现象与结论 | _______ |
化学反应方程式 | _______ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 Na2CO3与 HCl 反应分两步进行:
第一步 Na2CO3与 HCl 反应生成 NaHCO3:![]() ;
;
第二步 NaHCO3 与 HCl 反应生成 CO2:![]() 。
。
现有这样一个实验:在两支试管中分别加入 3mL 稀盐酸,将两个各装有 0.3g NaHCO3 或 Na2CO3 粉末的小气球分别套在两支试管口,将气球内的NaHCO3或 Na2CO3 同时倒入试管中(反应中盐酸足量)。观察到现象如下:
(1)盛________的试管中产生气体的速率要快得多。
(2)盛_________的试管中气球变得更大,大小气球中生成气体的质量之比为(填最简单整数比)_____。
(3)甲同学用手触摸试管,发现盛 NaHCO3 粉末的试管变冷,而盛 Na2CO3的试管温度有升高。为研究是吸热还是放热反应,继续进行了下列实验(每次实验各做 3 次平行实验,取平均值):
序号 | 试剂 1 | 试剂 2 | 混合前温度 | 混合后温度 |
① | 35mL 水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
② | 35mL 水 | 3.2 Na2CO3固体 | 20℃ | 24.3℃ |
③ | 35mL 稀盐酸 | 含2.5g NaHCO3的饱和溶液 32.5mL | 20℃ | 19℃ |
④ | 35mL 稀盐酸 | 含 3.2g Na2CO3的饱和溶液 23.1mL+10ml 水 | 20℃ | 24.2℃ |
⑤ | 35mL 稀盐酸 | 2.5gNaHCO3固体 | 20℃ | 16.2℃ |
⑥ | 35mL 稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
通过上述实验可得出五条结论:
①NaHCO3 的溶解是__(吸热或放热)过程;
②Na2CO3 的溶解是____(吸热或放热)过程;
③NaHCO3 的饱和溶液和盐酸的反应是___(吸热或放热)反应;
④Na2CO3 的饱和溶液和盐酸的反应是____(吸热或放热)反应;
⑤NaHCO3 固体与稀盐酸反应的反应热是由_____(填①~⑤序号)的热效应之和。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对销售的化肥,国家有明确的质量要求。某兴趣小组对市售的某钾肥进行了检测,称取2.0g样品放入烧杯中,加入适量的水溶解后,逐滴加入10%的BaCl2溶液,产生沉淀的质量与所加入BaCl2溶液质量的关系如图1所示(假定杂质不参加反应)。
已知:K2SO4+BaCl2═BaSO4↓+2KC1。

(1)20.8g BaCl2溶被中所含溶质的质量为_____g。
(2)通过计算,判断该钾肥中K2SO4的质量分数是否符合图2的包装说明________?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】随着时代的发展,我国工信部发布了《中国传统燃油车退出时间表研究》,提出一级城市私家车将在2030年实现全面新能源化,下图是汽车系统组成图,请回答下列问题。

(1)汽车底盘传动轴用到铝合金,铝合金有较好的抗腐蚀性。请用化学方程式写出其原因:_____。
(2)汽车内部车壳装饰等会用到塑料,塑料属于_____材料。
(3)车身大部分会用到合成钢,生铁和钢的区别是_____不同。
(4)传统燃油车尾气会排放出大气污染气体如二氧化硫、氮氧化物等导致的环境问题是_____的形成
(5)电动汽车在进行铅酸电池充电时,发生的反应:2PbSO4+2H2O![]() Pb+2H2SO4+X,则X的化学式为_____。
Pb+2H2SO4+X,则X的化学式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组发现铁钉生锈需要几天的时间,询问老师如何加快铁钉生锈的速度。
老师说氯化物可能加快铁钉生锈的速度。
【提出问题】氯化物对铁钉生锈有怎样的影响?
【查阅资料】
ⅰ.NaCl、CaCl2、CuCl2等由氯离子与金属离子构成的盐属于氯化物。
ⅱ.铜能与氧气反应,生成黑色的CuO。
ⅲ.CuO能与稀硫酸发生反应:CuO + H2SO4 ==== CuSO4 + H2O。
【进行实验、分析解释、获得结论】
实验1:探究氯化物对铁钉生锈速度的影响。
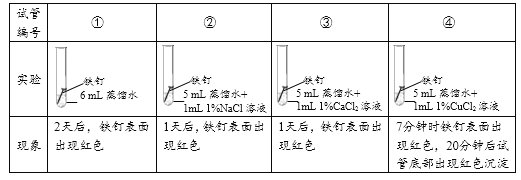
(1)对比实验①②③可以得到的结论是_________。
(2)小组同学认为,试管④中的红色沉淀可能是铁锈,也可能是铜。他们认为红色沉淀可能是铜的理由是__________(用化学方程式解释)。
实验2:探究试管④中红色沉淀的物质组成。
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 取出试管④中的铁钉,过滤剩余物,洗涤滤纸上的物质 | 固体为红色 |
Ⅱ | 将步骤Ⅰ所得红色固体加入试管中,再向试管中加入足量的___________ | 红色固体大部分溶解,溶液变为黄色 |
Ⅲ | 将步骤Ⅱ所得混合物过滤,洗涤、干燥滤纸上的固体后,置于石棉网上充分加热 | 红色固体变黑 |
Ⅳ | 向试管中加入步骤Ⅲ所得黑色固体,再加入足量稀硫酸 | 黑色固体全部溶解,溶液变为蓝色 |
(3)步骤Ⅱ中所加入的试剂是_________。
(4)步骤Ⅲ、Ⅳ的实验目的是_________。
(5)由实验2可得出结论:试管④中红色沉淀的物质组成是_________。
【反思与评价】
(6)结合实验1、2的结论,对于“氯化物对铁钉生锈速度的影响”,小组同学提出了进一步的假设:__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】废旧电池属于有害垃圾,其中锂电池主要回收工艺流程如下:
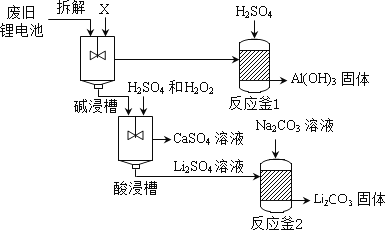
(1)碱浸槽中注入的X溶液,其pH>7,X是下列的______(填序号)。
A 稀盐酸 B 蒸馏水 C 氢氧化钠溶液
(2)反应釜2中发生复分解反应的化学方程式为_______。
(3)上述工艺回收到的产物有_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com