

| 浓度 时间(min) 条件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
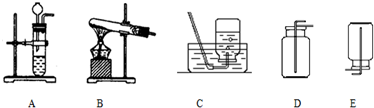
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
(4)氧气的密度比空气的密度大,不易溶于水,能够支持燃烧,能使带火星的木条复燃;
(5)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置;
(6)根据实验现象可以判断相关方面的问题.
解答 解:(1)a是酒精灯,常用作热源;b是铁架台,常用于固定、支持实验装置.
故填:酒精灯;铁架台.
(2)用双氧水和二氧化锰来制取氧气时不需要加热,可选用的发生装置是B,其中二氧化锰起催化作用.
故填:B;催化.
(3)用高锰酸钾制取氧气时,发生反应的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
故填:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(4)用E装置收集氧气的依据是氧气密度比空气大,检验氧气是否集满的方法是:把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
故填:氧气密度比空气大;把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
(5)实验室用氯化铵固体与碱石灰固体共热来制取氨气时,应该用A装置作为发生装置;
氨气极易溶于水,不能用排水法收集,密度比空气小,可以用向下排空气法收集,即用D装置收集;
若用F装置收集氨气,由于氨气不断比空气小,氨气应从n端进入.
故填:A;D;n.
(6)问题:
(1)由以上可知,二氧化锰和氧化铁能够加快过氧化氢分解的速率,而反应前后质量不变,因此MnO2、Fe2O3在上述反应中的作用是催化剂.
故填:催化剂.
(2)为了和①比较,实验 ②、③中H2O2的浓度(w%)以5%为宜.
故填:5%.
问题:(3)从上表中可知,相同浓度的过氧化氢溶液在相同质量的二氧化锰和氧化铁的催化作用下,加入二氧化锰的过氧化氢分解的快,说明二氧化锰的催化效果比氧化铁的催化效果好;
不同浓度的过氧化氢溶液,在相同催化剂的催化作用下,浓度大的过氧化氢分解的快,说明浓度越大,分解速率越快.
故填:二氧化锰的催化效果比氧化铁的催化效果好,浓度越大,分解速率越快.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:初中化学 来源: 题型:选择题
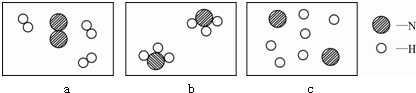
 如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法不正确的是( )
如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法不正确的是( )| A. | 反应物都是单质 | |
| B. | 该反应中,参加反应的两种分子个数比为2:1 | |
| C. | 反应前后,原子的种类与数目都发生了改变 | |
| D. | 反应前后,分子的种类与数目都发生了改变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
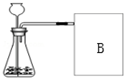
 A-F为初中化学中常见的物质,已知A为暗紫色固体,D为一种黑色粉末,它们的转化关系如图所示.请回答:
A-F为初中化学中常见的物质,已知A为暗紫色固体,D为一种黑色粉末,它们的转化关系如图所示.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 研究性学习小组选择“H2O2 溶液分解生成O2的反应快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
研究性学习小组选择“H2O2 溶液分解生成O2的反应快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2溶液 | 5%H2O2溶液 |
| 催化剂 | 1g水泥块 | 1gMnO2 |
| 时间 | 165秒 | 46秒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com