
【题目】甲乙两化学兴趣小组的同学按课本上的实验装置做“测定空气中氧气的体积分数”实验(如图甲所示),但测出的氧气的体积分数存在误差。

请你参与探究:
甲组测出氧气的体积分数小于五分之一
(提出问题)造成误差的原因是什么?如何改进课本上的实验装置?
(查阅资料)红磷、白磷的一些性质如下表:
颜色、状态 | 熔点/℃ | 着火点/℃ | 密度(g/cm3) | |
红磷 | 暗红色固体 | 590 | 240 | 2.34 |
白磷 | 白色或黄色固体 | 44.1 | 40 | 1.82 |
(猜想与假设)
A同学:可能是导管内原含有空气,后来留有吸入的水,影响实验的准确性。
B同学:可能是瓶内残留气体中还有氧气。
(1)你还能作出的猜想是____________________________。
(交流与讨论)
他们对课本上的实验装置进行了图乙所示的改进(其他仪器忽略)。
(2)与课本上的实验装置相比较,该装置的一个优点是 _______________。
(3)能得出空气中氧气约占五分之一体积的实验现象是 _______________。
乙组同学从课本镁条燃烧实验得到启发,用镁代替红磷,实验完毕,冷却后进入水的体积远大于总容积的1/5。
(猜想与假设)可能镁条与氮气发生了反应
(设计实验)
为检验镁条能否在N2中燃烧,兴趣小组展开如下探究:

①组装仪器(图1,钟罩下端无底),检查气密性:向水槽中加水,观察现象;
②将足量白磷在空气中点燃后,迅速伸入钟罩内,塞紧橡皮塞;
③待钟罩内水面不再变化时,向水槽中加水,使水槽中液面与钟罩内液面相平;
④打开橡皮塞,将燃着的螺旋状镁条迅速伸入钟罩内,塞紧橡皮塞(图2),观察液面变化;
(交流讨论)
(4)步骤①气密性良好的现象是________________________;
(5)步骤②目的是_____________________________________;
(6)步骤④观察到_____________________现象,说明镁条与氮气反应。
(结论)除氧气外,镁条还能与氮气反应。
(反思)乙组小罗同学认为只进行图2实验,当钟罩内进入水的体积大于总容积的1/5,就能说明镁与氧气、氮气都发生了反应,对此观点你认为是否正确_______,并说明理由__________________ 。
(拓展)①镁与氮气反应生成氮化镁(Mg3N2),由于氧气比氮气活泼,所以镁燃烧生成的氮化镁质量比氧化镁_______(大、小)。
②8g镁在空气中燃烧,若有30%的镁生成氮化镁,计算氮化镁的质量__________(写出计算过程)。
【答案】红磷量不足/橡皮塞未塞紧(合理即可) 确保装置不漏气 左边液面上升至“1”刻度处 表面皿上浮 对比实验 图2中的表面皿高于图1中的表面皿 不正确 可能实验误差造成,如:装置的气密性不好,导致气体逸出等 小 3.3g
【解析】
[猜想与假设]
(1)测定空气中氧气含量的原理是,利用物质与空气中的氧气反应,又不生成气体,使瓶内气体减少,压强变小,水倒流入集气瓶内,倒流的水的体积就等于瓶内氧气的体积。还可能作出的猜想是红磷量不足、橡皮塞未塞紧(即装置的气密性不好)或者没冷却到室温(合理即可)导致甲组测出氧气的体积分数小于五分之一;
[交流与讨论]
(2)与课本上的实验装置相比较,该装置的一个优点是确保装置不漏气(即能始终保持良好的气密性),使测定结果更准确;
(3)能得出空气中氧气约占五分之一体积的实验现象是左边液面上升至“1”刻度处;
[交流讨论]
(4)步骤①气密性良好的现象是表面皿上浮;
(5)步骤②目的是对照试验,通过比较表面皿上升的程度,探究镁条是否与氮气反应;
(6)步骤④观察到图2中的表面皿高于图1中的表面皿,说明镁条与氮气反应;
[反思]乙组小罗同学认为只进行图2实验,当钟罩内进入水的体积大于总容积的1/5,就能说明镁与氧气、氮气都发生了反应,此观点不正确,理由:可能实验误差造成,如:装置的气密性不好,导致气体逸出等;
[拓展]①镁与氮气反应生成氮化镁(Mg3N2),由于氧气比氮气活泼,所以镁燃烧时几乎都与氧气发生了反应,因此生成的氮化镁质量比氧化镁小;
②8g镁在空气中燃烧,若有30%的镁生成氮化镁,则氮化镁中镁元素的质量为8g×30%=2.4g,氮化镁的质量: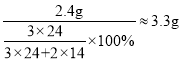 。
。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:
【题目】自然界的水含有各种杂质,可以用不同的方法进行净化。

(1)如图所示是用空塑料饮料瓶、带导管的单孔胶塞、蓬松棉、纱布、活性炭、小卵石、石英沙等材料自制的一个简易净水器。
①根据上述净化材料的特性,B层放置的材料最好是____;
②该净水器第二层纱布的主要作用是________;
③你认为上述简易净水器(填“可以”或“不可以”)___将硬水变成软水,原因___;用___能区分硬水和软水。
(2)如图为过滤装置,根据实验回答下列问题:
①写出标号仪器的名称:a______;
②实验过程中玻璃棒的作用是______;
③过滤后发现滤液仍然浑浊,可能的原因是(答出三点)____、_____、____
查看答案和解析>>
科目:初中化学 来源: 题型:
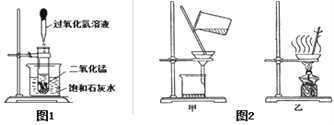
【题目】如图1所示,向试管中放入1.0g二氧化锰,把试管固定在盛有饱和石灰水(20℃)的烧杯中,再向试管中滴入约5mL的15%的过氧化氢溶液。
(1)实验中观察到的明显现象有:①______________________;②烧杯中的饱和石灰水变浑浊。
(2)分析产生上述现象②的原因是:①____________________;②__________________。
(3)写出试管中发生反应的化学方程式:____________________________。
(4)若要回收二氧化锰,可以选择图2操作中的__________(填“甲”或“乙”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究Fe、Cu、Ag的金属活动性强弱,某兴趣小组做如下实验:
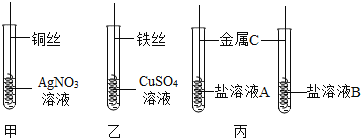
(1)甲实验中发生反应的化学方程式为_____;乙实验中观察到的现象为_____。
(2)通过甲乙实验探究,可得出三种金属活动性由强到弱的顺序为_____。
(3)若采用丙实验方案可得出相同结论,则金属C是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】汽车尾气净化装置中装有铂催化剂,尾气在催化剂表面反应的微观过程可用图表示.下列有关说法错误的是
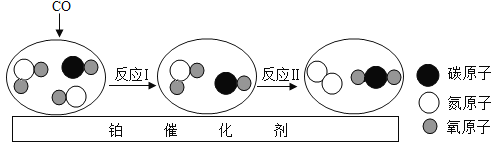
A. 化学反应前后原子的种类和个数保持不变
B. 反应Ⅱ元素的化合价都没有变化
C. 反应Ⅰ类型为化合反应
D. 此净化装置可以消除一氧化碳、一氧化氮、二氧化氮对空气的污染
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学在学习了拉瓦锡测空气中氧气含量的测定方法后,自己设计如图所示的装置,用来测空气中氧气的含量。该同学的实验步骤如下:
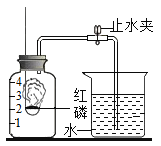
①将图中的集气瓶分为5等份,并做好标记;
②将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入瓶内,塞紧橡皮塞;
③充分反应后,冷却到室温,打开止水夹。
请回答下列问题:
(1)实验中红磷需稍过量,目的是_______________。
(2)步骤③中打开止水夹后观察到的现象是______________。
(3)该实验可推论出氮气_______(填“难”或“易”)溶于水和其化学性质________(填“活泼”或“不活泼”)的结论。
(4)实验中最终气体减少的体积常常小于拉瓦锡测定的1/5,从装置和操作的失误分析,其原因可能是__________(写出一条即可)。
(5)请写出磷燃烧的符号表达式_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】学习了氧气的性质后,小军和小宇同学取几根纱窗细铁丝,拧成一束呈螺旋状绕在一根火柴上,点燃火柴,待火柴临近烧完时缓缓伸入盛氧气的集气瓶中,实验流程如图所示:
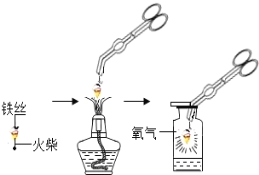
(1)老师在演示铁丝在氧气中燃烧的实验过程中,在铁丝上系一根火柴的目的是______,把铁丝绕成螺旋状的目的是____________________。
(2)小军同学在空气中进行过铁丝燃烧实验,发现铁丝不能燃烧,是由于________。
(3)小宇同学在空气中进行过铁丝燃烧实验,发现铁丝也不能燃烧,可能的原因是________(写一点即可)。
(4)若铝丝在纯氧气中也能剧烈燃烧,燃烧后的生成物是氧化铝,该反应的文字表达式为_______,其基本反应类型属于________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验装置图,回答问题。
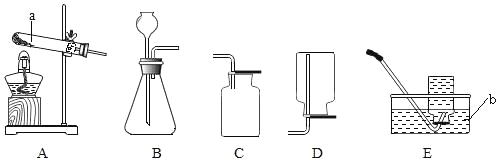
(1)图中仪器的名称:a________b________
(2)用高锰酸钾制氧气的化学方程式________应选用的发生装置为________ (填字母序号,下同)。
(3)用排水法收集氧气时,当观察到________时,开始收集。
(4)硫在氧气中燃烧实验中,集气瓶中要预留一些水,原因是________该实验的现象是________。
(5)实验结束时,发现试管炸裂了,分析其可能的原因________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素完全相同的化合物,丙是单质;乙通常为液体,在一定条件下可分解生成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去)。
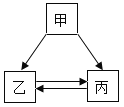
(1)甲分解生成乙和丙的化学式反应式为_____。
(2)从微观的角度解释甲、乙性质有差异的原因是_____。
(3)选择合适物质,让丙生成乙,化学反应式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com