
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管底部有黑色固体 | 燃烧产物中肯定有C |
| (2) | 取少量(1)所得上层溶液,加入过量的CaCl2溶液 | 有白色沉淀生成 | 燃烧产物中肯定有Na2CO3 |
| (3) | 取少量(2)所得上层清液,加入CuSO4(或CuCl2) | 溶液变红 | 燃烧产物中肯定有Na2O |
分析 【提出猜想】钠能发生类似于CO2与镁的反应,用类比的方法可书写其发生的化学方程式;
【实验】根据资料,同学们认为钠在CO2中燃烧的产物应该与Mg在CO2中燃烧的产物情况有所不同,并对产物提出几种猜想;通过质量守恒定律可知分析,猜想③肯定是错误的;
【验证猜想】
由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,推测操作.了解在步骤(2)中CaCl2溶液为什么要加入至过量的原因.
【结论】由猜想得结论.
解答 解:【提出猜想】钠能发生类似于CO2与镁的反应,故可用类比的方法书写其发生的化学方程式为:4Na+CO2 $\frac{\underline{\;点燃\;}}{\;}$2Na2O+C.
【实验】将燃着的钠伸入装有CO2的集气瓶中,钠能在CO2中继续燃烧.
进一步查阅资料得知:①Na2O是白色固体,能与CO2反应生成Na2CO3,与H2O反应生成NaOH.②Ca(OH)2溶于水而CaCO3不溶于水.③Na2CO3的存在会干扰NaOH的检测.基于以上资料,同学们认为钠在CO2中燃烧的产物应该与Mg在CO2中燃烧的产物情况有所不同,并对产物提出了以下几种猜想:①Na2O、C;②Na2CO3、C;③NaOH、C;④Na2O、Na2CO3、C;
通过理论分析,猜想:③肯定是错误的,理由是:NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知③错误.
【验证猜想】由操作和现象,得出结论;或由操作和结论,推测现象;或由现象和结论,推测操作:故
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管 底部有黑色固体 | 燃烧产物中肯定有C(炭) |
| (2) | 取(1)所得少量上层清液,加入过量的CaCl2溶液 | 有白色沉淀生成 | 燃烧产物中肯定有Na2CO3 |
| (3) | 取(2)所得少量上层清液,加入 CuSO4(或CuCl2)溶液 | 有蓝色沉淀生成 | 燃烧产物中肯定有 Na2O |
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | |||
| (2) | 有白色沉淀生成 | ||
| (3) | CuSO4(或CuCl2) | Na2O |
点评 掌握质量守恒定律的也是守恒的思想处理问题;了解物质的鉴别与推断的方法.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:初中化学 来源: 题型:解答题
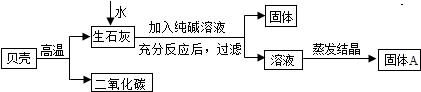
| 实验操作 | 现象 | 结论 | |
| 甲 | 取少量固体A,用适量水溶解后,滴加几滴无色酚酞溶液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体A,用适量水溶解后,滴加几滴饱和碳酸钠溶液 | 没有出现白色沉淀 | 猜想不成立 |
| 你 | 取少量固体A,溶于适量水形成溶液后,滴加足量的稀盐酸 | 有气泡产生 | 猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向盛有硫酸铜晶体的试管中加水,观察晶体的溶解情况 | |
| B. | 在硫酸铜溶液中滴加氢氧化钠溶液,观察溶液的变化 | |
| C. | 加热试管中的一块硫酸铜晶体,观察晶体的变化 | |
| D. | 在硫酸铜粉末中逐滴加入水,观察发生的现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入过量稀盐酸除去氢氧化钠溶液中混有的少量碳酸钠 | |
| B. | 用高温煅烧的方法除去生石灰中的石灰石 | |
| C. | 加入熟石灰,然后用研磨的方法鉴别氯化钾与氯化铵固体 | |
| D. | 用水鉴别碳酸钙和氢氧化钠两种粉末状固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
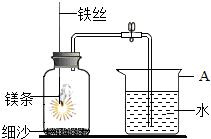 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
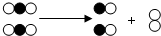 如图是表示物质间发生的一种化学反应模型示意图,图中“
如图是表示物质间发生的一种化学反应模型示意图,图中“ 、
、 ”分别表示两种不同元素的原子.该反应的类型属于( )
”分别表示两种不同元素的原子.该反应的类型属于( )| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 1g物质完全燃烧产生CO2的质量 | 1g物质完全燃烧放出的热量 | |
| CH4 | 2.75g | 56kJ |
| C | 3.67g | 32kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com