
| 白色粉末的成分 | 形成的原因 |
| 可能是CaCO3 | 石灰水与空气中CO2 反应,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O |
可能是Ca(OH)2 | 暑假气温较高,溶质的溶解度降低或溶剂蒸发, 石灰水中的溶质结晶析出 |
| OH- | Cl- | CO32- | NO3- | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
| 实验步骤 | 可能观察到的现象 | 结论 |
| 取上述试管中的上层清液,滴加1~2无色酚酞试液 | 酚酞试液变红色 | 溶液中含有含Ca(OH)2 |
| 往上述试管中的残留的固体中加入稀盐酸 | 有气泡产生 | 白色粉末中 (选填“有”或“无”)CaCO3 |
| 由上述实验可知白色粉末的成分是:CaCO3和Ca(OH)2的混合物. | ||
分析 (1)根据氢氧化钙能与二氧化碳反应生成碳酸钙沉淀,氢氧化钙溶液蒸发溶剂析出氢氧化钙分析白色粉末形成的原因及成分进行分析;
(2)根据氢氧化钙微溶于水、溶液显碱性、碳酸钙能与盐酸反应生成气体进行分析.
解答 解:(1)氢氧化钙能与二氧化碳反应生成碳酸钙沉淀,反应的方程式是:CO2+Ca(OH)2=CaCO3↓+H2O;由于氢氧化钙的溶解度随着气温的升高,溶质的溶解度会变小或溶剂蒸发,析出氢氧化钙粉末,所以白色粉末可能是碳酸钙,也可能是氢氧化钙,还可能是碳酸钙和氢氧化钙的混合物;
(2)甲同学的结论不严密的理由是:Ca(OH)2微溶于水也可能不溶解而沉淀;由于氢氧化钙溶液显碱性,由清液在滴加1~2滴无色酚酞试液后溶液变红,说明了溶液中含有含Ca(OH)2,;由于碳酸钙能与盐酸反应生成气体,所以实验中产生气泡,说明有碳酸钙;于是得出结论:白色粉末的成分是:CaCO3和Ca(OH)2的混合物.
故本题答案为:(1)CO2+Ca(OH)2=CaCO3↓+H2O;碳酸钙和氢氧化钙;
(2)Ca(OH)2微溶于水也可能不溶解而沉淀;溶液中含有含Ca(OH)2;有;CaCO3和Ca(OH)2的混合物.
点评 本题主要考查了氢氧化钙的变质,及氢氧化钙和碳酸钠的化学性质,培养学生分析问题、解决问题的能力.


科目:初中化学 来源: 题型:选择题
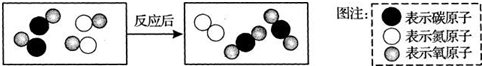
| A. | 图中单质的化学式为O2 | B. | 该反应使有害气体转化为无害气体 | ||
| C. | 该反应属于置换反应 | D. | 生成单质与化合物的质量比为7:11 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质是由原子组成的,原子中有原子核,所以利用任何物质都能得到核能 | |
| B. | 到目前为止,人类获得核能有两种途径,即原子核的裂变和聚变 | |
| C. | 原子弹和氢弹都是利用原子核裂变的原理制成的 | |
| D. | 自然界的原子核只有在人为的条件下才会发生聚变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验方案 | 使用的试剂 | 判断的方法 |
| A | 铁粉 | 如果有气泡产生,表明盐酸已经过量 |
| B | pH试纸 | 如果pH<7,表明盐酸已经过量 |
| C | 硝酸银溶液 | 如果有白色沉淀产生,表明盐酸已经过量 |
| D | 紫色石蕊试剂 | 如果溶液变成红色,表明盐酸已经过量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 浓硫酸(H2SO4)500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
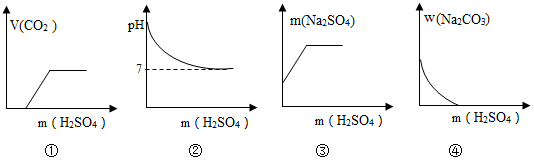
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na+Cu2+Cl- NO3- | B. | H+ Na+ Cl- SO42- | ||
| C. | Ag+ Na+NO3- Cl- | D. | Na+K+ NO3- CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com