
| A. | NaCl NaOH KNO3 | B. | Ba(NO3)2 KNO3 H2SO4 | ||
| C. | Ca(OH)2 HCl KCl | D. | Na2CO3 CaCl2 HNO3 |
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
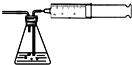 如图所示,某同学为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水,发现石灰水没有变化.据此,你认为该同学不应该( )
如图所示,某同学为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水,发现石灰水没有变化.据此,你认为该同学不应该( )| A. | 得出空气中没有二氧化碳的结论 | |
| B. | 仔细分析得到该结果现象的可能性,做出猜想 | |
| C. | 继续用大针筒向澄清石灰水压入空气 | |
| D. | 再一次检查该装置的气密性 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 选项 | 实验目的 | 实验设计 |
| A | 除去硫酸铜溶液中的硫酸 | 加入过量的 氢氧化铜,充分反应后过滤 |
| B | 区别氢气和一氧化碳 | 分别点燃后,观察火焰颜色 |
| C | 分离氯化钠和硝酸钾 | 充分溶解后,过滤 |
| D | 验证食醋具有酸的性质 | 用紫色石蕊检验,变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
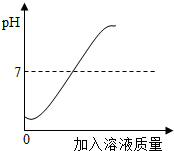 酸与碱作用生成盐和水的反应,叫中和反应.在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示:
酸与碱作用生成盐和水的反应,叫中和反应.在用盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程溶液的pH的变化曲线如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 样品中只含有NaHCO3 | B. | 样品中一定混有NaHCO3,可能有KCl | ||
| C. | 样品中有NaHCO3,也有Ba(NO3)2 | D. | 样品中一定混有KCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com