
 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 稀盐酸 | 产生大量的气泡 | 猜想②正确 相关的化学方程式Na2CO3+2HCl═2NaCl+CO2↑+H2O |
| 把产生的气体通入 澄清的石灰水 | 产生白色沉淀 | 相关的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O |
分析 【交流讨论】根据酸、碱、盐的组成特点及标签可见部分,猜测该溶液不可能属于哪类物质的溶液;
【得出结论】根据溶液中溶质溶解度与饱和溶液中溶质的质量分数的关系,由常温下各物质的溶解度及该溶液中溶质质量分数,判断溶液的可能性;
【作出猜想】根据提示物质的可能性,对该溶液进行猜想;
【设计并实验】(1)根据三种物质溶液的酸碱性及所测定溶液的酸碱度,对溶液的可能做出判断;
(2)利用碳酸钠、氢氧化钠性质差异及所设计实验中的现象,判断所采取的鉴别所用试剂、现象及结论;
【拓展与应用】根据碳酸钠、氢氧化钠的性质差异,另选一种试剂完成两种物质的鉴别.
解答 解:【交流讨论】破损标签可见部分为钠元素,可判断该物质由金属元素与根组成,而酸类物质由氢元素与酸根所组成,可判断该物质不可能为酸;
【得出结论】根据常温下碳酸氢钠的溶液为9.6g,可判断常温下碳酸氢钠的饱和溶液的溶质质量分数=$\frac{9.6g}{9.6g+100g}$×100%=8.8%,因此可判断该溶液不可能为碳酸氢钠溶液;
【作出猜想】除碳酸氢钠外,该溶液可能为氯化钠、碳酸钠或氢氧化钠溶液;
【设计并实验】(1)由于氢氧化钠、碳酸钠溶液都为碱性,溶液pH都大于7,只有氯化钙溶液的pH=7,所以该瓶pH大于7的溶液不可能是氯化钠溶液;
(2)根据碳酸钠能与盐酸反应放出二氧化碳而氢氧化钠与盐酸反应无明显现象,因此,可推断鉴别两物质时所加入的试剂为稀盐酸,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,观察有气泡可说明该物质为碳酸钠,把产生气体通入澄清石灰水,石灰水会变浑浊,反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;
【拓展与应用】利用氢氧化钙能与碳酸钠反应生成白色碳酸钙沉淀,而与氢氧化钠不能反应而无明显现象,可使用氢氧化钙溶液鉴别NaOH溶液和Na2CO3溶液;
故答案为:
【交流讨论】A
【得出结论】NaHCO3
【作出猜想】NaOH
【设计并实验】
(1)NaCl;
(2)
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 稀盐酸 | Na2CO3+2HCl═2NaCl+CO2↑+H2O | |
| 澄清的石灰水 | 产生白色沉淀 | CO2+Ca(OH)2═CaCO3↓+H2O |
点评 本题综合利用了物质的组成、物质的溶解性、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.


 高中必刷题系列答案
高中必刷题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
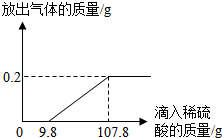 在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:
在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在“空气中氧气含量的测定”实验探究中,甲同学设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)
在“空气中氧气含量的测定”实验探究中,甲同学设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.(实验装置如图所示)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质发生化学变化时,一定不发生物理变化 | |
| B. | 物质有发光和放热的现象产生就一定是化学变化 | |
| C. | 物质发生化学变化后就一定有其它物质产生 | |
| D. | 化学变化中一定伴随着放热、发光、变色、放出气体、生成沉淀等现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com