
【题目】(5分)下列实验装置是初中化学实验室常用装置。根据你的实验操作体会和认识,回答下列问题:
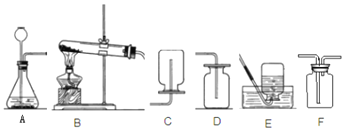
(1) 选择B与 组合成装置可制取干燥的氧气。
(2) 选B作制取气体的发生装置,应满足的条件是 。
(3)选A制取气体应满足的条件是 。
(4)若用F装置收集二氧化碳,从发生装置产生的二氧化碳应从F的___ _(填“左”或“右”)端通入,用来检验二氧化碳是否集滿的操作是 。
科目:初中化学 来源: 题型:
【题目】“低碳生活”、“低碳技术”的基本理念是节能减排。下列做法不符合“低碳”理念的是
A.用旧报纸制作铅笔杆 B.大力发展火力发电
C.垃圾回收处理后用于发电 D.城市公交车燃油改用天然气作燃料
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分)实验室有下列实验用品:①酒精灯、②试管夹、③10mL量筒、④100 mL量筒、 ⑤烧杯、⑥漏斗、⑦蒸发皿、⑧玻璃棒、⑨铁架台(带铁圈)、⑩滤纸、胶头滴管。请按要求选择相应实验用品填空(填序号):
(1)加热试管里的药品应使用 (填 2 种)
(2)量取5mL液体应使用 (填 2种)
(3)过滤操作中应使用 (填 5 种)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将60℃的硝酸钾溶液降温至20℃,有晶体析出.有关该过程的说法错误的是
A.60℃时的溶液一定是硝酸钾饱和溶液
B.20 摄氏度时的溶液一定是硝酸钾的饱和溶液
C.硝酸钾的溶解度随温度降低而减小
D.硝酸钾的晶体可采用降温结晶的方法得到
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】要从高锰酸钾加热完全分解后的剩余物中回收二氧化锰固体,有下列操作可选择:①过滤;②烘干;③加水溶解;④水洗;⑤蒸发结晶.其操作顺序正确的是
A.①→②→③→④ B.③→②→①→⑤ C.③→①→④→② D.③→①→⑤→④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验现象描述正确的是
A.木炭在氧气中燃烧,发出白光,放出大量的热
B.铁丝在空气中剧烈燃烧,放出大量的热,火星四射,生成黑色固体
C.红磷在氧气中剧烈燃烧,有黄色火焰,生成大量白色烟雾
D.硫在空气中燃烧,发出蓝紫色火焰,产生刺激性气味的气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(15分)制作糕点常用Na2CO3或NaHCO3作膨松剂,我校化学兴趣小组的同学根据Na2CO3和NaHCO3的性质进行了一系列探究。
【查阅资料】
(1)溶解度比较:
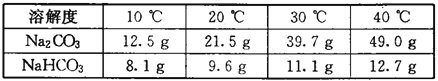
(2)已知碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解。
(3)常温下,浓度相同的Na2 CO3溶液比NaHCO3溶液的碱性强。
【探究一】NaHCO3和Na2CO溶解度差异的探究。
小方同学分别取xg两种固体粉末加入20℃10 g水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,x可能是_______。
A.2 B.0.96 C.0.5 D.3
【探究二】Na2CO3和NaHCO3鉴别探究
【猜想与假设】
(1)甲同学认为可用澄清石灰水鉴别Na2CO3和NaHCO3溶液.
(3)乙同学认为固体Na2CO3、NaHCO3可用加热的方法鉴别.
【实验探究】(1)甲同学在两支分别盛有少量Na2CO3、NaHCO3溶液的试管中,各加入澄清石灰水,观察到两支试管中的现象相同,均产生了白色沉淀,实验结果与猜想不一致,即不能用澄清石灰水鉴别Na2CO3和NaHCO3溶液.
(3)乙同学分别取了一定量的Na2CO3、NaHCO3固体于大试管中加热(如图所示):
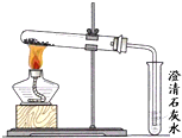
①加热Na2CO3时,开始即见小试管中有少量气泡产生,继续加热,气泡逐渐减少,未见澄清石灰水变浑浊,
②加热NaHCO3时,丙同学观察到实验现象与①不同,证实了自己的猜想是合理的.
【问题讨论】
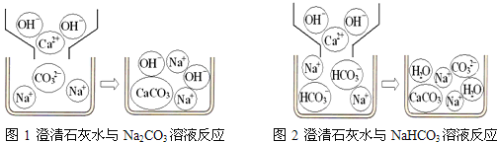
小组同学对上述实验展开了讨论,对甲同学的两个实验进行了比较,并从物质在溶液中解离出不同离子的微观角度分析了原因(如图1、图2).请写出Na2CO3与澄清石灰水发生反应的化学方程式________;写出NaHCO3与澄清石灰水混合时参与反应的离子:________.
【探究三】测定某Na2CO3和NaHCO3混合物中NaHCO3的质量分数
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为: ;
(2)实验中,需加热至恒重的目的是 。
[方案二]利用下图装置进行实验,装置B中放有样品(整套装置气密性良好,各装置中气体吸收剂足量)。
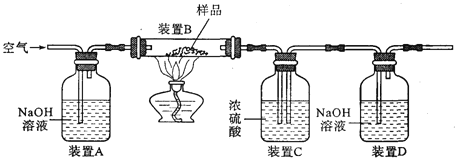
【实验步骤】
(1)检查装置的气密性;(2)称取样品10 g,加到装置B中;(3)称量装置B、C、D的质量(含药品);(4)连接装置;(5)加热;(6)停止加热继续通入空气;(7)再次称量装置B、C、D的质量(含药品)。
【数据记录】
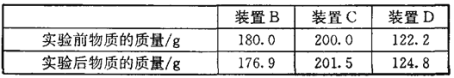
【问题回答】
①上图装置C的作用是_______,装置C中一个明显的错误是______________。
②实验过程中必须向装置内通入空气,装置A中发生反应的化学方程式为_______。若没有装置A,造成测定结果_______(填“偏大”“不变”或“偏小”)
【讨论分析】
小红同学认为,表格中三组数据都可以计算该样品中NaHCO3的质量分数,但小张认为不能用C装置的质量变化来计算,其理由是_______;改进方法:_______。小王又认为用装置D的质量差会偏大而影响计算,应增加一个操作:_______,目的是______________。
【数据处理】经过反复讨论,大家一致赞成应该利用表格中的装置B的质量变化进行计算NaHCO3和Na2CO3混合物中NaHCO3的质量分数 。
【拓展应用】固体Na2CO3中混有少量NaHCO3,可通过________方法除去.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com