
| A. | 甲醛是一种有机化合物 | |
| B. | 甲醛分子是由一个碳原子和一个水分子构成 | |
| C. | 一个甲醛分子中含有四个原子 | |
| D. | 甲醛中C、H、O三种元素的质量比为6:1:8 |
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:选择题
| A. | 除去CaO中混有的CaCO3,先加足量水,然后过滤 | |
| B. | 除去MnO2粉末中混有的KCl,先加足量水溶解、过滤,然后洗涤、干燥 | |
| C. | 用紫色石蕊试液鉴别稀盐酸和稀硫酸 | |
| D. | 用碘化钾检测食品中是否含有淀粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作 | 实验现象 | 原理或解释 | |
| 取 甲 酸 溶 于 水 | 滴加紫色石蕊 | 溶液变成红色 | 溶液中含氢离子 |
| 加适量的锌粒 | 观察到有气泡冒出 | 2HCOOH+Zn═(HCOO)2Zn+H2↑ | |
| 加氧化铁粉末 | 观察到红棕色固体消失,溶液变成黄色 | 甲酸可以与金属氧化物反应,工业上 可用甲酸除锈 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸 | B. | 盐 | C. | 碱 | D. | 氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
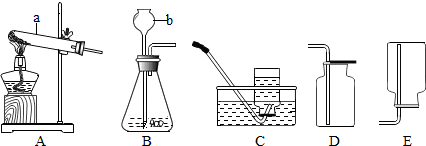
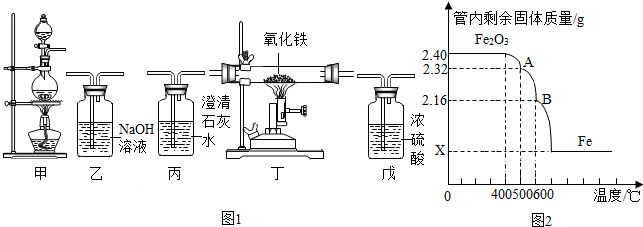
| 实验步骤 | 实验现象 | 实验结论 |
| 取少许剩余固体于试管中,加入一定量的稀盐酸(或稀硫酸),加热并观察现象. | ①试管内黑色固体逐渐消失,仍有红色固体存在. ②溶液由无色变成蓝色 | 小红的猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 名称 | 纯碱 | 3个硫原子 | 2个亚铁离子 | 正二价钡元素 | 乙醇 |
| 符号 | (1)Na2CO3 | (2)3S | (3)2Fe2+ | (4)$\stackrel{+2}{Ba}$ | (5)C2H5OH |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com