
分析 (1)根据碳酸盐的检验方法来分析;
(2)氧化钙能与水反应生成氢氧化钙;
(3)根据氯化铁能与铁反应生成氯化亚铁来进行分析;
(4)根据氧化钙与水反应放出热量进行分析.
解答 解:(1)为验证固体中 CaCO3是否存在,可取固体加稀盐酸,将产生的气体通入石灰水中,若观察到有气体产生,石灰水变浑浊,说明其中含有碳酸钙;故填:取固体加稀盐酸,将产生的气体通入石灰水中;有气体产生,石灰水变浑浊;
(2)因为氧化钙能与水反应生成氢氧化钙,此时滴加酚酞试液也会观察到溶液变红,所以此判断不正确;故填:不正确,因为也可能是氧化钙与水反应生成了碱--氢氧化钙.
(3)氧化铁与稀盐酸反应生成氯化铁和水,氯化铁与铁反应生成浅绿色的氯化亚铁溶液,所以看不到黄色;故填:不正确,氧化铁有可能存在.与盐酸反应生成的氯化铁又与铁反应变成了氯化亚铁,所以看不到黄色溶液.
(4)因为氧化钙与水反应生成氢氧化钙,并且会释放出大量的热,故可用此方法来进行检验,故填:把固体放入水中,若产生大量热说明有CaO.
点评 有关实验方案的设计是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法,本考点主要出现在实验题中.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
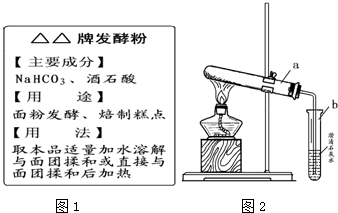
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
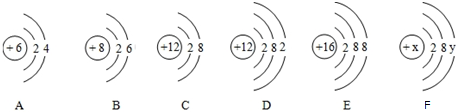
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
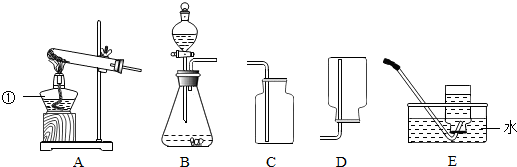
| 加入Na2CO3溶液的质量/克 | 20 | 40 | 60 | 80 | 100 |
| 生成沉淀的质量/克 | 0 | 1 | 3 | 4 | X |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定含碳、氢、氧元素 | B. | 一定含碳、氢元素,可能含氧元素 | ||
| C. | 只含碳、氢元素 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 根据如图中标签上信息填空:
根据如图中标签上信息填空:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
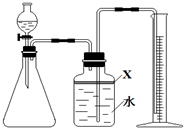 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.
氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域.某氮化铝中含有碳或氧化铝杂质,某化学研究性学习小组设计并完成了如下实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com