
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写;再根据反应特征确定反应类型.
解答 解:(1)硫是一种淡黄色粉末物质,在氧气中燃烧,发出明亮的蓝紫色火焰,反应的化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;该反应符合“多变一”的特征,属于化合反应.
(2)碳是一种黑色固体,在氧气中燃烧,其生成物二氧化碳可使澄清石灰水变浑浊,反应的化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;该反应符合“多变一”的特征,属于化合反应.
(3)铁是一种银白色金属丝,在氧气中剧烈燃烧,火星四射,生成四氧化三铁,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;该反应符合“多变一”的特征,属于化合反应.
(4)氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;该反应符合“一变多”的特征,属于分解反应.
故答案为:(1)S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;化合;(2)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;化合;(3)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;化合;(4)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;分解.
点评 本题难度不大,考查学生根据反应原理书写化学方程式、判定反应类型的能力,掌握化学方程式的书写方法(写、配、注、等)、四种基本反应类型的特征即可正确解答本题.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源: 题型:解答题
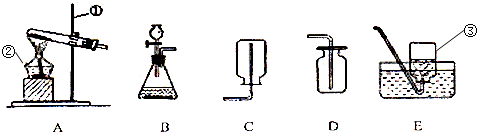
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
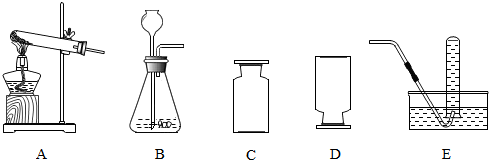
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
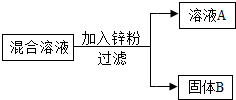 (1)R是银白色金属,将稀盐酸分别加入到盛有金属Fe、R、Cu的试管中,只有Cu表面无现象;将 FeSO4溶液中分别加入到盛有金属R、Cu的试管中,只有R表面有黑色物质析出,则金属H、Fe、R、Cu活动性由强到弱的顺序是R>Fe>H>Cu.
(1)R是银白色金属,将稀盐酸分别加入到盛有金属Fe、R、Cu的试管中,只有Cu表面无现象;将 FeSO4溶液中分别加入到盛有金属R、Cu的试管中,只有R表面有黑色物质析出,则金属H、Fe、R、Cu活动性由强到弱的顺序是R>Fe>H>Cu.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 需区分的物质 | 方法一 | 方法二 |
| A | 黄铜和黄金 | 比较硬度 | 看外观 |
| B | 铁粉和木炭粉 | 加入稀盐酸 | 用磁铁吸引 |
| C | 二氧化碳和氮气 | 取样品闻气味 | 观察颜色 |
| D | 水和酒精 | 闻气味 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
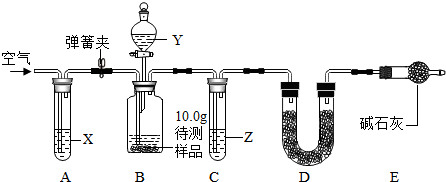
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入CaCl2溶液 | 有白色沉淀产生 | 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体过滤,取滤液于另一支试管中,滴加无色酚酞试液 | 酚酞试液变红 | 该氢氧化钠溶液已部分变质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com