
【题目】实验室使用块状石灰石(杂质不溶于水且不和水反应)和稀盐酸制取CO2,当观察不到有气泡产生,固体仍有剩余时,通常认为反应结束,剩余液呈中性,某兴趣小组对此进行了以下探究:
(实验操作)
(1)向试管中加入5粒石灰石,倾倒约试管容积1/3的稀盐酸(1:1);观察不到气泡后,仍有固体剩余;将试管静置。
(2)取上层清液,用pH试纸测得溶液pH=2,说明溶液显酸性
(提出问题Ⅰ)
反应后剩余溶液中有哪些物质?其中能使溶液pH=2的有哪些?
(实验探究Ⅰ)
(1)甲同学通过实验排除了CaCl2的可能性,简述其实验方案_____。
(2)乙同学将CO2通入蒸馏水中至饱和,测得pH>5。
(3)综合甲、乙两同学实验得出的结论是:剩余液中还含有_____。
(提出问题Ⅱ)
试管中剩余固体是否仍含有CaCO3?
(实验探究Ⅱ)
小组同学向试管中继续加入稀盐酸(1:1),又有大量气泡产生。
(1)由此得出的结论是剩余固体中含有CaCO3;发生反应的化学方程式是_____。
(2)比较稀盐酸加入前后的实验现象,解释“又有大量气泡产生”的原因是_____。
(拓展延伸)
(1)反应剩余液放置一段时间后,溶液pH增大,其主要原因是_____。
(2)假如用100g 14.6%的稀盐酸和足量的石灰石反应,看不到气泡产生时,停止收集气体,收集到的CO2质量_____(填“大于”、“小于”或“等于”)8.8g。
【答案】取CaCl2固体溶于水,测其溶液的pH 盐酸 ![]() 盐酸浓度增大,又与碳酸钙反应 碳酸钙与盐酸继续反应或剩余碳酸钙又消耗盐酸,使其浓度减小(合理答案均可) 小于
盐酸浓度增大,又与碳酸钙反应 碳酸钙与盐酸继续反应或剩余碳酸钙又消耗盐酸,使其浓度减小(合理答案均可) 小于
【解析】
本题通过分析反应剩余物质成分,可以得出反应物浓度对反应的影响。
(1)测定CaCl2溶液的的酸碱度,实验方案为取CaCl2固体溶于水,测其溶液的pH,且=7。
(2)综合甲、乙两同学实验得出的结论是氯化钙溶液和二氧化碳水溶液的pH不可能等于2,所以剩余液中还含有盐酸。
(3)再向剩余固体滴加稀盐酸,又有大量气泡产生,发生反应的化学方程式是![]() 。
。
(4)比较稀盐酸加入前后的实验现象,解释“又有大量气泡产生”的原因是盐酸浓度增大,又与碳酸钙反应。
(5)反应剩余液放置一段时间后,碳酸钙与盐酸继续反应,盐酸越来越少,浓度减小,溶液pH增大。
(6)解:设100g 14.6%的稀盐酸完全反应,生成二氧化碳的质量为X。

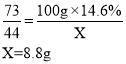
当稀盐酸和足量的石灰石反应时,盐酸的浓度降低至一定浓度时反应会停止,但盐酸没有完全参与反应,收集到的气体小于理论值,所以看不到气泡产生时,停止收集气体,收集到的CO2质量小于8.8g。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图是某实验小组将等质量、等质量分数的氢氧化钡溶液和稀盐酸充分混合过程中利用数字传感器测定的溶液pH曲线。
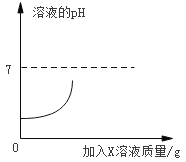
(1)写出上述反应的化学方程式_____。
(2)根据图示推测X的化学式_____。
(3)上述反应完全后,写出所得溶液与稀硫酸、硝酸银、硫酸铜、铜、铁五种物质中不能反应的物质名称并简述原因_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小强同学前往当地的石灰石矿区进行调查,他取回了若干块石灰石样品,对样品中碳酸钙的质量分数进行检测,采用如下方法:取8g这种石灰石样品,把40g稀盐酸分4次加入,测量过程所得数据如下表所示(已知石灰石样品中含的杂质不溶于水,也不与稀盐酸反应)。
序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
第1次 | 10 | 5.5 |
第2次 | 10 | M |
第3次 | 10 | 1.2 |
第4次 | 10 | 1.2 |
请计算:
(1)样品中碳酸钙的质量分数为________________________________;
(2)表中m的数值应为______________________________;
(3)所加稀盐酸的溶质质量分数________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气在中学化学中有着举足轻重的地位,根据下列实验装置图回答问题:
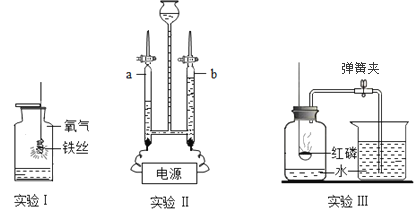
(1)实验Ⅰ中化学反应的现象为:铁丝剧烈燃烧,_____,产生一种黑色固体。
(2)实验Ⅱ中电解水制取氧气反应的化学方程式为_____,与电源负极相连的玻璃管内生成的气体是_____(填“氢气”或“氧气”)。
(3)实验Ⅲ是测定空气中氧气含量的实验,在瓶内加少量水并将水面上方空间分为5等份,接下来的实验步骤依次为_____(填序号),最后打开弹簧夹。
①冷却到室温
②弹簧夹夹紧橡皮管
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容。
(1)碳的单质主要有金刚石和石墨,两种物质物理性质差异较大的原因是_____。
(2)图1是元素周期表中的一格,写出一条你从中获取的信息_____。
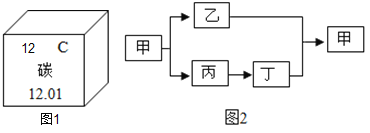
(3)甲、乙、丙、丁是初中化学常见的化合物,甲和乙中含有碳元素,丙能做干燥剂。它们之间有如图2所示的转化关系(部分物质和反应条件已略去)请写出丁的一种用途_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如何合理、高效、节约地使用煤、石油、天然气这三大当今世界最主要的化石燃料,加紧开发、研制其他清洁能源是全人类面临的共同课题,是发展低碳经济的当务之急。回答下列问题:

(1)天然气是乐山城市家庭的主要生活燃料。为防止因天然气泄漏造成危险,可在家中安装报警器,在甲、乙两图中,安装位置正确的是______。写出天然气燃烧的化学方程式:______。
(2)如直接用煤作家用燃料既污染空气又浪费能源。煤燃烧时产生的______是形成酸雨的主要气体之一。煤的气化是把煤变为清洁能源的重要一环,其中一个重要反应是: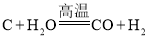 ,该反应的基本类型是______。
,该反应的基本类型是______。
(3)我国自主研发的一种电动汽车使用的能源是新型锂电池,从化学角度看,与使用汽油的汽车相比,其优点是______(举出一点即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】回答下列有关实验基本操作和设计的问题。
A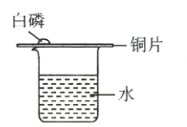 B
B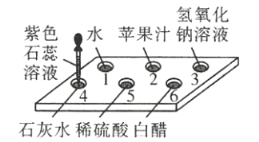
C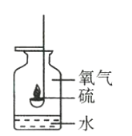 D
D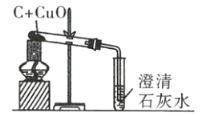
(1)![]() 图中,向烧杯内加入适量的______(填序号),可能引燃铜片上的白磷。
图中,向烧杯内加入适量的______(填序号),可能引燃铜片上的白磷。
A 生石灰 B 硝酸铵 C 氢氧化钠
(2)![]() 图是探究紫色石蕊变色规律的实验,往点滴板1~6号的孔穴中先加入如图所示的试剂,再分别滴入2滴紫色石蕊溶液。其中作为空白对照实验的是孔穴______(填孔穴编号)。
图是探究紫色石蕊变色规律的实验,往点滴板1~6号的孔穴中先加入如图所示的试剂,再分别滴入2滴紫色石蕊溶液。其中作为空白对照实验的是孔穴______(填孔穴编号)。
(3)![]() 图中集气瓶内水的作用是__________。
图中集气瓶内水的作用是__________。
(4)![]() 图中的化学方程式为__________。
图中的化学方程式为__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的实验图示回答问题。
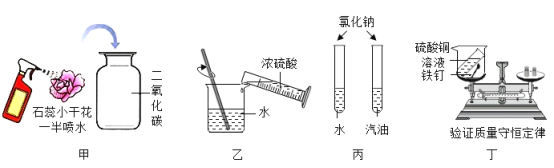
(1)甲实验:是验证二氧化碳与水反应的实验,其中的花朵是用石蕊溶液染成的紫色干燥纸花。把石蕊小干花一半喷水后放入盛满二氧化碳的集气瓶中,观察到的现象是_________;
(2)乙实验:稀释浓硫酸时,玻璃棒的作用_________;
(3)丙实验:是一组对比实验,实验目的是_________;
(4)丁实验:实验能充分证明质量守恒定律的现象是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com