
【题目】请根据下列装置图,回答有关问题:

(1)写出图中标号仪器的名称:①__________;
(2)实验室用高锰酸钾制氧气,发生装置应选____,实验时,需对该装置做一点改动_。写出用高锰酸钾制氧气的化学方程式___________________;若用F 装置收集氧气,如何验满?______________________________________________
(3)用C装置代替B装置制取氢气的优点是_______________;写出实验室制氢气的化学方程式 _______________________________;
(4)亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3。下图为制取少量NH3的装置(制取H2的装置已略去)。
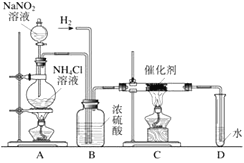
①C装置的硬质试管中发生反应的化学方程式为________________________。
②反应时N2和H2的最佳质量比是_________。如果按此比例进行反应,反应时,若D中导管口有气泡逸出,(已知NH3极易溶于水),说明逸出气泡的原因__________________。
③用实验方法证明确实有NH3生成: ________________________________。
【答案】长颈漏斗 A 在试管口放一团棉花 2KMnO4![]() K2MnO4 + MnO2 + O2↑ 在b端管口放一根带火星的木条,木条复燃,证明氧气满了 可以控制反应的发生和停止 Zn+H2SO4=ZnSO4+H2↑ N2+3H2
K2MnO4 + MnO2 + O2↑ 在b端管口放一根带火星的木条,木条复燃,证明氧气满了 可以控制反应的发生和停止 Zn+H2SO4=ZnSO4+H2↑ N2+3H2 ![]() 2NH3 14:3 氮气和氢气部分化合,仍会有未反应的H2和N2逸出 把湿润的红色石蕊试纸放在导管口,红色变蓝色,证明生成氨气
2NH3 14:3 氮气和氢气部分化合,仍会有未反应的H2和N2逸出 把湿润的红色石蕊试纸放在导管口,红色变蓝色,证明生成氨气
【解析】
(1)图中标号仪器的名称为:长颈漏斗;
(2)用高锰酸钾制氧气时,反应物的状态是固体,反应条件是加热,发生装置应选A;为防止高锰酸钾进入导气管,需在试管口放一团棉花,对该装置做一点改动是在试管口放一团棉花;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4![]() K2MnO4 + MnO2 + O2↑;氧气的密度大于空气,若用F装置收集氧气,气体需从a管通入,氧气具有助燃性,能使带火星的木条复燃。氧气验满的方法是:在b端管口放一根带火星的木条,木条复燃,证明氧气满了;
K2MnO4 + MnO2 + O2↑;氧气的密度大于空气,若用F装置收集氧气,气体需从a管通入,氧气具有助燃性,能使带火星的木条复燃。氧气验满的方法是:在b端管口放一根带火星的木条,木条复燃,证明氧气满了;
(3)在装置C中,固体药品物放在多孔隔板上,液体药品从长颈漏斗中加入。关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止,打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行。用C装置代替B装置制取氢气的优点是:可以控制反应的发生和停止;锌和硫酸反应生成硫酸锌和氢气反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(4)①N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3,反应的化学方程式为:N2+3H2 ![]() 2NH3;
2NH3;
②根据化学方程式N2+3H2 ![]() 2NH3可知,反应时N2和H2的最佳质量比=28:6=14:3,若D中导管口有气泡逸出,是因为氮气和氢气部分化合,仍会有未反应的H2和N2逸出;
2NH3可知,反应时N2和H2的最佳质量比=28:6=14:3,若D中导管口有气泡逸出,是因为氮气和氢气部分化合,仍会有未反应的H2和N2逸出;
③氨气溶于水呈碱性,红色石蕊试纸遇碱性物质变蓝色。用实验方法证明确实有NH3生成:把湿润的红色石蕊试纸放在导管口,红色变蓝色,证明生成氨气。


科目:初中化学 来源: 题型:
【题目】欲配制50g质量分数为15%的NaCl溶液,下图是某同学配制溶液的操作过程:
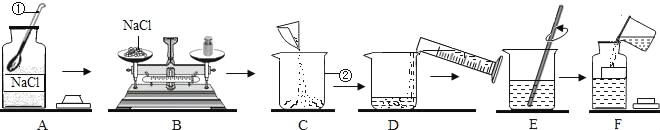
(1)写出标号仪器的名称:①_____,②_____。
(2)B操作中应称NaCl的质量是_____g.若称量时错把氯化钠放到了右盘(1g以下用游码),其他过程没有误差,则实际配制的NaCl溶液的溶质质量分数是_____。
(3)所需量取水的体积为_____(水的密度为lg/cm3),量筒的规格应为_____(填“10mL”或“50mL”)。
(4)D操作时有少量水溅出,可能导致溶质质量分数_____,F操作中溶液洒落可能导致溶质质量分数_____(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】写出下列反应的化学方程式,并在括号内注明基本反应类型:
(1)磷在空气中燃烧 ( )
(2)用氢氧化镁治疗胃酸过多 ( )
(3)硅是信息技术的关键材料。高温下氢气与四氯化硅(SiCl4)反应可制得高纯度的硅,同时生成氯化氢。该反应的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
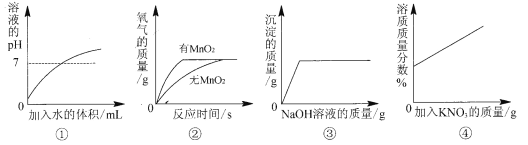
A.图①表示向稀盐酸中不断加水
B.图②表示探究过氧化氢制氧气的反应中二氧化锰的作用
C.图③表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液
D.图④表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液是生产生活中常见的物质,依据相关信息回答问题:
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(1)农业上,硝酸钾用作水溶性肥料,硝酸钾溶液中的溶质是_____。
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。
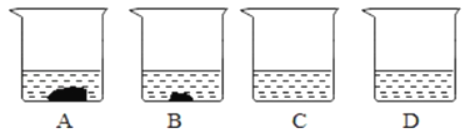
①_____(填字母序号)中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为_____g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是_____(填字母序号)。
A 溶剂质量可能相等 B 溶质质量可能相等
C 溶质质量分数可能有相等的 D 烧杯A中的溶液质量分数可能最大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液在日常生活,工农业生产和科学研究中具有广泛的用途.
(1)盛放过碘的汽油溶液的试管内壁往往粘有大量的植物油,可以使用洗涤剂进行清洗,这利用了________原理.
(2)在盛有水的烧杯中加入以下某种物质,形成溶液的过程中温度上升,这种物质是_______(填字母)
A 氯化钠 B 硝酸铵 C 氢氧化钠
(3)某同学在实验室用氯化钠固体和蒸馏水配制50g质量分数为6%的氯化钠溶液时,涉及以下实验步骤:①溶解②称量和量取③计算④装入试剂瓶并贴好标签,配制该溶液正确的实验步骤顺序是________(填序号),若配置该溶液的过程中,对量筒进行俯视读数,则结果将会________(填“偏大”、“不变”或“偏大”).
(4)某注射用药液的配制方法如下:
①把1.0g药品溶于水配制成4.0mL溶液a;
②取0.4mL溶液a,加水稀释至1.0mL,得溶液b.
由于在配制过程中药液很稀,其密度都可近似看做1g/cm3,则最终得到的药液(溶液b)中溶质的质量分数为________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
肼(N2H4)又称联氨,有类似于氨的刺鼻气味,贮存时用氮气保护并密封,用途广泛。肼燃烧放热量大且燃烧产物对环境无污染,常用作火箭燃料点燃时与助燃物质液态N2O4发生反应,生成N2和H2O。高压锅炉水处理时用于脱除氧气以防止锅炉的腐蚀,也可以把锅炉内表面锈蚀后的氧化铁还原为结构紧密的四氧化三铁保护层,减缓锅炉锈蚀。用于烟草、土豆、玉米的贮藏用于食用盐酸的制造等。熔点1.4℃,沸点113.5℃;有强烈的吸水性,形成水合肼(N2H4·H2O),可以用固体烧碱进行脱水;能吸收空气中的二氧化碳;易溶于水;与液氧接触能自燃;长期暴露在空气中或短时间受热时易发生分解。对眼睛有刺激作用,能引起延迟性发炎,对皮肤和粘膜也有强烈的腐蚀作用。
依据短文内容,回答下列问题
(1)肼的下列性质中,属于化学性质的是_________(填字母序号,下同)。
A.与氧化铁作用 B.易溶于水 C.易分解 D.有刺鼻的气味
(2)肼在常温下为_________ (填“固态”“液态”或“气态”)。
(3)肼作为火箭燃料燃烧时反应的化学方程式为__________________。
(4)肼有强烈的吸水性能吸收空气中的CO2,下列物质中的_________也具有这些性质。
A NaCl B.Ca( OH)2 C NaOH D NaHCO3
(5)肼需要密封保存的原因是①有强烈的吸水性;②能吸收空气中的二氧化碳;③__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】质量守恒定律的定量研究对化学科学发展具有重大意义。
(1)下图为某化学反应的微观模拟图,“○”和“●”分别表示两种不同的原子:
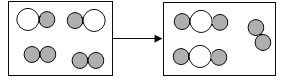
由“![]() ”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的两种反应物的分子个数比为 _____,此反应的基本反应类型为______。请写出一个符合上述反应的化学方程式_____。
”聚集成的物质______(填“可能”或“不可能”)是氧化物,参加反应的两种反应物的分子个数比为 _____,此反应的基本反应类型为______。请写出一个符合上述反应的化学方程式_____。
(2)已知m1g镁条放在空气中完全燃烧,生成m2g氧化镁(不考虑其它反应),则m1______m2。 小西在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1>m2,其原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com