
【题目】在托盘天平两边各放一只等质量的烧杯,调节至平衡,在两只烧杯里分别加入同体积同质量分数的稀盐酸,然后向左右两烧杯中分别加入质量相等的碳酸钙和碳酸钠。待充分反应后碳酸钠有剩余,则还可观察到的现象是( )
A. 天平指针最终偏向放碳酸钙的烧杯一边B. 天平指针最终偏向放碳酸钠的烧杯一边
C. 天平平衡D. 左边烧杯中碳酸钙有剩余
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题:

(1)_____℃时,a、c两物质的溶解度相等.
(2)若使a、c的饱和溶液同时析出晶体,方法是_____.
(3)在t2℃时,a、b、c三种饱和溶液降温至t1℃时溶质的质量分数由大到小的顺序是_____,析出晶体最多的是_____.(填“a”、“b”或“无法确定”)
(4)在t2℃时,将150克a的饱和溶液稀释成质量分数为20%的溶液需加水_____克.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从海水中制备碳酸钠和金属镁的流程如下图所示;
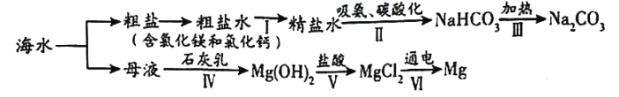
下列说法错误的是
A. 流程I依次向粗盐水中加入过量Ca(OH)2溶液、过量Na2CO3溶液和适量稀盐酸得到精盐水
B. 流程Ⅱ吸氨的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出碳酸氢钠的的固体
C. 上述流程涉及到三种基本反应类型
D. 流程IV、V是通过化学方法是将母液中的氯化镁富集起来,提纯氯化镁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学与生活密切相关.请回答下列问题.
(1)成语“釜底抽薪”运用的灭火原理是_____.
(2)饮食均衡,身体才能健康.食用蔬菜、水果能获取的基本营养素主要是_____.
(3)氢气是最清洁的能源,其原因是_____(用化学方程式表示).
(4)生活中服用含Al(OH)3的药丸治疗胃酸过多症的原理:_____(用化学方程式表示).
(5)智能手机是一种多功能通讯工具,一款智能手机通常含有41种以上化学元素.请回答:
①大部分手机外壳是用塑料或镁合金制成,二者中属于有机合成高分子材料的是_____.
②手机线路的主要原料是铜,微电子材料还用到金、银、钽等,在此主要利用了铜的_____性.③手机屏幕大部分用的是硅酸铝玻璃,下列关于硅酸铝玻璃性质的推测不正确的是_____(填序号).
①透光性好②常温下不易与氧气反应③易溶于水
(6)家庭常用的“84消毒液”中的主要成分是次氯酸钠(NaClO),次氯酸钠中氯元素的化合价是_____.
A ﹣1 B +1 C +3 D +5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的( )
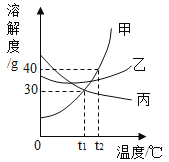
A. ![]() 时,甲、丙溶液中溶质质量分数相同
时,甲、丙溶液中溶质质量分数相同
B. 升温可使丙物质的不饱和溶液变成饱和溶液
C. ![]() 时,等质量甲、乙、丙的饱和溶液中溶剂的质量:甲
时,等质量甲、乙、丙的饱和溶液中溶剂的质量:甲![]() 乙
乙![]() 丙
丙
D. 分别将甲、乙、丙三种物质![]() 的饱和溶液降温到
的饱和溶液降温到![]() ,所得溶液溶质的质量分数:乙
,所得溶液溶质的质量分数:乙![]() 甲
甲![]() 丙
丙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了回收硝酸亚铁和硝酸银的混合溶液中的银,设计了如下的实验方案:
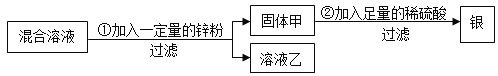
(1)若溶液乙为无色溶液,则固体甲一定有的物质是______,可能有的物是______,步骤②中肯定发生的反应的化学方程式为______。
(2)若溶液乙为浅绿色溶液,请设计实验证明滤液的成分:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学取8gZnO、Al2O3、Cu的混合固体,与73g20%的稀盐酸混合后恰好完全反应,则该混合固体中金属元素的百分含量为
A. 70%B. 40%C. 30%D. 60%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读短文后回答下列问题。
燃料电池(Fuelcell),是一种使用燃料进行化学反应产生电能的装置,最早于1839年由英国的Grove发明。燃料的选择性非常多,包括纯氢气(H2)、甲醇(CH3OH)、乙醇(CH3CH2OH)、天然气,甚至于现在运用最广泛的汽油,都可以作为燃料电池的燃料。这是目前其他所有动力来源无法做到的。而以燃料电池做为汽车的动力,已被公认是二十一世纪必然的趋势。2017年,我国共有8个品牌的10款车型燃料电池汽车在产,总产量为1272辆,2018年国产燃料电池汽车已经超过3000辆。
燃料电池是以特殊催化剂作电极使燃料与氧气发生反应,生成二氧化碳和水。因其不需推动涡轮等发电器具,也不需将水加热至水蒸气再经散热变回水,所以能量转换效率高达70%左右,足足比一般发电方法高出了约40%;优点还不只如此,其二氧化碳排放量比一般方法低许多,且水又是无害的生成物,所以燃料电池是一种高效、低污染装置。
燃料电池主要由正极、负极、电解质溶液和外部电路4部分组成,其正极和负极分别通入燃料气和氧气(空气),负极上燃料气放出电子,外电路传导电子到正极并与氧气结合生成离子,在电场作用下,离子通过电解质转移到负极上再与燃料气进行反应,最后形成回路产生电能。与此同时,因为燃料自身的反应及电池存在的内阻,燃料电池也要排出一定的热量,以保持电池恒定的工作温度。右图是甲烷燃料电池的工作原理示意图。
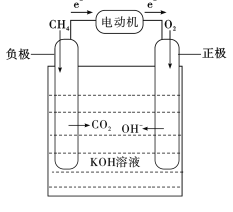
(1)燃料电池是将_________能转化为电能的装置。
(2)下列说法错误的是_________。
A 化学反应放出的能量可以是光能、热能、电能等
B 燃料电池可以广泛用于新能源汽车。
C 氢燃料电池汽车所需要的H2可电解水生成。
D 燃料电池都要排放CO2气体
(3)写出甲醇完全燃烧的化学方程式_________。
(4)甲烷燃料电池释放能量的总反应化学方程式是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电解水的实验装置如图所示,根据图回答:
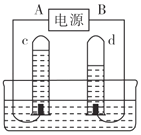
(1)电源中A电极是电源的_____(填“正”或“负”)极。
(2)若收集到c气体22.4 mL,则理论上应收集到d气体大约是_____mL。
(3)电解水时的最小粒子是_____。
(4)电解水反应的化学方程式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com