
科目: 来源: 题型:
【题目】实验室用铜和硫酸制取CuSO4有下列几种做法:
(1)甲学生进行了下列实验:取6.4g铜片和10mL某浓度的浓硫酸放在圆底烧瓶中共热,发现溶液慢慢变成蓝色,同时有刺激性气味气体生成。写出反应的化学方程式_____;直到反应完毕,最后发现烧瓶中还有铜片剩余。他根据自己所学的化学知识,认为烧瓶中还有较多的硫酸剩余。他这样认为的理由是:_____。
(2)乙同学认为甲设计的实验方案不好,他自己设计的思路是第一步:![]() 第二步:_____。对比甲的方案,乙同学的优点是_____、_____。
第二步:_____。对比甲的方案,乙同学的优点是_____、_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是_____;
(2)由粮食发酵获得X的化学变化过程中,最主要的两个反应是①粮食中淀粉在酶的作用下水解成葡萄糖②葡萄糖催化分解成X物质和另一种氧化物。写出反应化学方程式是:_____,_____;
(3)X可以和金属钠发生置换反应放出氢气,反应的化学方程式是_____;
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E分别是初中化学常见的五种不同类别的物质,其中B的固体和E的浓溶液常用作实验室的干燥剂。F是常见的一种红棕色物质。它们之间存在如图所示的关系(图中“—”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出)。下列说法错误的是( )
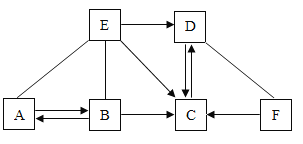
A.A物质可能是碳酸钠或者碳酸氢钠
B.C物质一定条件下也可以转化为B物质或E物质
C.F转化为C不一定是置换反应
D.图中一共11个反应,至少有4个反应为复分解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可利用黄铁矿(主要成分是Fe2S)煅烧的产物冶炼铁和生产硫酸,其反应方程如下:
① ②
②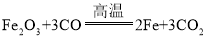 ③
③ ④
④![]()
下列说法不正确的是( )
A.反应①②③均有元素化合价发生变化
B.反应①②不属于四种基本反应类型中的任何一种,反应③④属于化合反应
C.将100g蒸馏水加入100g98%的浓硫酸中,可配制200g质量分数为49%的稀硫酸
D.将5gSO3溶于95g水形成溶液,其溶液中溶质的质量分数大于5%
查看答案和解析>>
科目: 来源: 题型:
【题目】已知铜、铁均能与FeCl3溶液反应,![]() ,
,![]() 。现将铜、铁混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,有关烧杯中物质组成的说法正确的是( )
。现将铜、铁混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,有关烧杯中物质组成的说法正确的是( )
A.溶液中一定含有FeCl3,固定一定有Cu,可能有Fe
B.溶液中一定含有FeCl2,固体一定含Cu
C.溶液中一定含有FeCl2、CuCl2,固体一定含有Cu
D.溶液一定含有FeCl2,固体一定是Fe和Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】如图利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,将产生氨气。立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
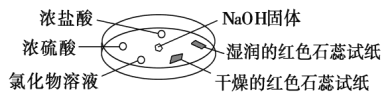
选项 | 实验现象 | 解释 |
① | 浓盐酸附近产生白烟 | NH3与HCl反应生成了NH4Cl固体 |
② | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
③ | 氯化物溶液中有红褐色沉淀 | 该溶液一定有FeCl3溶液 |
④ | 干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
A.②③④
B.①③④
C.①③
D.③④
查看答案和解析>>
科目: 来源: 题型:
【题目】M、N两种物质的溶解度曲线如图所示。t2℃时往一杯100g水中加入质量都是ag的M和N两种物质(假设两种物质的溶解性互不影响),制成混合物。将该混合物的温度降低到tl℃,下列说法正确的是( )
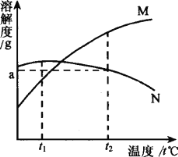
A.t2℃温度下,得到的溶液中溶质M、N的质量分数都为a%
B.温度降低到t1℃时,溶液中两种物质均饱和
C.如果温度升高,溶液中将析出N的晶体,溶质M的质量分数保持不变,溶质N的质量分数将减小
D.温度降到t1℃时,溶液中N的质量分数大于M的质量分数
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质间不能通过一步反应就能实现如图转化的是( )
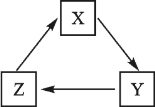
X | Y | Z | |
A | H2SO4 | HCl | H2O |
B | CuSO4 | CuCl2 | Cu(OH)2 |
C | CaCO3 | CO2 | K2CO3 |
D | Ca(OH)2 | NaOH | Mg(OH)2 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学利用锌、氧化铜和稀硫酸制取铜,他设计了两套方案,方案Ⅰ:利用锌与足量稀硫酸反应制氢气,氢气还原氧化铜;方案Ⅱ:氧化铜溶于稀硫酸生成硫酸铜,然后用锌与硫酸铜反应制备铜。下列关于方案Ⅰ和Ⅱ的评价不正确的是( )
A.方案Ⅱ比方案Ⅰ操作简便
B.等质量的锌,相同条件下在方案Ⅰ和方案Ⅱ中制得的铜的质量相同
C.等质量的H2SO4参加反应,方案Ⅰ制取铜的质量比方案Ⅱ的少
D.为了加快锌与稀硫酸反应,可以在溶液中加入少量氧化铜
查看答案和解析>>
科目: 来源: 题型:
【题目】将质量为m的氧化铜粉末加入到100g14%的稀硫酸中,微热至氧化铜全部溶解,再向该蓝色溶液中加入10g铁粉,充分反应后,过滤,得滤液和5.2g滤渣。求:
(1)氧化铜的质量m的值。
(2)最后得到的滤液中溶质的质量分数。(最后结果精确到0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com