
【题目】氧硫化碳(COS,结构类似于CO2)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。有多种方法可以脱氧硫化碳中的硫,其中氢解和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g) +H2(g)![]() H2S(g) + CO(g) ΔH1= +7kJ/mol
H2S(g) + CO(g) ΔH1= +7kJ/mol
②水解反应:COS(g) +H2O(g)![]() H2S(g) +CO2(g) ΔH2=-35kJ/mol
H2S(g) +CO2(g) ΔH2=-35kJ/mol
请回答下列问题:
(1)氧硫化碳的电子式为_____。
(2)CO和H2O(g)能反应生成CO2和H2,写出该反应的热化学方程式_______。
(3)水解反应达到平衡后,若减小容器的体积,逆反应速率将_____(填增大、减少或不变,下同),COS的转化率____。
(4)某温度下,体积为2L的恒容体系中,物质的量分别为mmol、nmol的COS蒸气和H2气发生氢解,已知COS的转化率为α,则该温度下的平衡常数K= ____(用m、n、α等符号表示)。
(5)某科研小组研究改进催化剂TiO2/Al2O3和温度对COS水解的影响,得到如图

COS水解的最佳温度是________;理由是___________。
【答案】![]() CO(g)+H2O(g)
CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-42kJ/mol 增大 不变 m α2 /(1-α)(n-mα) 300℃ 催化剂活性高,转化率很大
CO2(g)+H2(g) △H=-42kJ/mol 增大 不变 m α2 /(1-α)(n-mα) 300℃ 催化剂活性高,转化率很大
【解析】
(1)氧硫化碳是共价化合物,碳原子分别与氧原子、硫原子之间形成2个共用电子对;
(2)根据盖斯定律计算可得;
(3)平衡后减小容器体积,容器中压强增大,增大压强,正、逆反应速率都增大,平衡不移动;
(4)依据题意建立三段式,依据平衡常数公式计算;
(5)由图中信息分析300℃时COS的转化率最高,催化剂的活性最强。
(1)氧硫化碳是共价化合物,碳原子分别与氧原子、硫原子之间形成2个共用电子对,其电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)根据盖斯定律,②-①得CO(g)+H2O(g)![]() H2(g)+CO2(g),则△H3=△H2-△H1=(-35kJmol-1)-(+7kJmol-1)=-42kJmol-1,故答案为:CO(g)+H2O(g)
H2(g)+CO2(g),则△H3=△H2-△H1=(-35kJmol-1)-(+7kJmol-1)=-42kJmol-1,故答案为:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-42kJmol-1;
CO2(g)+H2(g)△H=-42kJmol-1;
(3)平衡后减小容器体积,容器中压强增大,增大压强,正、逆反应速率都增大;该反应是气体体积不变的反应,增大压强,平衡不移动,COS的转化率不变,故答案为:增大;不变;
(4)假设反应容器体积为VL,COS起始物质的量为m,转化率为a,则变化量为ma,则依据题意建立如下三段式:
COS(g)+H2(g)![]() H2S(g)+CO(g)
H2S(g)+CO(g)
起始(mol)m n 0 0
转化(mol)ma ma ma ma
平衡(mol)m(1-a) n-ma ma ma
则平衡常数K=![]() =
= =
=![]() ,故答案为:
,故答案为:![]() ;
;
(5)由图中信息分析300℃时COS的转化率最高,催化剂的活性最强,则COS水解的最佳温度是300℃,此时催化剂活性高,转化率很大,故答案为:300℃;催化剂活性高,转化率很大。


科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是
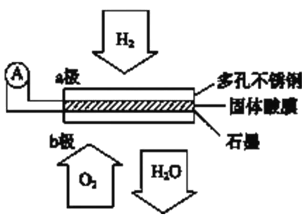
A. 电子通过外电路从b极流向a极
B. b极上的电极反应式为:O2+2H2O+4e--=4OH--
C. 每转移0.1mol电子,消耗1.12L的H2
D. H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见反应的化学方程式有A+B→X+Y+H2O或H2O+A+B→X+Y(未配平,反应条件略去),下列问题所涉及反应是上述两个方程式之一。请回答:
(1)常温下,若A为黄绿色气体,B为非金属氧化物,A、B均能使品红溶液褪色,A+B+H2O→X+Y,则该反应的化学方程式_________________
(2)若A为金属单质,其与B的浓溶液常温钝化而加热则可以反应,而且所得的三种产物在常温下又可以发生反应,则作氧化剂的B与表现酸性的B的物质的量之比是_____。
(3)若A为常见的非金属单质,B的溶液为某浓酸,其中A、B的物质的量之比为1∶4,而且该反应能产生一种造成光化学烟雾的气体,则该反应化学方程式为_______________
(4)若A、B均为化合物,Y为白色沉淀(不含金属元素),B为引起温室效应的主要气体,写出B(过量)与A反应生成Y的离子方程式________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池在净化废水的同时能获得能源或得到有价值的化学产品,左图为其工作原理,右图为废水中Cr2O72-离子浓度与去除率的关系。下列说法不正确的是
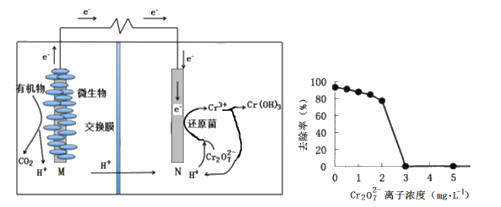
A. 有机物被氧化,M为电源负极
B. 电池工作时,N极附近溶液pH增大
C. Cr2O72-离子浓度较大时,可能会造成还原菌失活
D. 处理0.1 mol Cr2O72-时有1.4 mol H+从交换膜左侧向右侧迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用NaOH溶液滴定H2C2O4溶液,溶液中-lg[c(H+)/c(H2C2O4)]和-lgc(HC2O4-)或-lg[c(H+)/c(HC2O4-)]和-lgc(C2O42-)关系如图所示,下列说法错误的是( )
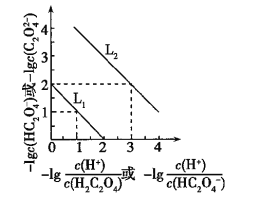
A. Ka1(H2C2O4)=1×10-2
B. 滴定过程中,当pH=5时,C(Na+)-3C(HC2O4-)>0
C. 向1 mol/L的H2C2O4溶液中加入等体积等浓度的NaOH溶液,完全反应后显酸性
D. 向0.1 mol/L的H2C2O4溶液中加水稀释,C(HC2O4-)/C(H2C2O4)比值将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由NO2、O2、熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )
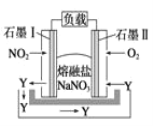
A. 石墨Ⅰ极为正极,石墨Ⅱ极为负极
B. Y的化学式可能为NO
C. 石墨Ⅰ极的电极反应式为NO2+NO3--e-===N2O5
D. 石墨Ⅱ极上发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长期存放的亚硫酸钠可能会被空气中的氧气氧化。某化学兴趣小组通过实验来测定某无水亚硫酸钠试剂的质量分数,设计了如图所示实验装置:
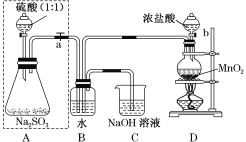
请回答下面的问题:
(1)若将虚线框内的分液漏斗换成长颈漏斗,则应该怎样检查虚线框内装置的气密性?________。
(2)D装置中反应的化学方程式为_________。B装置中反应的离子方程式为__________。
(3)称量a g Na2SO3样品放入锥形瓶中,向B装置反应后的溶液中加入足量的BaCl2溶液充分反应,过滤、洗涤、干燥,得白色沉淀b g,原样品中Na2SO3的质量分数为______。
(4)C装置中反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的叙述中正确的是( )
A.在SiO2晶体中,由Si、O构成的最小单元环中共有8个原子
B.在28g晶体硅中,含Si﹣Si共价键个数为4NA
C.金刚石的熔沸点高于晶体硅,是因为C﹣C键键能小于Si﹣Si键
D.镁型和铜型金属晶体的配位数均为12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com