
【题目】常用补钙片的有效成分是CaCO3,某化学探究小组欲测定某补钙片中碳酸钙的含量。查阅资料得知:
一种常用的分析试剂 EDTA二钠盐(用Na2H2Y2H2O表示)可用于测定Ca2+,其反应为:
Ca2++H2Y2-=CaY2-+2H+,以铬黑T为指示剂,滴定终点溶液由红色变为蓝色。于是该实验小组做了如下实验:
步骤一:配制待测溶液。取适量补钙片研碎后,准确称取0.400g配成250mL溶液。
步骤二:滴定。用移液管取待测液25.00mL于锥形瓶中,加入适量NaOH溶液,摇
匀,再加入铬黑T指示剂3滴,用0.0100molL1EDTA二钠盐溶液滴定至终点。三次重复滴定平均消耗EDTA二钠盐溶液22.50mL。
请回答下列问题:
(1)步骤一中补钙剂要用2mol/L的盐酸溶解,反应的离子方程式为__________________,配制待测溶液所必需的仪器除研钵、药匙、分析天平、称量瓶、烧杯、玻璃棒外,还有_______、________,操作的先后顺序为:e→____→____→d→f→____→____→____(填下列操作的序号)。
A.盐酸溶解 b.称量 c.定容摇匀 d.加蒸馏水稀释 e.研磨
f.用NaOH溶液调节溶液pH至7 g.转移溶液 h.洗涤并转移
(2)实验测得补钙片中CaCO3的含量为_______。
(3)下列操作会导致测定结果偏高的是_______(填下列选项的字母序号)。
A.未将洗涤烧杯内壁的溶液转入容量瓶
B.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
C.定容时俯视刻度线
D.滴定管下端尖嘴中有气泡存在,滴定后气泡消失
E.滴定管用蒸馏水洗净后未用标准液润洗
【答案】CaCO3+2H+=Ca2++CO2↑+H2O 250mL容量瓶 胶头滴管 b a g h c 56.3% CDE
【解析】
(1)步骤一中补钙剂要用2mol/L的盐酸溶解,碳酸钙和盐酸反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,配制待测溶液所必需的仪器除研钵、药匙、分析天平、称量瓶、烧杯、玻璃棒外,还有250mL容量瓶、胶头滴管,操作的先后顺序为:研磨→称量→盐酸溶解→加蒸馏水稀释→用NaOH溶液调节溶液pH至7→转移溶液→洗涤并转移→定容摇匀,即e→b→a→d→f→g→h→c;
(2)实验测得补钙片中CaCO3的物质的量为![]() ,CaCO3的含量为
,CaCO3的含量为![]() 56.3%;
56.3%;
(3)A.未将洗涤烧杯内壁的溶液转入容量瓶,碳酸钙质量偏小,导致测定结果偏低;
B.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水,测定结果无影响;
C.定容时俯视刻度线,溶液体积偏小,浓度偏大;
D.滴定管下端尖嘴中有气泡存在,滴定后气泡消失,消耗EDTA体积偏大,导致测定结果偏高;
E.滴定管用蒸馏水洗净后未用标准液润洗,使EDTA浓度偏小,消耗体积偏大,导致测定结果偏高;
故选CDE。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】按要求写出下列相关表达式:
(1)丙烯电子式:_________________
(2)顺-1,2 -二溴乙烯结构式:______________________。
(3)CH3CH2CHO+Cu(OH)2 +NaOH_____________________。
(4)![]() + H2(足量)_____________________________。
+ H2(足量)_____________________________。
(5)![]() + O2 → _____________________________________。
+ O2 → _____________________________________。
(6)CH3CH=C(CH3)2+HCl→__________________________________。
(7)2-丁烯加聚反应方程式:________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是( )

A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能用于做喷泉实验
C.HCl、NH3和SO2均能用该装置做喷泉实验
D.用NO2和N2O4的混合气体做喷泉实验,烧瓶中将充满稀硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉通过如图所示转化可以得到多种有机物:
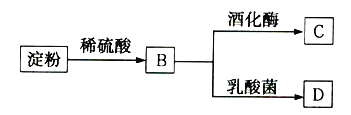
(1)检验淀粉是否完全水解,可以选用的试剂是__________(填序号)。
a.石蕊试液 b.淀粉碘化钾溶液 c.碘水
(2)B是一种单糖,则B的名称是____________________。
(3)B转化为C的化学方程式是______________________________。
(4)一分子B可在乳酸菌作用下分解生成两分子D,D与乙酸、乙醇均能发生酯化反应,且D的结构中含有甲基,则D的结构简式是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到目的的是( )

A.用灼烧的方法鉴别棉麻与真丝
B.加入浓溴水除去苯中溶解的杂质苯酚
C.用图甲装置制取并收集乙酸乙酯
D.用图乙装置验证溴乙烷与NaOH醇溶液共热产生了乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组对KSCN的性质进行探究,设计如下实验:
试管中试剂 | 实验 | 滴加试剂 | 现象 |
| Ⅰ | ⅰ.先加1mL 0.1mol/L FeSO4溶液 ⅱ.再加硫酸酸化的KMnO4溶液 | ⅰ.无明显现象 ⅱ.先变红,后褪色 |
Ⅱ | ⅲ.先加1mL 0.05mol/L Fe2(SO4)3溶液 ⅳ.再滴加0.5mL 0.5mol/L FeSO4溶液 | ⅲ.溶液变红 ⅳ.红色明显变浅 |
(1)SCN-存在两种结构式,分别为N≡C-S-和S=C=N-,SCN-是二者的互变异构的混合物,请写出N≡C-S-的电子式__________________________。
(2)用离子方程式表示FeSO4溶液显酸性的原因______________________。
(3)①用离子方程式表示实验Ⅰ溶液变红的原因___________。
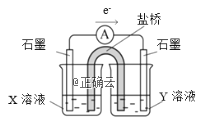
②针对实验Ⅰ中红色褪去的原因,小组同学认为是SCN-被酸性KMnO4氧化为SO42-,并设计如图实验装置证实了猜想是成立的。其中X溶液是_______,Y溶液是_______,检验产物SO42-的操作及现象是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常把原子总数和价电子总数相同的分子或离子称为等电子体,等电子体具有相似的化学结构,则下列有关说法中正确的是![]()
A.![]() 和
和![]() 是等电子体,化学键类型完全相同
是等电子体,化学键类型完全相同
B.![]() 和
和![]() 是等电子体,均为平面正三角形结构
是等电子体,均为平面正三角形结构
C.![]() 和
和![]() 是等电子体,均为三角锥形结构
是等电子体,均为三角锥形结构
D.![]() 和
和![]() 是等电子体,
是等电子体,![]() 和
和![]() 具有相同的化学性质
具有相同的化学性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为更有效处理工业废气中排放的氮氧化物(NOx)、SO2等,减少大气污染。科学家不断对相关反应进行研究尝试。
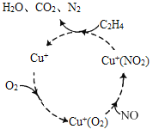
(1)脱硝反应机理如图,Cu+的作用是___,C2H4参与的反应方程式__。
(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g);ΔH=-1627kJmol-1
4N2(g)+6H2O(g);ΔH=-1627kJmol-1
①该方法应控制反应温度在315~400℃之间,反应温度不宜过高的原因是__。
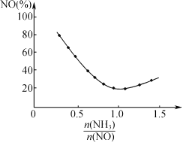
②氨氮比n(NH3)/n(NO)![]() 会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当
会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当![]() >1.0时,烟气中NO含量反而增大,主要原因是___。
>1.0时,烟气中NO含量反而增大,主要原因是___。
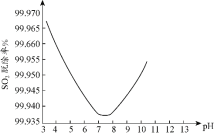
(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点。ClO2及NaClO2均是性能优良的脱硫脱硝试剂。
某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是___;在pH约7.8之后,随pH的增大,SO2脱除率又开始升高,其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①已知白磷和氯酸溶液可发生如下反应,将该反应进行配平:
______P4+_______HClO3+_______ ______=______HCl+____H3PO4
②白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
在该反应中30 mol CuSO4可氧化P4的物质的量是______mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com