
【题目】甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
(1)甲醇蒸汽完全燃烧的热化学方程式为_____________。
(2)反应②中的能量变化如下图所示,则△H2=______(用E1和E2表示)。

(3)H2(g)的燃烧热为__________ kJ· mol-1。
(4)请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:__________________(写出一点)
【答案】CH3OH(g)+![]() O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol; E1-E2 285.9 来源广、热值高、不污染环境
O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol; E1-E2 285.9 来源广、热值高、不污染环境
【解析】
(1)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(2)依据反应焓变△H=生成物总能量-反应物总能量分析;
(3)依据燃烧热的概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量,结合热化学方程式分析计算;
(4)根据氢能源的优点和氢能源的开发和利用的最新动向即可作答。
(1)①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
由盖斯定律②+①得到甲醇蒸气完全燃烧的热化学反应方程式为:CH3OH(g)+![]() O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol;
O2(g)═CO2(g)+2H2O(l)△H2=-764.7kJ/mol;
(2)反应②中的能量变化如图所示,依据图象分析,反应焓变△H=生成物总能量-反应物总能量,△H2=E1-E2;
(3)燃烧热的概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量,根据2H2(g)+O2(g)═2H2O(l) △H1=-571.8kJ/mol可知2mol氢气完全燃烧生成液态水放出的热量为571.8kJ,则1mol氢气完全燃烧生成液态水放出的热量为285.9kJ,故氢气燃烧热为285.9kJ/mol;
(4)地球上水资源丰富,可以从水中提取氢气,说明资源广泛;依据燃烧热计算分析,氢气的燃烧值高;因为氢气燃烧产物是水,不污染环境。


科目:高中化学 来源: 题型:
【题目】在2 L的密闭容器中,发生以下反应:2A(g)+B(g) ![]() 2C(g)+D(g),若最初加入的A和B都是4 mol,在前10 s A的平均反应速率为0.12 mol/(L·s),则10 s时,容器中B的物质的量是( )
2C(g)+D(g),若最初加入的A和B都是4 mol,在前10 s A的平均反应速率为0.12 mol/(L·s),则10 s时,容器中B的物质的量是( )
A.3.4 molB.3.2 molC.2.8 molD.1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是( )

A. HA是一种强酸
B. x点,c(A-)=c(B-)
C. HB是一种弱酸
D. 原溶液中HA的物质的量浓度为HB的10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛是一种重要的化工原料,常用于生产脲醛树脂及酚醛树脂,在木材加工中的地位及其重要。
(1)工业中甲醛的制备方法常用以下几种。
①甲醇氧化法
CH3OH(g)=HCHO(g)+H2(g) △H = +84kJ/mol
2H2(g)+O2(g)=2H2O(g) △H = -484kJ/mol
CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式是_______。
②天然气氧化法
在600-680℃下,使天然气(主要成分是CH4)和空气的混合物通过铁、钼等的氧化物催化剂,直接氧化生成甲醛。反应的化学方程式是_______。
(2)甲醛是污染室内环境的主要污染物,被称为室内污染“第一杀手”。
①去除甲醛有多种方法,其中,催化氧化法是一种比较高效的除甲醛方法。Na-Pt/TiO2催化剂催化氧化甲醛的反应机理如下图所示:
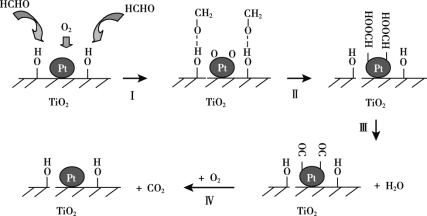
下列有关说法正确的是______(选填字母序号)。
a.该方法除去甲醛的化学方程式是:HCHO+O2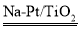 CO2+H2O
CO2+H2O
b.Na-Pt/TiO2催化剂能加快甲醛氧化速率,也能提高甲醛的转化率
c.反应过程中,HCHO只有部分化学键发生断裂
② 为测定居室中甲醛含量,将50L居室中气体缓缓通入25.00mL 0.01molL-1高锰酸钾酸性溶液中,使空气中的甲醛完全吸收,再用0.05molL-1H2C2O4溶液滴定,至终点时消耗H2C2O4溶液12.20mL 。
反应原理为:4MnO4—+12H++5HCHO=4Mn2++5CO2↑+11H2O
2MnO4— +6H++5H2C2O4=2Mn2++10CO2↑+8H2O
滴定终点的现象是_______。该室内空气中甲醛的含量是______mg/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氧化法制硝酸的主要反应是:4NH3(g) + 5O2(g) ![]() 4NO(g) + 6H2O(g)。
4NO(g) + 6H2O(g)。
(1)升高温度,反应的平衡常数K值减小,则该反应的焓变△H_____0(填“>”、“<”或“=”)。
(2)下列能说明上述反应已达到平衡状态__________(填序号)
A.NH3的浓度不随时间变化
B.v正(O2)= v逆(NO)
C.体系的分子总数不再变化
D.单位时间内消耗4molNH3的同时生成6molH2O
(3)若其他条件不变,下列关系图错误的是______(选填序号)。
A.  B.
B.  C.
C.  D.
D. 
(4)在容积固定的密闭容器中发生上述反应,容器内各物质的浓度如下表:
时间/浓度/(mol·L-1) | c(NH3) | c(O2) | c(NO) | c(H2O) |
起始 | 4.0 | 5.5 | 0 | 0 |
第 2 min | 3.2 | 0.8 | 1.2 | |
第 4 min | 2.0 | 3.0 | 2.0 | 3.0 |
第 6 min | 2.0 | 3.0 | 2.0 | 3.0 |
①上表中空白处应填的数字为______。
②反应在第 2 min 到第 4 min 时,反应速率v(O2)=___________。
③反应在第 2 min 时改变了条件,改变的条件可能______;该条件下,反应的平衡常数K=_______(只写计算结果,不标单位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图

下列叙述正确的是( )
A.迷迭香酸属于芳香烃
B.1 mol迷迭香酸最多能和9 mol氢气发生加成反应
C.迷迭香酸可以发生水解反应,取代反应和酯化反应
D.1 mol迷迭香酸最多能和含5 mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成导电高分子材料PPV的反应如下。下列说法正确的是( )
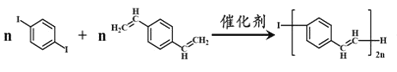 +(2n-1)HI
+(2n-1)HI
A.合成PPV的反应为加聚反应
B.1molPPV最多能与4 molH2发生加成反应
C. 与溴水加成后的产物最多有16个原子共平面
与溴水加成后的产物最多有16个原子共平面
D.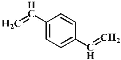 和苯乙烯互为同系物
和苯乙烯互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为电解饱和食盐水的简单装置,下列有关说法正确的是( )
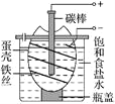
A.电解一段时间后,向蛋壳内的溶液中滴加几滴酚酞,呈红色
B.蛋壳表面缠绕的铁丝上发生氧化反应
C.铁丝表面生成的气体能使湿润的淀粉碘化钾试纸变蓝
D.蛋壳可阻止生成的氯气与氢气、氢氧化钠溶液接触
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以0.10mol/L的氢氧化钠溶液滴定同浓度某一元酸HA的滴定曲线如图所示(![]() )。下列表述错误的是( )
)。下列表述错误的是( )
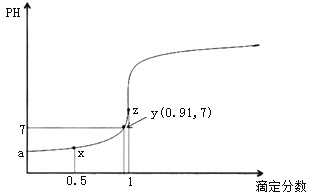
A.z点后存在某点,溶液中的水的电离程度和y点的相同
B.a约为3.5
C.z点处,![]()
D.x点处的溶液中离子满足:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com