
ΓΨΧβΡΩΓΩœ¬Ν–”–ΙΊΒγΫβ÷ »ή“Κ÷–ΝΘΉ”≈®Ε»ΙΊœΒ’ΐ»ΖΒΡ «Θ® Θ©
A.ΫΪ HCl ”κ CH3COONa ΝΫ»ή“ΚΜλΚœΚσΘ§»ή“Κ≥ ÷––‘Θ§‘ρ c(Na+) < c(ClΘ≠)
B.œρ NH4Cl »ή“Κ÷–Ά® NH3Θ§‘ρ c(![]() ) >c(ClΘ≠) > c(OHΘ≠)> c(H+)
) >c(ClΘ≠) > c(OHΘ≠)> c(H+)
C. “Έ¬œ¬Θ§c(![]() )œύΆ§ΒΡΔΌ(NH4)2CO3 ΔΎ(NH4)2SO4 Δέ(NH4)2Fe(SO4)2 »ή“Κ≈®Ε»¥σ–ΓΥ≥–ρΈΣΘΚΔΌ>ΔΎ>Δέ
)œύΆ§ΒΡΔΌ(NH4)2CO3 ΔΎ(NH4)2SO4 Δέ(NH4)2Fe(SO4)2 »ή“Κ≈®Ε»¥σ–ΓΥ≥–ρΈΣΘΚΔΌ>ΔΎ>Δέ
D.“―÷Σ pKa= Θ≠lgKaΘ§pKa(HF)=3.1Θ§pKa(C6H5COOH) = 4.2Θ§ “Έ¬œ¬Θ§Β»ΧεΜΐΓΔΒ»≈®Ε»ΒΡ NaFΓΔC6H5COONa »ή“Κ÷–Θ§«Α’ΏάκΉ”Ήή ΐ–Γ”ΎΚσ’Ώ
ΓΨ¥πΑΗΓΩC
ΓΨΫβΈωΓΩ
A. ΫΪHCl”κCH3COONaΝΫ»ή“ΚΜλΚœΚσΘ§ΗυΨί»ή“ΚΒγΚ… ΊΚψΒΡΒΟΒΫc(H+)ΘΪc(Na+)ΘΫ c(ClΘ≠) ΘΪc(OHΘ≠) ΘΪ c(CH3COOΘ≠)Θ§»ή“Κ≥ ÷––‘Φ¥c(H+)ΘΫc(OHΘ≠)Θ§‘ρ”–c(Na+)ΘΫc(ClΘ≠) ΘΪ c(CH3COOΘ≠)Θ§“ρ¥Υc(Na+)ΘΨc(ClΘ≠)Θ§Ι A¥μΈσΘΜ
B. œρNH4Cl»ή“Κ÷–Ά®NH3Θ§≤Μ«ε≥ΰ»ή“ΚΥαΦν–‘Θ§“ρ¥ΥΈόΖ®≈–Εœc(OHΘ≠)”κc(H+)¥σ–ΓΘ§Ι B¥μΈσΘΜ
C. ΔΌ(NH4)2CO3 «œύΜΞ¥ΌΫχΒΡΥΪΥ°ΫβΘ§Υ°Ϋβ≥ΧΕ»Ήν¥σΘΜΔΎ(NH4)2SO4 «ΒΞ“ΜοßΗυάκΉ”Υ°ΫβΘ§Υ°Ϋβ≥ΧΕ»–ΓΘΜΔέ(NH4)2Fe(SO4)2 «œύΜΞ“÷÷ΤΒΡΥΪΥ°ΫβΘ§Υ°Ϋβ≥ΧΕ»Ήν–ΓΘ§ “Έ¬œ¬Θ§c(![]() )œύΆ§Θ§Υ°Ϋβ≥ΧΕ»‘Ϋ¥σΘ§ΥΒΟς‘≠»ή“ΚΒΡ≈®Ε»‘Ϋ¥σΘ§“ρ¥ΥΔΌ(NH4)2CO3ΔΎ(NH4)2SO4Δέ(NH4)2Fe(SO4)2»ή“Κ≈®Ε»¥σ–ΓΥ≥–ρΈΣΘΚΔΌΘΨΔΎΘΨΔέΘ§Ι C’ΐ»ΖΘΜ
)œύΆ§Θ§Υ°Ϋβ≥ΧΕ»‘Ϋ¥σΘ§ΥΒΟς‘≠»ή“ΚΒΡ≈®Ε»‘Ϋ¥σΘ§“ρ¥ΥΔΌ(NH4)2CO3ΔΎ(NH4)2SO4Δέ(NH4)2Fe(SO4)2»ή“Κ≈®Ε»¥σ–ΓΥ≥–ρΈΣΘΚΔΌΘΨΔΎΘΨΔέΘ§Ι C’ΐ»ΖΘΜ
D. “―÷ΣpKa= Θ≠lgKaΘ§pKa(HF)=3.1Θ§pKa(C6H5COOH) = 4.2Θ§‘ρKa(HF)=1.0ΓΝ103.1Θ§Ka(C6H5COOH)=1.0ΓΝ104.2Θ§ΗυΨίΒγΚ… ΊΚψΘ§c(H+)ΘΪc(Na+)ΘΫc(OHΘ≠) ΘΪ c(FΘ≠)Θ§c(H+)ΘΪc(Na+)ΘΫc(OHΘ≠) ΘΪ c(C6H5COOΘ≠)Θ§‘ρΝΫ’ΏΒΡάκΉ”≈®Ε»÷°ΚΆΕΦΈΣ2c(H+)ΘΪ2c(Na+)Θ§ΡΤάκΉ”≈®Ε»ΕΦœύΆ§Θ§ΒΪ«βάκΉ”≈®Ε»ΝΫ’Ώ≤ΜœύΆ§Θ§ΗυΨίΕ‘”ΠΒΡΥα‘Ϋ»θΘ§Υ°Ϋβ≥ΧΕ»‘Ϋ¥σΘ§‘ρC6H5COONaΥ°Ϋβ≥ΧΕ»Ηϋ¥σΘ§Φν–‘Ηϋ«ΩΘ§»ή“Κ÷–ΒΡ«βάκΉ”≈®Ε»Ηϋ–ΓΘ§“ρ¥Υ “Έ¬œ¬Θ§Β»ΧεΜΐΓΔΒ»≈®Ε»ΒΡNaFΓΔC6H5COONa»ή“Κ÷–Θ§«Α’ΏάκΉ”Ήή ΐ¥σ”ΎΚσ’ΏΘ§Ι D¥μΈσΓΘ
Ήέ…œΥυ ωΘ§¥πΑΗΈΣCΓΘ


 Χτ’Ϋ100ΒΞ‘ΣΦλ≤β ‘ΨμœΒΝ–¥πΑΗ
Χτ’Ϋ100ΒΞ‘ΣΦλ≤β ‘ΨμœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ2020ΡξΜ·―ßΩΤ―ßΦ“”ΟΈΔ…ζΈο»ΦΝœΒγ≥ΊΉςΒγ‘¥Ϋχ––ΡΘΡβœϊ≥ΐΥα–‘ΙΛ“ΒΖœΥ°÷–ΒΡ÷ΊΗθΥαΗυάκΉ”(Cr2O72-)ΒΡ Ψ“βΆΦ»γΆΦΥυ ΨΘ§Ζ¥”Π“ΜΕΈ ±ΦδΚσΘ§‘ΎΉΑ÷ΟΔΎ÷–ΒΟΒΫFe(OH)3ΚΆCr(OH)3ΝΫ÷÷≥ΝΒμΓΘ“―÷Σ6Fe2++ Cr2O72-+14H+=6Fe3++2Cr3++7H2OΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©

A.ΉΑ÷ΟΔΌ÷–Θ§aΦΪΒΡΒγΦΪΖ¥”ΠΈΣHS--8e-+4H2O=SO42-+9H+
B.œρΉΑ÷ΟΔΎ÷–Φ”»κ ΝΩNa2SO4Θ§Τδ÷ς“ΣΉς”Ο «‘ω«Ω»ή“ΚΒΡΒΦΒγ–‘
C.ΉΑ÷ΟΔΌ÷–Θ§bΦΪ…œœϊΚΡΒΡn(O2)”κΉΑ÷ΟΔΎ÷–Εη–‘ΒγΦΪ…œ…ζ≥…ΒΡn(…ζ≥…Έο)œύΒ»
D.Β±ΉΑ÷ΟΔΌ÷–”–0.6mol H+Ά®Ιΐ÷ Ή”ΫΜΜΜΡΛ ±Θ§ΉΑ÷ΟΔΎ÷–≤ζ…ζ0.4mol≥ΝΒμ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬ΆΦ÷–ΒΡ«ζœΏΖ÷±π±μ Ψ‘ΣΥΊΒΡΡ≥÷÷–‘÷ ”κΚΥΒγΚ… ΐΒΡΙΊœΒ(ZΈΣΚΥΒγΚ… ΐΘ§YΈΣ‘ΣΥΊΒΡ”–ΙΊ–‘÷ )ΘΚ
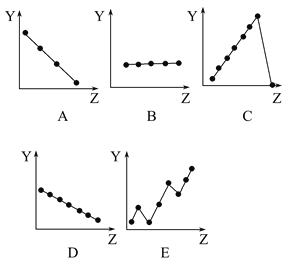
Α―”κ‘ΣΥΊ”–ΙΊ–‘÷ œύΖϊΒΡ«ζœΏΒΡ±ξΚ≈Χν»κœύ”Πά®Κ≈÷–ΘΚ
Θ®1Θ©ΔρAΉε‘ΣΥΊ‘≠Ή”ΒΡΦέΒγΉ” ΐ___________ΘΜ
Θ®2Θ©ΒΎ»ΐ÷ήΤΎ‘ΣΥΊΒΡΉνΗΏ’ΐΜ·ΚœΦέ___________ΘΜ
Θ®3Θ©FΘ≠ΓΔNaΘΪΓΔMg2ΘΪΓΔAl3ΘΪΥΡ÷÷άκΉ”ΒΡάκΉ”ΑκΨΕ___________ΘΜ
Θ®4Θ©ΒΎΕΰ÷ήΤΎ‘ΣΥΊΒΡ‘≠Ή”ΑκΨΕ(≤ΜΑϋά®œΓ”–ΤχΧε) ___________ΘΜ
Θ®5Θ©ΒΎΕΰ÷ήΤΎ‘ΣΥΊΒΡΒΎ“ΜΒγάκΡή ___________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύœ¬Ν–Ης»ή“Κ÷–Θ§άκΉ”“ΜΕ®Ρή¥σΝΩΙ≤¥φΒΡ «Θ® Θ©
A.«ΩΦν–‘»ή“Κ÷–ΘΚK+ΓΔAl3+ΓΔCl-ΓΔSO![]()
B. “Έ¬œ¬Θ§pHΘΫ1ΒΡ―ΈΥα÷–ΘΚNa+ΓΔFe2+ΓΔNO![]() ΓΔSO
ΓΔSO![]()
C.Κ§”–Ca2+ΒΡ»ή“Κ÷–ΘΚNa+ΓΔK+ΓΔCO![]() ΓΔCl-
ΓΔCl-
D.Υ°Βγάκ≤ζ…ζΒΡcΘ®H+Θ©ΘΫ1x10-13 mol/LΒΡ»ή“Κ÷–ΘΚNa+ΓΔK+ΓΔCl-ΓΔSO![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Ά§―ß”ϊάϊ”Ο»γΆΦΉΑ÷Ο÷Τ»ΓΡήΫœ≥Λ ±Φδ¥φ‘ΎΒΡFe(OH)2Θ§Τδ÷– Β―ιΥυ”Ο»ή“Κœ÷≈δœ÷”Ο«“’τΝσΥ°œ»Φ”»»÷σΖ–ΓΘœ¬Ν–Ζ÷Έω’ΐ»ΖΒΡ «

A. XΩ…“‘ «œΓΝρΥαΜρœΓœθΥαΜρœΓ―ΈΥα
B. Β―ιΩΣ Φ ±”Πœ»ΙΊ±’÷ΙΥ°Φ–aΓΔ¥ρΩΣbΘ§‘Όœρ…’ΤΩ÷–Φ”»κX
C. Ζ¥”Π“ΜΕΈ ±ΦδΚσΩ…‘Ύ…’ΤΩ÷–Ιέ≤λΒΫΑΉ…Ϊ≥ΝΒμ
D. Ζ¥”ΠΫα χΚσ»τΙΊ±’bΦΑΖ÷“Κ¬©ΕΖΜν»ϊΘ§‘ρFe(OH)2Ω…Ϋœ≥Λ ±Φδ¥φ‘Ύ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–±μ ω÷–’ΐ»ΖΒΡ « ( )
A.»ΈΚΈΡή ΙλΊ÷Β‘ω¥σΒΡΙΐ≥ΧΕΦΡήΉ‘ΖΔΫχ––
B.“―÷Σ»»Μ·―ßΖΫ≥Χ Ϋ2SO2(g)ΘΪO2(g)![]() 2SO3(g)ΠΛHΘΫΘ≠Q kJΓΛmolΘ≠1(QΘΨ0)Θ§‘ρΫΪ2 mol SO2(g)ΚΆ1 mol O2(g)÷Ο”Ύ“ΜΟή±’»ίΤς÷–≥δΖ÷Ζ¥”ΠΚσΖ≈≥ωQ kJΒΡ»»ΝΩ
2SO3(g)ΠΛHΘΫΘ≠Q kJΓΛmolΘ≠1(QΘΨ0)Θ§‘ρΫΪ2 mol SO2(g)ΚΆ1 mol O2(g)÷Ο”Ύ“ΜΟή±’»ίΤς÷–≥δΖ÷Ζ¥”ΠΚσΖ≈≥ωQ kJΒΡ»»ΝΩ
C.Μ·―ßΤΫΚβΖΔ…ζ“ΤΕ·Θ§ΤΫΚβ≥Θ ΐ“ΜΕ®ΖΔ…ζ±δΜ·
D.1 mol NaOHΖ÷±πΚΆ1 mol CH3COOHΓΔ1 mol HNO3Ζ¥”ΠΘ§Κσ’Ώ±»«Α’ΏΖ≈≥ωΒΡ»»ΝΩΕύ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γΆΦΥυ ΨΘ§…’±≠ΡΎ Δ”–≈®œθΥαΘ§‘Ύ…’±≠ΡΎΖ≈»κ”ΟΒΦœΏΝ§Ϋ”ΒΡΧζΓΔ«ΠΝΫΗωΒγΦΪΘ§“―÷Σ‘≠Βγ≥ΊΆΘ÷ΙΙΛΉς ±Θ§FeΓΔPbΨυ”– Θ”ύΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
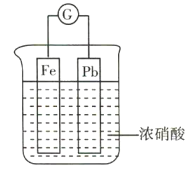
A.Fe±»PbΜνΤΟΘ§Ι Fe Φ÷’ΉςΗΚΦΪ
B.Fe‘Ύ≈®œθΥα÷–ΕέΜ·Θ§Ι Φ÷’≤Μ»ήΫβ
C.‘≠Βγ≥ΊΆΘ÷ΙΙΛΉς ±Θ§»ή“Κ÷–”–![]()
D.άϊ”Ο≈®œθΥαΉςΒγΫβ÷ »ή“Κ≤ΜΖϊΚœΓΑ¬Χ…ΪΜ·―ßΓ±ΒΡΥΦœκ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΒΣΓΔΗθΦΑΤδœύΙΊΜ·ΚœΈο”ΟΆΨΖ«≥ΘΙψΖΚΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΜυΧ§N‘≠Ή”ΒΡΚΥΆβΒγΉ”≈≈≤Φ ΫΈΣ___Θ§CrΈΜ”Ύ‘ΣΥΊ÷ήΤΎ±μΒΎΥΡ÷ήΤΎ___ΉεΓΘ
(2) Cr”κKΈΜ”ΎΆ§“Μ÷ήΤΎ«“ΉνΆβ≤ψΒγΉ” ΐœύΆ§Θ§ΝΫ÷÷‘ΣΥΊ‘≠Ή”ΒΎ“ΜΒγάκΡήΒΡ¥σ–ΓΙΊœΒΈΣ___ΘΜCrcl3ΒΡ»έΒψ(83Γφ)±»CrF3ΒΡ»έΒψ(1100Γφ)ΒΆΒΟΕύΘ§’β «“ρΈΣ___ΓΘ
(3) CrΒΡ“Μ÷÷≈δΚœΈοΫαΙΙ»γΆΦΥυ ΨΘΚ

ΔΌ“θάκΉ”C1O4Θ≠ΒΡΩ’ΦδΙΙ–ΆΈΣ___–ΈΓΘ
ΔΎ≈δάκΉ”÷–Θ§÷––ΡάκΉ”ΒΡ≈δΈΜ ΐΈΣ___Θ§N”κ÷––Ρ‘≠Ή”–Έ≥…ΒΡΜ·―ßΦϋ≥ΤΈΣ___ΦϋΓΘ
Δέ≈δΧεH2 NCH2 CH2 NH2(““ΕΰΑΖ)÷–ΧΦ‘≠Ή”ΒΡ‘”Μ·ΖΫ Ϋ «______ Θ§Ζ÷Ή”÷–»ΐ÷÷‘ΣΥΊΒγΗΚ–‘¥”¥σΒΫ–ΓΒΡΥ≥–ρΈΣ___
(4)ΒΣΜ·ΗθΒΡ»έΒψΈΣ1770ΓφΘ§ΥϋΒΡ“Μ÷÷ΨßΧεΒΡΨßΑϊΫαΙΙ»γΆΦΥυ ΨΘ§ΤδΟήΕ»ΈΣ5. 9 gΓΛcm Θ≠3Θ§ΒΣΜ·ΗθΒΡΨßΑϊ±Ώ≥ΛΈΣ___(Ν–≥ωΦΤΥψ Ϋ)nm.

≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΜ«θΘ¬»Θ®SO2Cl2Θ© «“Μ÷÷”–Μ欻̷ΦΝΘ§“≤ «ο°Βγ≥Ί’ΐΦΪΜν–‘Έο÷ ΓΘ“―÷ΣΜ«θΘ¬» «“Μ÷÷Έό…Ϊ“ΚΧεΘ§»έΒψ-54.1ΓφΘ§Ζ–Βψ69.1ΓφΘ§”ωΥ°ΖΔ…ζΨγΝ“Υ°ΫβΓΘ
Θ®1Θ©“―÷ΣΘΚSO2(g) +Cl2(g)+ SCl2(g)![]() 2SOCl2(g) ΓςH=a kJΓΛmol-1
2SOCl2(g) ΓςH=a kJΓΛmol-1
SO2Cl2(g)+ SCl2(g)![]() 2SOCl2(g) ΓςH=b kJΓΛmol-1
2SOCl2(g) ΓςH=b kJΓΛmol-1
‘ρΖ¥”ΠΘΚSO2(g) + Cl2(g)![]() SO2Cl2(g) ΓςH =______kJΓΛmolΘ≠1Θ®”ΟΚ§aΓΔbΒΡ¥ζ ΐ Ϋ±μ ΨΘ©ΘΜΗΟΖ¥”ΠΤΫΚβ≥Θ ΐ±μ¥ο ΫΈΣK =______ΓΘ
SO2Cl2(g) ΓςH =______kJΓΛmolΘ≠1Θ®”ΟΚ§aΓΔbΒΡ¥ζ ΐ Ϋ±μ ΨΘ©ΘΜΗΟΖ¥”ΠΤΫΚβ≥Θ ΐ±μ¥ο ΫΈΣK =______ΓΘ
Θ®2Θ©Μ«θΘ¬»Ω…”κΑΉΝΉΖΔ…ζΖ¥”ΠΈΣΘΚP4+ 10SO2Cl2= 4PCl5+ 10SO2ΓϋΘ§»τ…ζ≥…1molSO2Θ§‘ρΉΣ“ΤΒγΉ”ΒΡΈο÷ ΒΡΝΩΈΣ_____molΓΘ
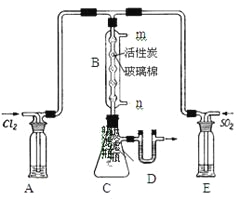
Θ®3Θ©Ρ≥―ßœΑ–ΓΉιΒΡΆ§―ß“άΨίΖ¥”ΠΘΚSO2(g)+ Cl2(g)![]() SO2Cl2(g) ΓςH ΘΦ0Θ§…ηΦΤΒΡ÷Τ±ΗΜ«θΘ¬»ΉΑ÷Ο»γΆΦΓΘ
SO2Cl2(g) ΓςH ΘΦ0Θ§…ηΦΤΒΡ÷Τ±ΗΜ«θΘ¬»ΉΑ÷Ο»γΆΦΓΘ
![]()
![]()
ΔΌ»τ”Ο≈®―ΈΥα”κΕΰ―θΜ·ΟΧΈΣ‘≠Νœ÷Τ»ΓCl2Θ§ΤδΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_____ΓΘ
ΔΎ…œΆΦΥυ ΨΒΡΉΑ÷ΟΥΒΖ®’ΐ»ΖΒΡ «_____Θ®≤ΜΕ®œν―Γ‘ώΘ©ΓΘ
a.AΓΔE¥Πœ¥ΤχΤΩ÷– ΔΖ≈ΒΡΩ…ΡήΖ÷±π «±ΞΚΆ ≥―ΈΥ°ΚΆ±ΞΚΆNa2SO3»ή“Κ
b.B¥ΠΖ¥”ΠΙήΡΎΈε«ρ÷–≤ΘΝßΟό…œΒΡΜν–‘ΧΩΉς¥ΏΜ·ΦΝ
c.B¥ΠΖ¥”ΠΙήά以հ”Π¥”mΫ”ΩΎΆ®»κ
d.ΉΑ÷ΟC¥ΠΈϋ¬ΥΤΩ”ΠΖ≈‘Ύ±υΥ°÷–ά以
e.D¥ΠU–ΈΙή÷– ΔΖ≈ΒΡΩ…Ρή «Φν ·Μ“
Δέ¥”Μ·―ßΤΫΚβ“ΤΕ·Ϋ«Ε»Ζ÷ΈωΘ§Ζ¥”ΠΙήΆ®Υ°ά以ΒΡΡΩΒΡΈΣ______ΓΘ
Θ®4Θ©GETΙΪΥΨΩΣΖΔΒΡLi-SO2Cl2Ψϋ”ΟΒγ≥ΊΘ§Τδ Ψ“βΆΦ»γΆΦΥυ ΨΘ§
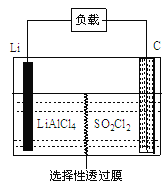
“―÷ΣΒγ≥ΊΖ¥”ΠΈΣΘΚ2Li + SO2Cl2=" 2LiCl" + SO2ΓϋΘΜ‘ρΒγ≥ΊΙΛΉς ±Θ§’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ_______ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com