
【题目】恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是
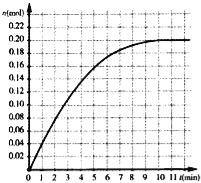
A.其它条件不变,若改用5L容器达到平衡需要的时间将大于10min
B.N2平衡转化率为25%
C.平衡时气体总压强为开始时的90%
D.反应前10min反应速率v(H2)=0.01molL﹣1min﹣1
【答案】D
【解析】
A.体积变大浓度减小,反应速率减慢,达平衡所需时变长,所以平衡需要的时间大于l0min,故A正确;
B. N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
起始量(mol):0.4 1.6 0
变化量(mol):0.1 0.3 0.2
平衡量(mol):0.3 1.3 0.2
所以N2平衡转化率为:![]() ×100%=25%,故B正确;
×100%=25%,故B正确;
C.平衡时气体总压强为开始时压强的倍数为:![]() ×100%=90%,故C正确;
×100%=90%,故C正确;
D.反应前l0min反应速率v(NH3)= =0.01molL﹣1min﹣1,所以v(H2)=
=0.01molL﹣1min﹣1,所以v(H2)=![]() v(NH3)=
v(NH3)=![]() ×0.01molL﹣1min﹣1=0.015molL﹣1min﹣1,故D错误;
×0.01molL﹣1min﹣1=0.015molL﹣1min﹣1,故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】铋为第五周期VA族元素,利用湿法冶金从辉铋矿(含Bi2S3、Bi、Bi2O3等)提取金属铋的工艺流程如下图所示:
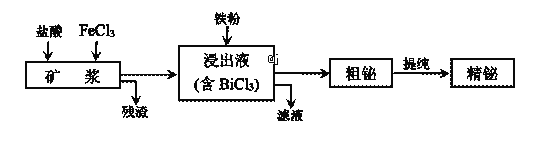
已知:BiCl3水解的离子方程式为:BiCl3+H2O![]() BiOCl+2H++2Cl-。
BiOCl+2H++2Cl-。
(1)矿浆浸出时加入盐酸的作用是______________。
(2)浸出时,Bi溶于FeCl3溶液的化学方程式为________________。
(3)残渣中含有一种单质,该单质是_______________。
(4)精辉铋矿中含有Ag2S,被氧化溶解后不会进入浸出液,银元素以___________(填化学式)进入残渣中。
(5)粗铋提纯时,阴极的电极反应式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp(AgCl)=1.8×10—10,Ksp(AgI)=1.5×10—16 ,Ksp(Ag2CrO4)=2.0×10—12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是 ( )
A.AgCl>AgI> Ag2CrO4B.AgCl> Ag2CrO4>AgI
C.Ag2CrO4>AgI>AgClD.Ag2CrO4>AgCl>AgI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是______(填字母代号),负极Zn发生了_____反应(填“氧化”或“还原”)。
(2)将纯锌片和纯铜片按如图所示方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是_______(填字母代号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲______乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置负极的电极反应式___________。
④当乙中产生1.12 L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B发生反应:
3A(g)+2B(g)![]() 4C(s)+2D(g),5min后达到平衡,测得生成1.6 mol C,则下列说法正确的是
4C(s)+2D(g),5min后达到平衡,测得生成1.6 mol C,则下列说法正确的是
A. 该反应的化学平衡常数表达式是K=![]()
B. 此时,B的平衡转化率是40%
C. 增大该体系的压强,平衡向右移动,化学平衡常数增大
D. 若向平衡体系中加入少量C,则正、逆反应速率均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在室温时纯水中存在电离平衡:H2O![]() H++OH-。下列叙述正确的是( )
H++OH-。下列叙述正确的是( )
A. 向水中加入少量NH4Cl,由水电离出的c(H+)>1×10-7mol/L
B. 升高温度,水的电离程度增大,c(H+)增大,pH<7,所以溶液显酸性
C. 向水中加入氨水,平衡逆向移动,水的电离受到抑制,所以c(OH-)降低
D. 向水中加入少量硫酸,c(H+)增大,所以由水电离出的c(H+)>1×10-7mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温条件下,将一定量![]() 和
和![]() 的混合气体通入一容积为2L的密闭容器中,测得各物质的浓度随时间变化关系如图所示.下列说法正确的是
的混合气体通入一容积为2L的密闭容器中,测得各物质的浓度随时间变化关系如图所示.下列说法正确的是![]()
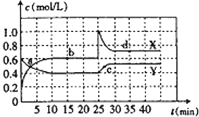
A.图中的两条曲线中,Y是表示![]() 浓度随时间的变化曲线
浓度随时间的变化曲线
B.前10min内,用![]() 表示的化学反应速率为
表示的化学反应速率为![]()
C.在25min时,反应改变的条件是增大了![]() 的浓度
的浓度
D.a、b、c、d四个点中,有a、b、d点的化学反应处于平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列图像的描述正确的是
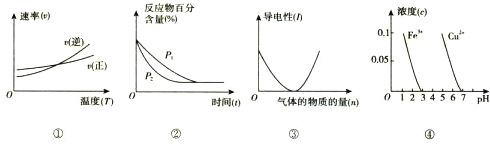
A. 根据图①判断反应A2(g)+3B2(g) ![]() 2AB3(g)的 △H>0
2AB3(g)的 △H>0
B. 图②可表示压强(P)对反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响
3C(g)+D(s)的影响
C. 图③可表示向醋酸溶液通入氨气时,溶液导电性随氨气量的变化
D. 根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某种苯的同系物0.1mol在足量的氧气中完全燃烧,将产生的高温气体依次通过浓硫酸和氢氧化钠溶液,使浓硫酸增重9g,氢氧化钠溶液增重35.2g。该有机物的分子式为______。
Ⅱ.为了证明溴乙烷中存在溴原子,某同学设计如下实验:
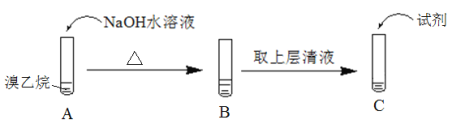
①将试管C中加入的试剂及相应的实验现象补充完整:_________。
②溴乙烷在NaOH水溶液中反应的化学方程式是_____________。
Ⅲ.为实现以下各步转化,请在下列括号中填入适当试剂。______、______
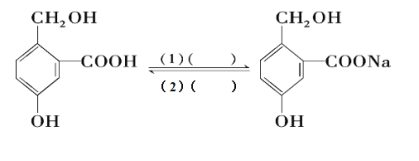
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com