
【题目】阿托酸是一种常用的医药中间体,其结构如图所示.下列关于阿托酸的说法正确的是( ) 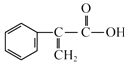
A.分子式为C9H10O2
B.能发生取代、加聚、氧化等反应
C.不能与Na2CO3溶液反应放出气体
D.1 mol阿托酸最多能和5 mol Br2发生加成反应
科目:高中化学 来源: 题型:
【题目】按如图1所示装置进行铁和水蒸气反应的实验. 
(1)铁粉与水蒸气反应的化学方程式是:;
(2)为检验生成的气体产物,需从下图选择必要的装置,其正确的连接顺序为(用接口字母表示)a﹣ fgbch , 描述能验证气体产物的实验现象; 
(3)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应,过滤.简述检验所得滤液中Fe3+的操作方法:;
(4)经检验上述滤液中不含Fe3+ , 这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁.原因是(用离子方程式说明):;
(5)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色.
①沉淀由白色变为红褐色的化学方程式是:;
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有同学设计如图2所示的装置:通电后,溶液中产生大量的白色沉淀,且较长时间不变色.下列说法中正确的是(填序号).
A.电源中的a为正极,b为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是2H++2e﹣═H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,试管②中一定观察不到的现象是( )
选项 | a | b | c | 试管②中现象 |
|
A | NaOH溶液 | Al | 肥皂水 | 肥皂泡可点燃 | |
B | 稀盐酸 | 碳酸钙 | NaAlO2溶液 | 生成白色絮状沉淀生成 | |
C | 稀硫酸 | NaHCO3 | BaCl2溶液 | 溶液变浑浊 | |
D | 水 | Na2O2 | 酸化的FeSO4溶液 | 溶液变黄 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施中能减慢食品的腐败,延长其保质期的是( )
①降温冷冻 ②用食盐腌制 ③加热烘干 ④适当地使用防腐剂
A.①②
B.④
C.①②④
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氢化物的叙述中正确的是( )
A.稳定性:H2S>HF
B.HCl的电子式为 ![]()
C.一个D2O分子所含的中子数为8
D.在卤化氢中HF最稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们生活质量的提高,废电池必须进行集中处理的问题提到议事日程,其主要原因是
A. 利用电池外壳的金属材料
B. 防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C. 不使电池中渗泄的电解液腐蚀其他物品
D. 回收其中石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MO2受热分解为+4和+2价的混合氧化物,+4价的M能氧化浓盐酸生成Cl2 , 将1mol MO2加热分解得到O2 , 再向残余固体中加入过量的浓盐酸得到Cl2 , 所得 O2和Cl2物质的量之比为3:2,则残余固体的组成及物质的量之比可能是( )
A.M3O4、MO 1:1
B.MO2、MO 3:1
C.M3O4、MO2 2:1
D.MO2、MO 1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石灰水保存鲜蛋是一种化学保鲜法。石灰水能保存鲜蛋的原理是( )
①石灰水具有强碱性,杀菌能力强 ②Ca(OH)2能与鲜蛋呼出的CO2反应,生成CaCO3薄膜,起保护作用 ③石灰水是电解质溶液,能使蛋白质凝聚 ④石灰水能渗入蛋内中和酸性物质
A.①②
B.③④
C.②④
D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:P4(g)+6Cl2(g)═4PCl3(g)△H=a kJmol﹣1 , P4(g)+10Cl2(g)═4PCl5(g)△H=bkJmol﹣1 , P4具有正四面体结构,PCl5中P﹣Cl键的键能为c kJmol﹣1 , PCl3中P﹣Cl键的键能为1.2c kJmol﹣1 . 下列叙述正确的是( )
A.P﹣P键的键能大于P﹣Cl键的键能
B.可求Cl2(g)+PCl3(g)═PCl5(s)的反应热△H
C.Cl﹣Cl键的键能为 (b﹣a+5.6c)/4 kJmol﹣1
D.磷元素的非金属性比氯强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com